1. AM:光誘發的納米藥物用于提高遞送效果和增強癌癥免疫治療
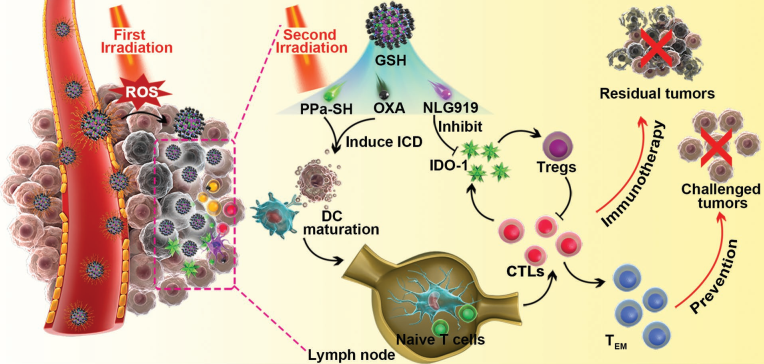
通過全身給藥的方式進行的化學-免疫治療往往存在著腫瘤特異性低、副作用嚴重等諸多問題。盡管目前利用納米顆粒進行協同遞送的策略可以對其進行改善,但實體腫瘤的病理生理屏障還是會影響載藥納米顆粒的積累和滲透腫瘤的效果。中科院上海藥物研究所于海軍研究員和李亞平研究員合作報道了一種光誘發的免疫治療納米藥物(LINC)。LINC由光敏劑脫鎂葉綠酸 a (PPa)和吲哚胺2,3-雙加氧酶1 (IDO-1)抑制劑NLG919構建的異二聚體以及光激活前藥奧沙利鉑(OXA)所組成。
在被靜脈注射后,LINC會在腫瘤部位積累并產生近紅外(NIR)熒光信號。而在熒光成像的指導下,利用第一次近紅外激光照射會誘導生成活性氧(ROS)并使得聚乙二醇(PEG)冠層發生裂解,從而提高LINC在腫瘤的保留和穿透的效果。而在第二次近紅外激光的照射下,LINC可以有效地激發免疫反應,促進細胞毒性T淋巴細胞(CTL)在腫瘤內的浸潤。此外,LINC還可以由NLG919去抑制IDO-1的活性進而逆轉免疫抑制的腫瘤微環境,因此LINC可以通過化學-免疫聯合治療抑制腫瘤的生長、肺轉移和復發。
Bing Feng, Haijun Yu, Yaping Li. et al. Self-Amplified Drug Delivery with Light-Inducible Nanocargoes to Enhance Cancer Immunotherapy. Advanced Materials. 2019
DOI: 10.1002/adma.201902960
https://onlinelibrary.wiley.com/doi/10.1002/adma.201902960
2. Small:黑磷納米片組成的多功能納米水凝膠用于促進骨的形成
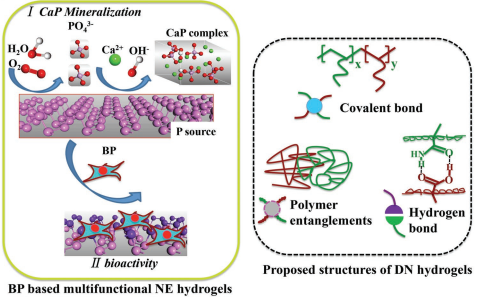
水凝膠因具有可調力學性能、化學成分和生物信號而可以模擬細胞外基質(ECM)環境,因此在組織工程領域受到了廣泛的關注。深圳市人民醫院楊大志教授、彭松林博士和暨南大學張榮華教授合作制備了一種具有可調力學性能的新型雙網(DN)水凝膠,并在其中加入了超薄的二維黑磷納米片,用于模擬ECM微環境并誘導組織再生。
實驗結果發現,BP納米片具有誘導CaP晶體形成的性能,因此可以提高NE水凝膠的礦化能力。體內外數據表明,該水凝膠材料可以為成骨細胞的分化和骨再生提供良好的ECM微環境。因此,這一工作也為開發用于骨組織再生的新型生物材料提供了新的方法。
Zhenming Wang, Ronghua Zhang, Dazhi Yang, Songlin Peng. et al. Multifunctional Nanoengineered Hydrogels Consisting of Black Phosphorus Nanosheets Upregulate Bone Formation. Small. 2019
DOI: 10.1002/smll.201901560
https://onlinelibrary.wiley.com/doi/10.1002/smll.201901560
3. Nano Lett.:利用熒光納米傳感器對細胞釋放的血清素進行近紅外成像
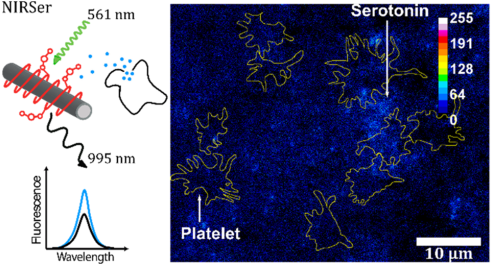
血清素是一種重要的神經遞質,它會影響并參與神經、血液和免疫系統的各種功能環節。但是目前利用傳統的傳感器對血清素等小生物分子進行高分辨率的實時檢測還十分困難。
哥廷根大學Sebastian Kruss團隊設計了一種基于熒光單分子碳納米管(SWCNTs)的近紅外(NIR)熒光納米傳感器(NIRSer)來對人類血小板釋放的血清素進行實時成像。該納米傳感器由單壁碳納米管(SWCNT)作為骨架,并連接有可結合血清素的DNA適配體。結果表明,NIRSer可以在單細胞水平上對活化血小板的血清素釋放模式進行檢測,并且具有很好的時空分辨率。
Meshkat Dinarvand, Sebastian Kruss. et al. Near-Infrared Imaging of Serotonin Release from Cells with Fluorescent Nanosensors. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b02865
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b02865
4. AM綜述:可釋放一氧化氮的生物材料用于對干細胞微環境進行調控
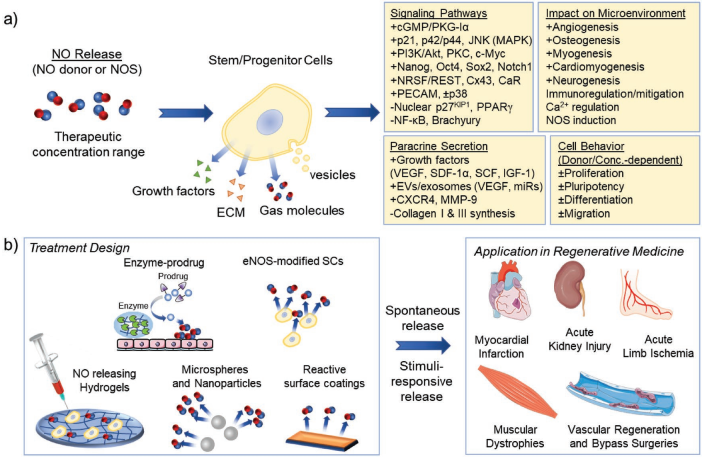
干細胞療法已被證明是治療退行性疾病損傷的一個有效方案。但是,細胞的移植不佳和其在損傷組織部位的存活能力差也嚴重影響了干細胞治療的臨床應用。一氧化氮(NO)是一種參與多種生理過程的重要信號分子。已有研究表明,NO在調節干細胞的行為例如存活、遷移、分化和旁分泌促再生因子等方面具有重要的作用。
因此,利用可控制生成或釋放NO以及支持干細胞遞送的生物材料進行聯合治療,有望協同增強和提高組織再生修復的效果。南開大學趙強教授團隊對目前用于遞送釋放NO并增強干細胞介導的損傷組織再生治療的平臺的最新研究進展進行了綜述,并對這些生物材料調控干細胞微環境的機制做了重點說明。
Adam C. Midgley, Qiang Zhao. et al. Nitric-Oxide-Releasing Biomaterial Regulation of the Stem Cell Microenvironment in Regenerative Medicine. Advanced Materials. 2019
DOI: 10.1002/adma.201805818
https://onlinelibrary.wiley.com/doi/10.1002/adma.201805818
5. AM:被腫瘤微環境激活的、納米酶介導的納米反應器用于腫瘤診療
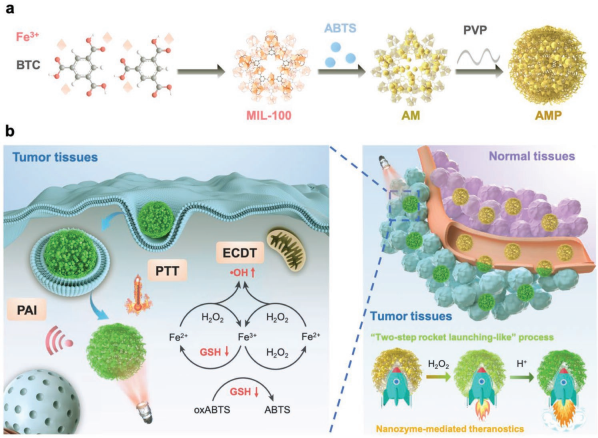
可被腫瘤微環境激活的納米診療試劑往往具有很高的特異性和敏感度。中科院長春應化所田華雨研究員和陳學思研究員合作開發了一種可被激活的、納米酶介導的、負載有ABTS的納米反應器ABTS@MIL-100/聚乙烯吡咯烷酮(AMP NRs),并將其用于成像指導的腫瘤聯合治療。
該AMP NRs可以通過納米酶介導的兩步過程被腫瘤微環境特異性地激活,從而產生光聲成像和光熱治療(PTT)的功能。此外, AMP NRs也可以對腫瘤微環境內高水平的H2O2做出響應并產生羥基自由基,并且可以破壞細胞內的谷胱甘肽(GSH)來進一步增強AMP NRs的化學動力學治療效果。由于AMP NRs會被腫瘤微環境特異性地激活,因此它對正常組織具有很好的安全性。這一研究也為開發有納米酶參與的納米反應器以實現智能高效的癌癥診療應用開辟了一條新的途徑。
Feng Liu, Huayu Tian, Xuesi Chen. et al. A Tumor-Microenvironment-Activated Nanozyme-Mediated Theranostic Nanoreactor for Imaging-Guided Combined Tumor Therapy. Advanced Materials. 2019
DOI: 10.1002/adma.201902885
https://onlinelibrary.wiley.com/doi/10.1002/adma.201902885
6. Adv. Sci.綜述:心血管支架在未來的發展趨勢
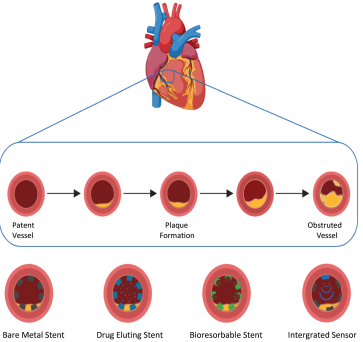
心血管疾病是造成人類死亡的最主要原因,而動脈粥樣硬化則是占其中的三分之二。這種疾病是由于不良的飲食習慣、高血壓和遺傳等因素引起的,并且肥胖、糖尿病和久坐不動的生活方式也會加重這種疾病。目前,利用藥物去治療動脈粥樣硬化的策略仍不能夠有效地控制疾病,因此往往需要采用臨床干預措施,例如使用可擴張的金屬支架進行治療。
但是這種方法也會產生支架內再狹窄,使得支架內血管被重新阻塞住。格拉斯哥大學John Mercer團隊綜述了目前支架技術和克服支架內再狹窄的生物傳感裝置的最新研究進展;對將由納米技術開發的新的傳感策略以及生物傳感器集成到支架內的研究做了介紹;詳細討論了植入式醫療設備的前景和未來的發展趨勢。
Daniel Hoare, John Mercer. et al. The Future of Cardiovascular Stents: Bioresorbable and Integrated Biosensor Technology. Advanced Science. 2019
DOI: 10.1002/advs.201900856
https://onlinelibrary.wiley.com/doi/10.1002/advs.201900856
7. Nature. Commun.:納米凝膠用于重塑腫瘤微環境并防止腫瘤轉移和復發
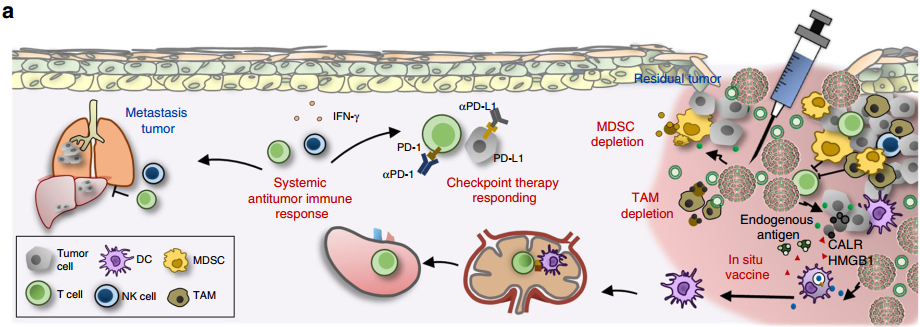
腫瘤免疫治療的效果不佳往往是由于腫瘤微環境(TME)中存在少量抗原特異性T細胞和大量的免疫抑制因子。韓國成均館大學Yong Taik Lim團隊、韓國建國大學Tae Heung Kang團隊和Yeong-Min Park團隊合作開發了一種可注射的、用于免疫調節的納米凝膠(iGel),它可以通過重塑腫瘤TME進而增強免疫治療的效果。
實驗證明,從iGel中釋放的免疫調節藥物可以消耗免疫抑制細胞,并且會誘導免疫原性細胞死亡以及增強免疫原性。實驗在利用iGel進行術后治療發現,它會誘導產生全身性抗腫瘤免疫和記憶T細胞的反應,進而明顯抑制腫瘤的復發和轉移。
Chanyoung Song, Tae Heung Kang, Yeong-Min Park, Yong Taik Lim. et al. Syringeable immunotherapeutic nanogel reshapes tumor microenvironment and prevents tumor metastasis and recurrence. Nature Communications. 2019
https://www.nature.com/articles/s41467-019-11730-8
8. ACS Nano:共摻雜納米閃爍體用于x射線激活的癌癥協同治療
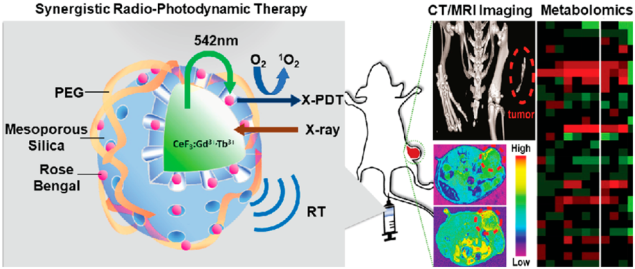
放療和光動力治療是目前治療癌癥的兩種重要策略。但它們各自也都有著很突出的弊端,如外源光的穿透性差和x射線對正常組織產生的副作用高等。因此,開發一種具有診斷功能的,可以協同實現放療和光動力治療的多功能納米平臺來對抗癌癥是目前研究的一大熱點。此外,通過將癌癥治療與代謝組學分析相結合,也有望改善早期的診斷和預后。
上海交通大學李萬萬研究員團隊通過共摻雜Tb3+和Gd3+的策略來增強CeF3納米顆粒(NPs)的閃爍體性能。實驗在共摻雜的CeF3:Gd3+,Tb3+閃爍體NPs表面包覆介孔二氧化硅,然后負載光敏劑RB構建了CGTS-RB并將其用于CT和磁共振成像(MRI)指導的、x射線激發的協同放射治療(RT+XPDT)。實驗也進一步利用代謝組學分析對協同治療的機制進行了研究,并且證明這種分析可以為改善腫瘤治療的預后提供幫助。
Farooq Ahmad, Wanwan Li. et al. Codoping Enhanced Radioluminescence of Nanoscintillators for X?ray-Activated Synergistic Cancer Therapy and Prognosis Using Metabolomics. ACS Nano. 2019
DOI: 10.1021/acsnano.9b04213
https://pubs.acs.org/doi/10.1021/acsnano.9b04213
9. Chem. Mater.:光敏劑-細菌混合材料用于增強光動力治療和細胞內的蛋白遞送
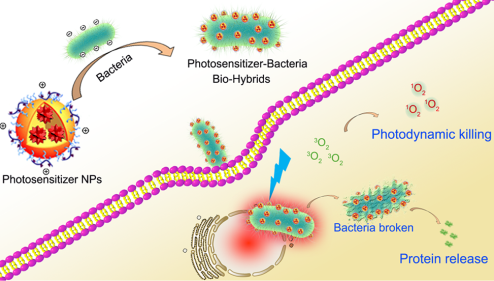
活菌具有良好的生物相容性和活性靶向性,可以將基因或蛋白質轉入真核細胞中從而治療癌癥,因此受到人們的廣泛關注。然而,如何有效地實現基因和蛋白的釋放仍然目前研究所面臨的一大問題。新加坡國立大學劉斌教授團隊利用具有AIE效應的光敏劑(PS)納米粒子TDNPP去修飾大腸桿菌(E. coli),構建了一種新型的生物混合型材料,并將其作為向癌細胞遞送光敏劑的載體。
實驗結果表明,大腸桿菌表面的TDNPP納米粒子可以促進其侵入癌細胞,并在光照射下產生活性氧(ROS)來有效地釋放蛋白。與沒有細菌作為載體的PS NPs相比,該多功能TDNPPs在體外具有更好的癌細胞成像和光介導的腫瘤殺傷性能。因此,這一的研究也為開發用于細菌介導的癌癥治療和細胞內蛋白遞送的平臺提供了新的思路。
Min Wu, Wenbo Wu, Bin Liu. et al. Photosensitizer-Bacteria Biohybrids Promote Photodynamic Cancer Cell Ablation and Intracellular Protein Delivery. Chemistry of Materials. 2019
DOI: 10.1021/acs.chemmater.9b01518
https://pubs.acs.org/doi/10.1021/acs.chemmater.9b01518
10. Angew:NIR II光激發的SPR效應可增強O2的產生以解決腫瘤放療耐受性
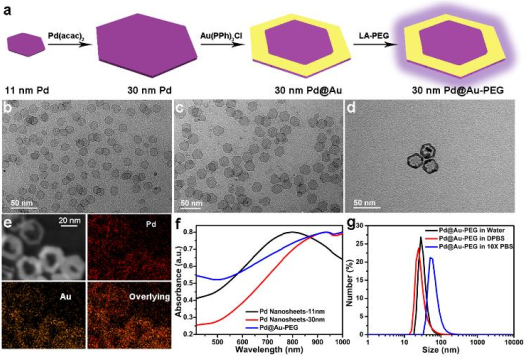
乏氧是實體腫瘤微環境的一種重要特征,而它對腫瘤的放療、光動力治療和化療的效果也會產生很明顯的負面影響。湖南大學張曉兵教授團隊提出了一種用于解決乏氧所誘導的腫瘤放療耐受的新策略。實驗制備了二維Pd@Au雙金屬核殼納米結構(TPAN),發現其在內源性H2O2的催化下可以長期穩定地產生O2以改善腫瘤的乏氧微環境,并且研究發現利用NIR II激光照射引起的表面等離子體共振(SPR)效應可以增強TPAN的催化活性,從而提高O2的生成效率。
概括來說,TPAN可以通過三個途徑來提高放療的效果:NIR II激光觸發的SPR效應可增強TPAN產生O2;Au和Pd這兩種高原子序數元素具有放療增敏的性能以及TPAN可以通過多模態成像來精確地指導癌癥治療,從而減少放療的副作用。
Yue Yang, Mei Chen, Xiao-Bing Zhang. et al. NIR-II Driven Plasmon-Enhanced Catalysis for Timely Supply of Oxygen to Overcome Hypoxia Induced Radiotherapy Tolerance. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201906758
https://onlinelibrary.wiley.com/doi/10.1002/anie.201906758
11. Adv. Sci.:光敏微載體用于修復組織缺損
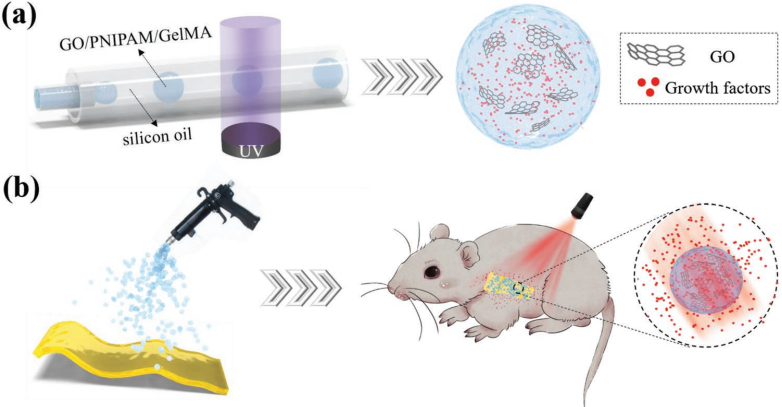
智能響應型微載體可以對外界刺激做出反應,從而主動地釋放藥物,因此可用于治療和組織再生等領域。而在各種刺激中,近紅外(NIR)光是一種很好的選擇,因為它可以穿透生物組織,具有足夠的強度也不會造成嚴重的損傷。東南大學趙遠錦教授、南京大學孫凌云教授和Qian Huang博士合作,利用微流體技術,制備了一種用于遞送藥物的光敏微載體(PDMs)。該微載體由可吸收NIR光的氧化石墨烯、對熱敏感的聚(N-異丙基丙烯酰胺)和明膠甲基丙烯酸酯組成。
在近紅外光照射下,PDMs的體積會發生收縮從而能有效地觸發藥物釋放;而當近紅外光消失后,縮小的微載體也會恢復到原來的大小,并且這個可逆的過程可以穩定地重復許多次。體外實驗表明,在激光照射下的PDMs能有效釋放負載的血管內皮生長因子,進而促進人臍靜脈內皮細胞的成管化。體內實驗結果也表明, PDMs在組織缺損大鼠模型上具有顯著的光熱效應和良好的治療效果。
Xin Zhao, Qian Huang, Lingyun Sun, Yuanjin Zhao. et al. Photoresponsive Delivery Microcarriers for Tissue Defects Repair. Advanced Science. 2019
DOI: 10.1002/advs.201901280
https://onlinelibrary.wiley.com/doi/10.1002/advs.201901280
12. Adv. Sci.:超薄黑云母納米片用于腫瘤診療
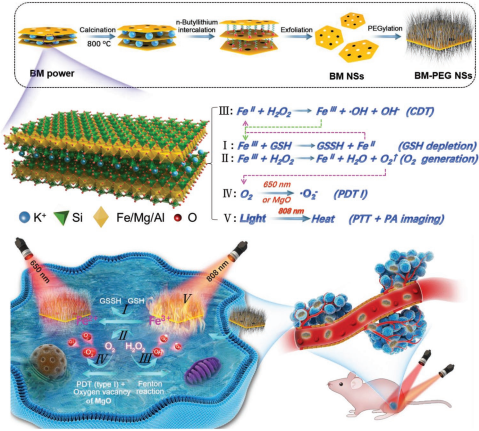
黑云母(BM)是一種片狀硅酸鹽礦物,在許多領域中都具有廣闊的應用前景。但是目前BM納米片(NSs)的合成卻還是一個不小的難題。深圳人民醫院Xiaobin Zeng博士、哈佛醫學院Omid C. Farokhzad教授和Wei Tao博士合作提出了一種高效合成超薄BM NSs的方法,并且由于這些NSs中存在MgO、Fe2O3和FeO,因此被聚乙二醇化后的BM NSs可以作為一種智能的腫瘤診療平臺,它具有以下特點:Fe3+可以通過消耗谷胱甘肽和生成O2來重塑腫瘤微環境(TME);生成的O2會被含有氧空位的MgO進一步催化生成·O2?;鐵離子催化的類芬頓反應可以通過TME中的H2O2生成·OH。
并且,BM NSs可以通過第二步和第三步的循環反應生成Fe2+和Fe3+,進而持續消耗谷胱甘肽和H2O2并生成·OH和O2。同時,在650 nm激光照射下,該NSs能夠利用O2產生·O2?,而在808 nm激光下則會產生光熱治療的效果,并且其自身也是一種可用于熒光、光聲和光熱成像的多模態成像造影劑。
Xiaoyuan Ji, Xiaobin Zeng, Omid C. Farokhzad, Wei Tao. et al. Synthesis of Ultrathin Biotite Nanosheets as an Intelligent Theranostic Platform for Combination Cancer Therapy. Advanced Science. 2019
DOI: 10.1002/advs.201901211
https://onlinelibrary.wiley.com/doi/10.1002/advs.201901211
13. Angew:對鋅特異性的iCEST MRI用于診斷前列腺癌
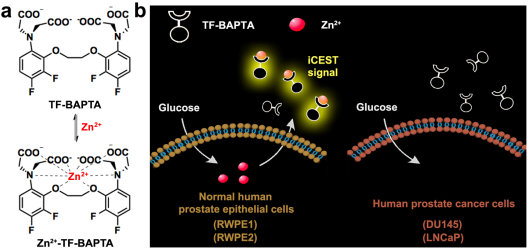
健康的前列腺是人體中含鋅量最高的軟組織。而在前列腺癌的早期發展過程中,含鋅量的水平會急劇下降,因此這可用于前列腺癌的診斷。約翰霍普金斯大學醫學院Jeff W. M. Bulte團隊將TF-BAPTA作為一種氟化的、可結合鋅的探針,證明了利用19F離子化學交換飽和轉移磁共振成像(iCEST MRI)可以區分正常和惡性前列腺細胞,并且具有微摩爾級別的敏感性。
在正常的前列腺細胞中,當ZIP1鋅轉運蛋白下調時,iCEST MRI信號也會發生明顯下降。在體內研究中,實驗使用原位前列腺癌小鼠模型和轉基因前列腺癌小鼠模型(TRAMP)證明了當正常前列腺上皮細胞轉變成癌細胞后, iCEST MRI的對比信號會逐漸下降超過300%。這一研究表明,通過利用iCEST MRI對前列腺內的鋅含量進行連續檢測,可以實現對前列腺癌進行有效的早期診斷。
Yue Yuan, Jeff W. M. Bulte. et al. Developing Zinc-Specific iCEST MRI as Imaging Biomarker for Prostate Cancer.
DOI: 10.1002/anie.201909429
https://onlinelibrary.wiley.com/doi/10.1002/anie.201909429
14. ACS Nano:納米黑色素用于光熱清除耐藥細菌感染并增強組織修復
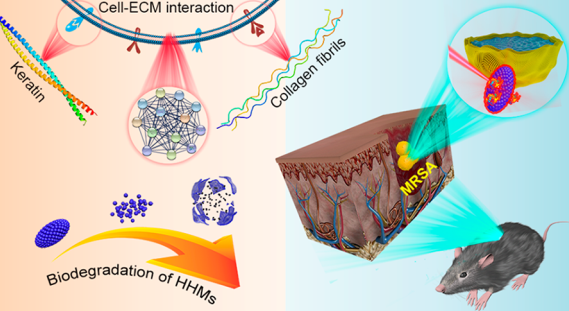
患者常常面臨著抗生素耐藥性細菌感染和術后長期組織重建的挑戰。湖北大學劉想梅博士和天津大學吳水林教授團隊合作利用人類頭發的黑色素衍生物(HHMs)開發了一種低溫的堿熱治療的策略。這種桑葚狀的HHMs的平均寬度為270 nm,平均長度為700 nm。帶負電荷的HHMs可以吸收帶正電荷的溶菌酶(Lyso),并通過靜電相互作用形成HHMs-Lyso復合材料。
這種可生物降解的納米結構可以通過光熱和溶菌素的輔助作用在體內有效治療耐甲氧西林金黃色葡萄球菌(MRSA)感染,并具有很高的抗菌效果(97.19 ± 2.39%)。此外,HHMs還可通過蛋白的消化和吸收這一信號實現對膠原alpha鏈蛋白的調控,進而有效地增強組織的修復。因此,這一研究工作也為在蛋白水平了解組織修復的機制提供了新的策略。
Jun Li, Xiangmei Liu, Shuilin Wu. et al. Lysozyme-Assisted Photothermal Eradication of Methicillin-Resistant Staphylococcus aureus Infection and Accelerated Tissue Repair with Natural Melanosome Nanostructures. ACS Nano. 2019
DOI: 10.1021/acsnano.9b03982
https://pubs.acs.org/doi/10.1021/acsnano.9b03982
15. Nano Lett.:對納米材料進行生物分子功能化進而控制其在活細胞中的性能
單鏈DNA和單壁碳納米管(SWCNTs)的非共價雜化可以增強其生物相容性、光穩定性、環境響應性和近紅外(NIR)熒光等性能,目前已在生物醫學成像和傳感領域得到了廣泛的應用。
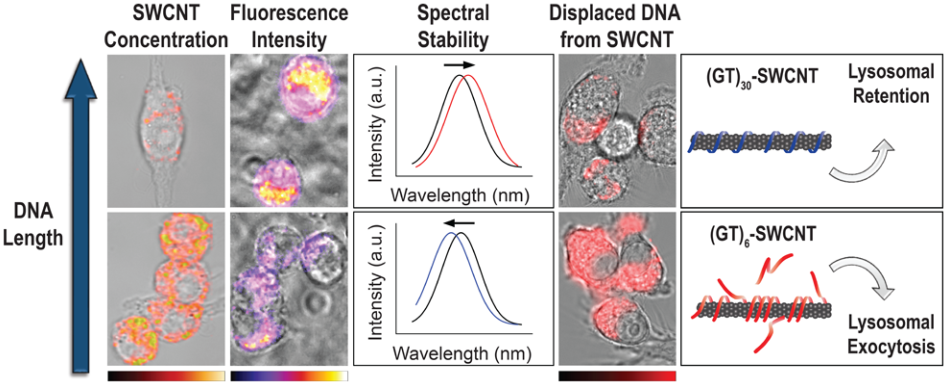
羅德島大學Daniel Roxbury團隊通過可見和近紅外熒光成像以及共聚焦拉曼顯微鏡等手段發現,通過調節寡核苷酸鏈的長度可以控制DNA-SWCNTs在哺乳動物細胞中的攝取、光學穩定性和保留效果等性能。此外,實驗通過藥物抑制研究也確定了SWCNT從細胞中排出的機制為溶酶體胞吐。這一研究為了解SWCNTs與活細胞之間的相互作用提供了有力的幫助,并且證明了通過改變包裹的DNA的類型就能有效控制納米材料的在生物體內的命運。
Mitchell Gravely, Daniel Roxbury. et al. Biomolecular Functionalization of a Nanomaterial To Control Stability and Retention within Live Cells. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b02267
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b02267
16. Angew:可同時監測酶活性和環境pH值的雙響應DNA探針
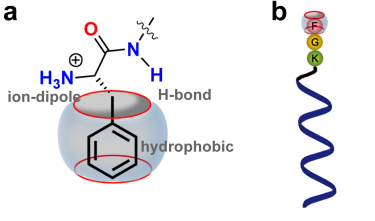
蛋白酶過表達和微環境的pH都是腫瘤的重要特征。然而,目前要實現對蛋白酶活性以及腫瘤微環境中pH值的精確同步檢測仍然具有很大挑戰性。中科院化學所吳海臣研究員團隊開發了一種雙響應型的DNA探針,它可以同時監測蛋白酶的活性和局部的pH值。
該DNA探針上帶有含苯丙氨酸(F)的短肽,而酶解作用會使之與葫蘆[7]脲形成復合物,進而在通過溶血素時產生電流信號,故可以用來量化蛋白酶的活性。此外,這一過程也和環境的pH相關,因此它也可以準確地反映局部的pH值。綜上所述,這一多功能DNA探針有望在未來用于對單個細胞等復雜系統的多個參數進行同時測量。
Lei Liu, Hai-Chen Wu. et al. A Dual Response DNA Probe for Simultaneously Monitoring Enzymatic Activity and Environmental pH by Nanopores. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201907816
https://onlinelibrary.wiley.com/doi/10.1002/anie.201907816
17. Small:聚乙二醇修飾的鉭納米顆粒用于腫瘤成像
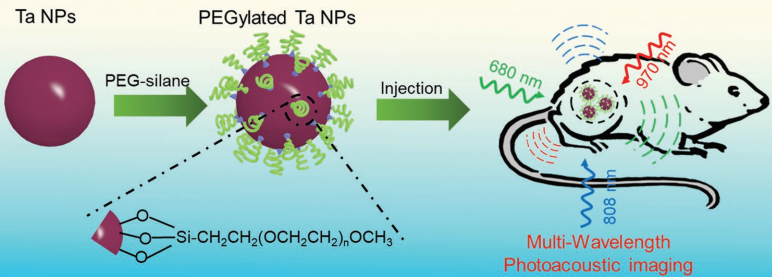
鉭基材料具有很高的生物相容性,是目前臨床上應用較為廣泛一種的醫用金屬材料。哈爾濱工業大學徐成彥教授團隊制備了一種聚乙二醇修飾的鉭納米粒子(Ta NPs),并將其作為腫瘤多波長成像的光聲(PA)造影劑。Ta NPs具有從可見光到近紅外的廣域光譜吸收能力和較高的光熱轉換效率(27.9%),因此可以實現多波長的、增強的PA成像,從而滿足臨床診斷的需要。
研究發現,在680 nm、808 nm和970 nm激光照射下,注射材料后腫瘤區域的PA強度較注射前分別提高了4.87、7.47和6.87倍。并且該Ta NPs也具有很低的毒性和消除不良活性氧的能力,因此是一種具有良好生物相容性的金屬PA造影劑。
Zhaohua Miao, Cheng-Yan Xu. et al. PEGylated Tantalum Nanoparticles: A Metallic Photoacoustic Contrast Agent for Multiwavelength Imaging of Tumors. Small. 2019
DOI: 10.1002/smll.201903596
https://onlinelibrary.wiley.com/doi/10.1002/smll.201903596
18. Nano Lett.:具有多尺度結構的納米纖維蛋白原支架用于促進傷口愈合
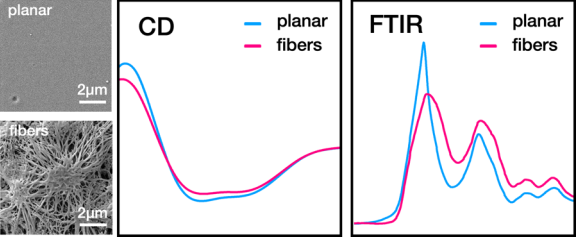
纖維蛋白原作為凝血和組織修復的關鍵成分,被廣泛地用于開發促進傷口愈合的納米纖維生物支架材料。目前制備蛋白質納米纖維的技術,如靜電紡絲或擠壓等都會引起蛋白質構象的變化。并且這種變化往往與淀粉樣變性相關,進而也會引發疾病。從我們最近引進的在生理鹽緩沖液中自組裝纖維蛋白原支架的技術開始,英國諾丁漢特倫特大學Monika Michaelis團隊和德國不萊梅大學Dorothea Bruggemann團隊合作,對新型纖維蛋白原納米纖維的形態和二級結構進行了研究,并考察了纖維蛋白原的濃度和pH值對蛋白構象的影響。
實驗觀察到,在形成纖維結構時,部分蛋白會由α-螺旋轉變為β-折疊。硫黃蛋白T染色實驗則表明,這種構象的轉變與淀粉樣蛋白的形成無關。由于該纖維支架材料的多尺度結構可以被很好地控制,因此不會產生致病的淀粉樣變性,從而證明了它是一種促進創傷愈合的良好材料。
Karsten Stapelfeldt, Monika Michaelis, Dorothea Bruggemann. et al. Controlling the Multiscale Structure of Nanofibrous Fibrinogen Scaffolds for Wound Healing. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b02798
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b02798
19. JACS:點擊反應輔助的靶向免疫細胞策略促進載藥納米粒子深入穿透腫瘤
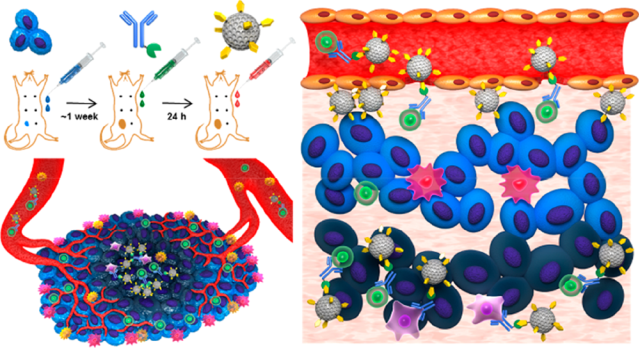
納米顆粒可以通過被動靶向的EPR效應或修飾的腫瘤特異性配體的主動靶向作用在腫瘤組織富集,進而遞送治療藥物。然而,由于納米粒子在腫瘤組織中的穿透深度有限,分布往往不均,這也影響了載藥納米粒子的腫瘤治療效果。韓國國民大學Nohyun Lee、韓國基礎科學研究所Taeghwan Hyeon團隊和Seung-Hae Kwon團隊合作開發了一種點擊反應輔助的靶向免疫細胞(CRAIT)策略,用于促進載藥納米顆粒更加深入地穿透腫瘤。
實驗將可靶向免疫細胞的CD11b抗體修飾反式環辛烯后,發現它能和被四嗪功能化的介孔二氧化硅納米顆粒(MSNs-Tz)發生生物正交的點擊化學反應。實驗將修飾后的抗體和MSNs-Tz間隔24小時注射入小鼠體內,證明了這一策略可使納米顆粒靶向結合到CD11b+髓樣細胞上,進而隨之一起進入腫瘤的內部,從而增強了載藥納米粒子治療原位4T1乳腺腫瘤模型的效果。并且該CRAIT策略不需要對細胞進行體外操作,因此可以用于各種類型的細胞和納米載體。
Soo Hong Lee, Nohyun Lee, Seung-Hae Kwon, Taeghwan Hyeon. et al. Deep Tumor Penetration of Drug-Loaded Nanoparticles by Click Reaction-Assisted Immune Cell Targeting Strategy. Journal of the American Chemical Society. 2019
DOI: 10.1021/jacs.9b04621
https://pubs.acs.org/doi/10.1021/jacs.9b04621
20. AFM綜述:用于癌癥免疫治療的智能注射水凝膠
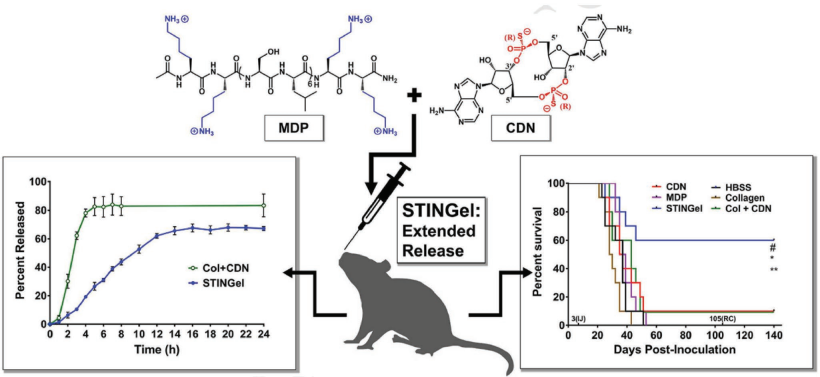
水凝膠是一種具有三維網絡結構的材料,在許多領域都有著廣泛的應用。而在生物醫學領域中,可注射的水凝膠一般用于對小分子或大分子治療藥物甚至細胞進行包封和控制釋放。隨著免疫治療的迅速發展,可注射的水凝膠因其能實現局部的免疫調節并促進全身抗癌免疫響應而受到人們的廣泛關注。
蘇州大學陳倩教授和劉莊教授合作,對目前用于癌癥免疫治療的可注射水凝膠的最新研究進展進行了綜述。雖然這種可注射水凝膠往往是在局部使用,但它能夠激活全身的抗腫瘤免疫反應,安全有效地抑制腫瘤轉移和復發;同時也討論了這類可注射水凝膠未來的發展方向及其臨床轉化的潛力。
Yu Chao, Qian Chen, Zhuang Liu. Smart Injectable Hydrogels for Cancer Immunotherapy. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201902785
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201902785
21. Nano Lett.:脂質體包封的量子點靶向腫瘤組織的研究
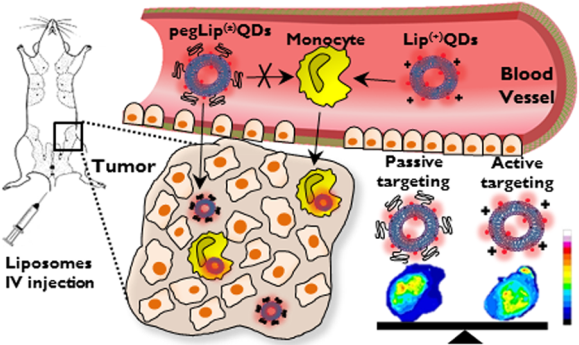
大多數的抗癌納米藥物都是利用EPR效應實現在腫瘤的富集。然而, EPR效應在不同的腫瘤類型和動物物種中表現往往差異很大,且在用于人類癌癥治療時的臨床效果不佳。耶路撒冷希伯來大學Gershon Golomb團隊對比研究了脂質體量子點(LipQDs)通過單核細胞的主動靶向和通過EPR效應的被動靶向的積累效果差異。
實驗將合成的親水性量子點包封在功能化的脂質體中,構建了用于被動和主動兩種模式靶向腫瘤的LipQDs,并對影響包封率和光學穩定性的各種理化參數進行了分析。研究發現,LipQDs通過被動和主動兩種模式靶向腫瘤的效率是相似的。這一結果表明,將量子點包封在納米脂質體中可以更好地保持其光學穩定性,并且顯著提高腫瘤對量子點的吸收效果。
Gil Aizik, Gershon Golomb. et al. Liposomes of Quantum Dots Configured for Passive and Active Delivery to Tumor Tissue. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b01027











