1. Nature Commun.:基于腫瘤外泌體的納米粒子用于遞送化療藥物
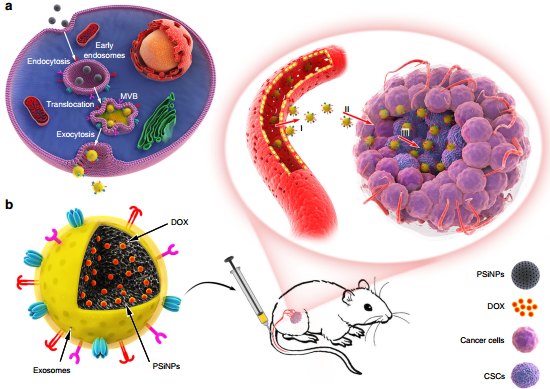
在不破壞蛋白質完整性的情況下開發仿生納米粒子仍然是癌癥化療的一大挑戰。華中科技大學甘璐教授、楊祥良教授和赫爾辛基大學Hélder A. Santos合作開發了一種具有良好生物相容性的、基于腫瘤細胞外泌體的仿生多孔硅納米顆粒(PSiNPs),并將其作為靶向腫瘤的化療藥物遞送載體。
這種外泌體包裹的負載有阿霉素的PSiNPs (DOX@E-PSiNPs)在被靜脈給藥后可有效在腫瘤富集并深入滲透腫瘤內部。并且該DOX@E-PSiNPs可以被癌細胞和癌癥干細胞(CSCs)有效地攝取并具有顯著地細胞毒性。體內實驗結果表明,DOX@E-PSiNPs可以在腫瘤處大量積累,因此在皮下、原位和轉移性腫瘤模型中表現出很高的抗癌活性。這一研究表明,基于腫瘤外泌體的仿生納米顆粒可以作為一種高效的腫瘤化療藥物遞送載體。
Tuying Yong, Lu Gan, Hélder A. Santos, Xiangliang Yang. et al. Tumor exosome-based nanoparticles are efficient drug carriers for chemotherapy. Nature Communications. 2019
https://www.nature.com/articles/s41467-019-11718-4
2. Angew:64Cu標記的二價前列腺特異性膜抗原抑制劑用于腫瘤診斷
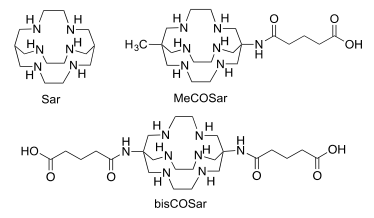
含有賴氨酸-脲基-谷氨酸官能團的分子可以與在前列腺癌中過表達的前列腺特異性膜抗原上的活性位點相結合。有鑒于此,墨爾本大學PaulS. Donnelly團隊、彼得·麥卡勒姆癌癥中心Carleen Cullinane團隊和Rodney J. Hicks團隊合作制備了一種64Cu標記的、將兩個靶向配體連接在單個銅絡合物上的二價試劑。這種二價試劑的腫瘤攝取和保留效果都會顯著地優于單配體試劑。實驗結果表明,在注射24小時后,該二價試劑仍具有很高的腫瘤攝取,低的成像背景和長時間的腫瘤保留效果,因此是一種很好的前列腺癌診斷試劑。
Nicholas Zia, Carleen Cullinane, Rodney J. Hicks, Paul S. Donnelly. et al. A Bivalent Inhibitor of Prostate Specific Membrane Antigen Radiolabeled with Copper-64 with High Tumour Uptake and Retention. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201908964
https://onlinelibrary.wiley.com/doi/10.1002/anie.201908964
3. AFM:鋁基MOF保護的抗原用于口服疫苗接種并誘導免疫反應
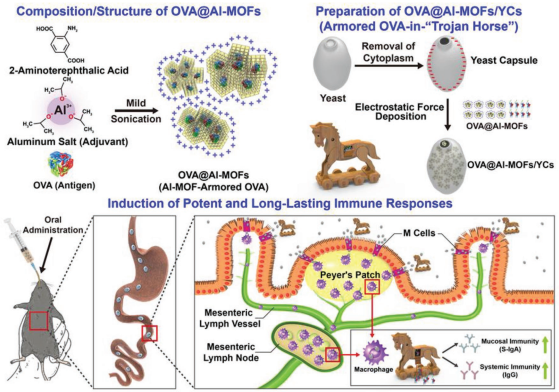
通過口服抗原的方式進行疫苗接種會面臨著胃腸道(GI) 的蛋白水解和粘膜屏障等問題。臺灣清華大學Hsing-Wen Sung團隊和慈濟大學Yen Chang團隊合作,在模型抗原卵白蛋白(OVA)上合成了一種生物礦化鋁基MOF(Al-MOF)材料,并將其作為一種遞送的載體和佐劑。而為了克服粘膜屏障,實驗利用酵母衍生的膠囊來和Al-MOF OVA組成一種類似于特洛伊木馬的系統。
體外實驗表明,Al-MOFs會在OVA上形成一層保護層,使其不被GI降解。并且這種礦化的Al-MOFs會在含有磷酸鹽離子的細胞內液中逐漸分解,進而慢慢釋放其包覆的OVA。體內研究表明,這種類似于特洛伊木馬的遞送平臺可以特異性地靶向腸道的M細胞,有利于OVA發生跨膜轉運和隨后被巨噬細胞內吞,最終積累在腸系膜淋巴結,進而產生持久有效的免疫反應。
Yang-Bao Miao, Yen Chang, Hsing-Wen Sung. et al. Engineering a Nanoscale Al-MOF-Armored Antigen Carried by a “Trojan Horse”-Like Platform for Oral Vaccination to Induce Potent and Long-Lasting Immunity. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201904828
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201904828
4. Adv. Sci.:利用細胞膜上的液晶液滴對單細胞釋放氨的過程進行實時成像
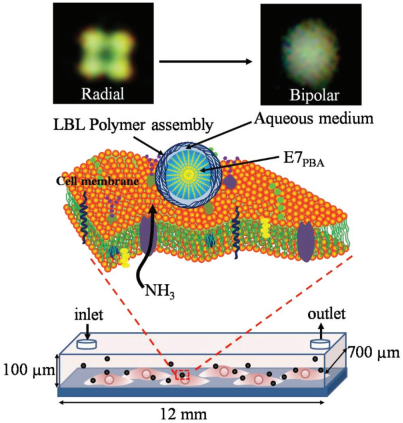
腫瘤細胞會發生顯著的代謝變化以適應微環境,因此這些細胞往往具有較高的谷氨酰胺分解速率,并會釋放出副產物氨(NH3)。這一過程既是癌細胞之間的擴散性信號,也可以用于揭示細胞的異質性。
清華大學林金明教授團隊將液晶(LC)E7與4-戊基-4 -聯苯羧酸(PBA)進行摻雜并包裹在聚合物微膠囊(P-E7PBA)中,然后在將其固定在細胞膜上,從而對正常人臍靜脈內皮細胞(HUVECs)和骨髓瘤、人原發性膠質母細胞瘤(U87)、人結腸癌(Caco-2)和人乳腺腺癌(MCF-7)細胞釋放NH3的情況進行了研究。實驗發現,P-E7PBA能夠在偏振光顯微鏡下通過由放射狀-雙極(R-B)的方向變化來觀察細胞釋放NH3的過程,并且不同的細胞系在R-B變化所需的響應時間上也有著顯著的差異。
Mashooq Khan, Jin-Ming Lin. et al. Real-Time Imaging of Ammonia Release from Single Live Cells via Liquid Crystal Droplets Immobilized on the Cell Membrane. Advanced Science. 2019
DOI: 10.1002/advs.201900778
https://onlinelibrary.wiley.com/doi/10.1002/advs.201900778
5. Small:超小氧化釓納米顆粒用于腫瘤的磁共振成像
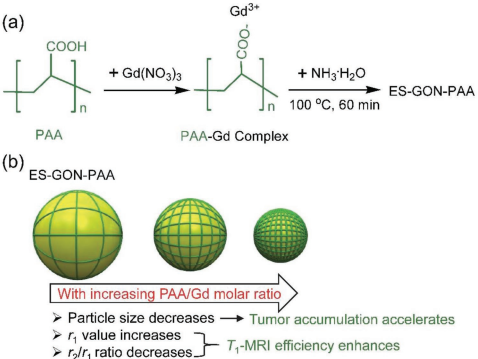
近幾十年來,Gd螯合物占據了磁共振成像(MRI)造影劑的大部分市場。然而,它也存在著很多諸如腎毒性、非特異性和低的r1弛豫率等問題。美國NIH范文培博士和陳小元教授、中科院寧波材料技術與工程研究所吳愛國研究員和廈門大學劉婷博士合作提出了一種制備聚(丙烯酸)(PAA)穩定的超小氧化釓納米顆粒 (ES-GON-PAA)的方法,它具有很好的水分散性,且尺寸小于2納米。
實驗表明,ES-GON-PAA是一種性能強大的T1加權磁共振成像造影劑,其 r1值比商業的Gd螯合物和已有研究報道的氧化釓納米顆粒(GONs)要高得多,而r2/r1則會低得多。實驗進一步將ES-GON-PAA與RGD2 (RGD二聚體)結合構建了 ES-GON-PAA@RGD2,并將其用于對過表達RGD受體的腫瘤進行T1加權的MRI,同樣證明了其具有非常顯著的腫瘤成像效果,性能也大大優于商業的Gd螯合物。
Zheyu Shen, Wenpei Fan, Ting Liu, Aiguo Wu, Xiaoyuan Chen. et al. Exceedingly Small Gadolinium Oxide Nanoparticles with Remarkable Relaxivities for Magnetic Resonance Imaging of Tumors. Small. 2019
DOI: 10.1002/smll.201903422
https://onlinelibrary.wiley.com/doi/10.1002/smll.201903422
6. ACS Nano:近紅外激發正交發射上轉換納米粒子用于成像指導的按需治療
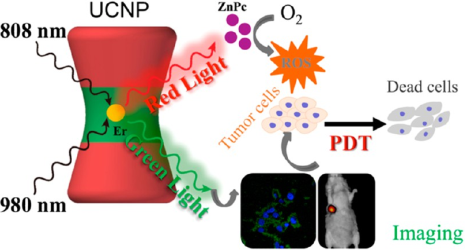
光動力療法(PDT)是一種重要的臨床腫瘤治療策略。但是,如何建立一個智能的診療平臺來對PDT治療過程中活性氧的生成進行時空控制仍然具有很大的挑戰性。上海大學朱曉輝博士、劉金亮博士和張勇教授合作制備一種了可被808和980 nm兩種不同的近紅外光(NIR)激發的,具有正交發射特性的上轉換納米粒子(UCNPs),其在980nm激發下會發射紅色光,在808nm激發下則發射綠色光。
與傳統的UCNPs不同,這一研究制備的具有核殼結構的UCNPs沒有復雜的多層摻雜,它的紅色和綠色上轉換發光都來自于核結構中的Er3+離子。研究也進一步證明這些UCNPs可用于用于成像指導的PDT治療,它發射的紅色光可以用于觸發PDT,而發射的綠色光可用于診斷和監測治療。這一工作表明,具有正交發射性能的UCNPs有望對近紅外光成像指導的治療實現精確時空控制。
Ming Tang, Xiaohui Zhu, Jinliang Liu, Yong Zhang. et al. Near-Infrared Excited Orthogonal Emissive Upconversion Nanoparticles for ImagingGuided On-Demand Therapy. ACS Nano. 2019
DOI: 10.1021/acsnano.9b04200
https://pubs.acs.org/doi/10.1021/acsnano.9b04200
7. ACS Nano:對pH敏感的Fe5C2@Fe3O4納米粒子用于腫瘤診療
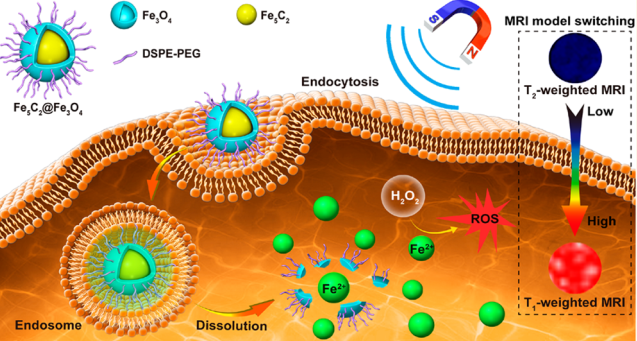
活性氧(ROS)是一種可以治療腫瘤的重要分子,然而其在臨床上的治療效果卻并不理想,主要原因是其產生的條件十分的苛刻。浙江工業大學車聲雷教授、浙江省人民醫院牟曉洲博士和北京大學侯仰龍教授合作報道了一種核殼結構的Fe5C2@Fe3O4納米顆粒,并將其作為產生ROS的納米反應器。
研究發現,Fe5C2@Fe3O4能夠在酸性微環境中釋放亞鐵離子,并和H2O2反應生成羥基自由基,從而有效抑制腫瘤細胞在體內外的增殖。并且,具有高磁化強度的Fe5C2@Fe3O4 NPs也可以實現磁靶向和T2加權的磁共振成像(MRI)。而它發生的電離過程會使得MRI 的T2信號降低,T1信號增強,這一T2/T1的轉換過程也為鐵離子釋放和ROS生成的可視化以及監測腫瘤治療的提供了支持。
Jing Yu, Xiaozhou Mou, Shenglei Che, Yanglong Hou. et al. Magnetic Reactive Oxygen Species Nanoreactor for Switchable Magnetic Resonance Imaging Guided Cancer Therapy Based on pH-Sensitive Fe5C2@Fe3O4 Nanoparticles. ACS Nano. 2019
DOI: 10.1021/acsnano.9b01740
https://pubs.acs.org/doi/10.1021/acsnano.9b01740
8. Chem. Sci.:DNA酶增強的DNA電路用于MicroRNA的檢測和細胞內成像
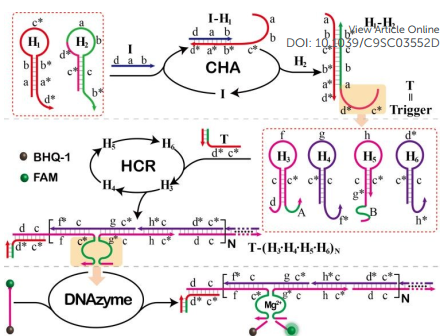
武漢大學王富安教授團隊設計了一種由DNA酶增強的DNA電路CHA-HCR-DNAzyme,并在體外對其性能進行了系統的研究。實驗結果表明,CHA-HCR-DNAzyme可以顯著地提高對miRNA的檢測性能,并且可以在活細胞中對其進行精確成像。這一結果源于CHA-HCR-DNAzyme具有的協同信號增強的機制,因此它在用于分析臨床研究中的痕量生物標志物時具有很好的應用價值。
Hong Wang, Fuan Wang. et al. DNAzyme-amplified DNA Circuit for Highly Accurate MicroRNA Detection and Intracellular Imaging. Chemical Science. 2019
DOI: 10.1039/C9SC03552D
https://pubs.rsc.org/en/content/articlelanding/2019/sc/c9sc03552d#!divAbstract
9. Small:響應pH的白蛋白/聚苯胺組裝物用于光聲成像和光熱治療
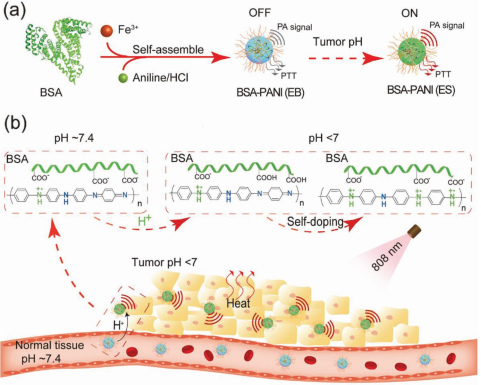
對腫瘤微環境響應的診療材料在實現腫瘤的精確診斷和有效治療方面具有巨大的應用價值。聚苯胺(PANI)是目前已知的第一種對pH響應的有機光熱試劑,而對腫瘤微環境的pH敏感的PANI型診療試劑目前還尚未被探索,這主要是因為PANI從EB態轉化為ES態時需要pH值小于 < 4,低于腫瘤微環境的pH值。
上海師范大學楊仕平教授和深圳大學黃鵬教授團隊合作,通過牛血清白蛋白的羧基(BSA)與PANI的亞胺基之間的分子酸堿反應,設計并制備了一種對腫瘤微環境pH響應的PANI診療試劑,并將其用于光聲成像指導的增強型光熱治療(PTT)。白蛋白/PANI組裝體(BSA-PANI)在pH < 7時就可以從EB態轉變為ES態,其吸收也會從可見光區紅移至近紅外區。體內外實驗結果表明,腫瘤酸性微環境能夠有效觸發BSA-PANI組裝體實現光聲成像(PAI)信號和PTT效應的增強。這一研究也為開發基于PANI的腫瘤診療一體化試劑提供了新的策略。
Qiwei Tian, Peng Huang, Shiping Yang. et al. Tumor pH-Responsive Albumin/Polyaniline Assemblies for Amplified Photoacoustic Imaging and Augmented Photothermal Therapy. Small. 2019
DOI: 10.1002/smll.201902926
https://onlinelibrary.wiley.com/doi/10.1002/smll.201902926
10. AFM:納米顆粒誘導和增強免疫原細胞死亡用于三陰性乳腺癌的免疫治療
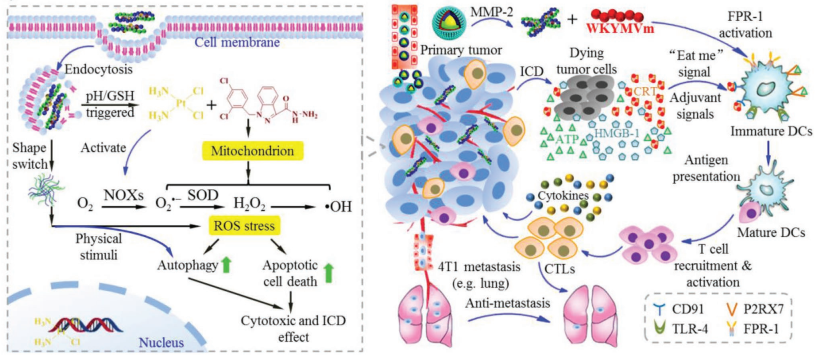
以順鉑為主的新輔助化療是治療三陰性乳腺癌(TNBC)的一種有效方法,但是這一方法的預后較差。華中科技大學張志平教授團隊制備了一種可誘導和增強免疫原性細胞死亡(ICD)的納米材料對順鉑、adjudin和WKYMVm進行協同遞送,進而用于針對TNBC的免疫治療。該納米粒子可對基質金屬蛋白酶-2、pH和谷胱甘肽等做出順序響應以實現結構的轉化,進而使其具有最優的尺寸大小、高的藥物遞送效率和可控制釋放的性能等優點。
實驗發現,順鉑和adjudin可以協同增強活性氧(ROS)的級聯反應,提高過氧化氫和高毒性羥基自由基的形成,并通過內質網應激、凋亡性細胞死亡和自噬機制等誘導ICD反應。而WKYMVm可通過激活甲酰肽受體1進而在樹突狀細胞和瀕死癌細胞之間建立穩定的相互作用,進一步增強抗TNBC的免疫響應。研究表明,該納米顆粒具有顯著的抑制原發性腫瘤和其肺轉移的作用,可增強機體的先天和適應性抗TNBC免疫響應。
Chenfeng Xu, Zhiping Zhang. et al. Transformable Nanoparticle-Enabled Synergistic Elicitation and Promotion of Immunogenic Cell Death for Triple Negative Breast Cancer Immunotherapy. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201905213
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201905213
11. ACS Nano:具有可控尺寸的酶驅動納米馬達用于生物醫學
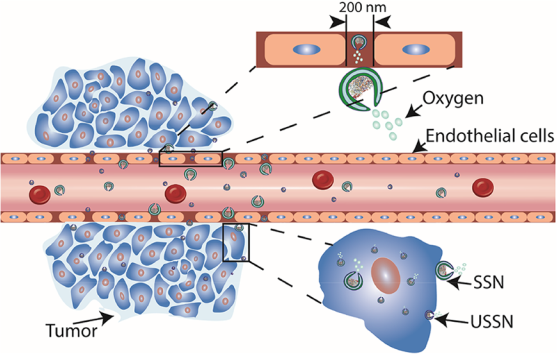
自驅動納米馬達在醫學領域有著廣闊的應用前景。然而,它們大多在尺寸上會有一個范圍,這也往往限制了它們在體內的進一步應用。已有研究表明,大小在20-200nm左右的納米粒子在克服細胞屏障和被細胞內化等方面具有很好的優勢。因此,減小這種口腔紅細胞狀的納米馬達的尺寸是非常重要的。拉德堡德大學Daniela A. Wilson團隊制備了尺寸約為150納米的超小口形紅細胞狀的聚合物泡囊,并將其作為一種用于生物醫學的載體。
實驗結果證明,通過引入PEG既可以使得該聚合物泡囊的形狀轉化為口型紅細胞狀,也可以對生物材料進行封裝。實驗將過氧化氫酶封裝在該納米馬達的內腔室中,既可以保護酶,同時也能提供足夠的推力來驅動馬達。該納米馬達可以只有2mM H2O2存在的情況下將H2O2轉化為O2來推動其發生運動,并且運動的速度與O2的產生有關。并且得益于更小的尺寸優勢,該納米馬達具有更強的穿透血管的能力,并且可以更好地被HeLa細胞吸收。
Jiawei Sun, Daniela A. Wilson. et al. Enzyme-Powered Nanomotors with
Controlled Size for Biomedical Applications. ACS Nano. 2019
DOI: 10.1021/acsnano.9b03358
https://pubs.acs.org/doi/10.1021/acsnano.9b03358
12. ACS Nano綜述:用于遞送miRNA修復心肌梗死的納米粒子-水凝膠系統
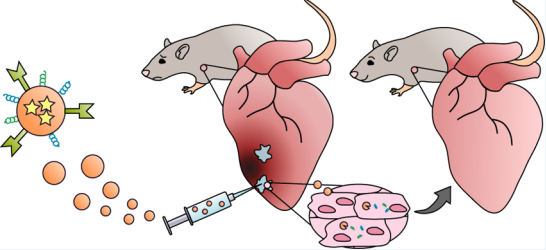
目前,針對于心肌梗死(MI)后的心臟修復和再生的有效治療方法還十分有限。雖然已有研究表明在心肌梗死發生后,miRNA (miRs)會在細胞水平上對改善心臟功能發揮重要作用,但如何實現miRs的靶向遞送和保留仍具有很大挑戰性。而為了解決這一難題,很多種的miRs載體被開發出來,但這些載體自身也還有很多的局限性,如免疫原性和對梗死部位的靶向性差等。
佐治亞理工學院和埃默里大學Michael E. Davis團隊總結了對心臟組織進行miRs給藥的不同機制,對目前已被開發的臨床使用的注射型水凝膠-納米顆粒遞送載體系統進行了綜述;并對這一領域未來的發展方向和尚待解決的問題做了詳細介紹。
Sruti Bheri, Michael E. Davis. Nanoparticle?Hydrogel System for Post
myocardial Infarction Delivery of MicroRNA. ACS Nano. 2019
DOI: 10.1021/acsnano.9b05716
https://pubs.acs.org/doi/10.1021/acsnano.9b05716
13. Nature Commun.:可穿過血腦屏障的納米材料用于誘導免疫反應治療膠質瘤
利用細胞毒性T淋巴細胞相關抗原4 (a-CTLA-4)和程序性細胞死亡-1 (a-PD-1)等檢查點抑制劑抗體去治療腦膠質瘤往往療效往往很差,這主要是由于它們不能跨越血腦屏障(BBB)。西達斯-西奈醫學中心Julia Y. Ljubimova團隊制備了一種在聚(β-L-蘋果酸) 支架上的納米免疫偶聯物材料(NICs),同時共價連接了a-CTLA-4和a-PD-1用于穿過BBB進行遞送并激活大腦局部的抗腫瘤免疫反應。
實驗發現,利用NICs治療小鼠GL261膠質母細胞瘤(GBM)后會導致腦腫瘤區CD8+ T細胞、NK細胞和巨噬細胞增多,而調節性T細胞(Tregs)則會減少。結果表明,利用NICs對GBM荷瘤小鼠進行聯合治療后,其效果也會明顯優于單一的檢查點抑制劑治療或游離的a-CTLA-4和a-PD-1治療。
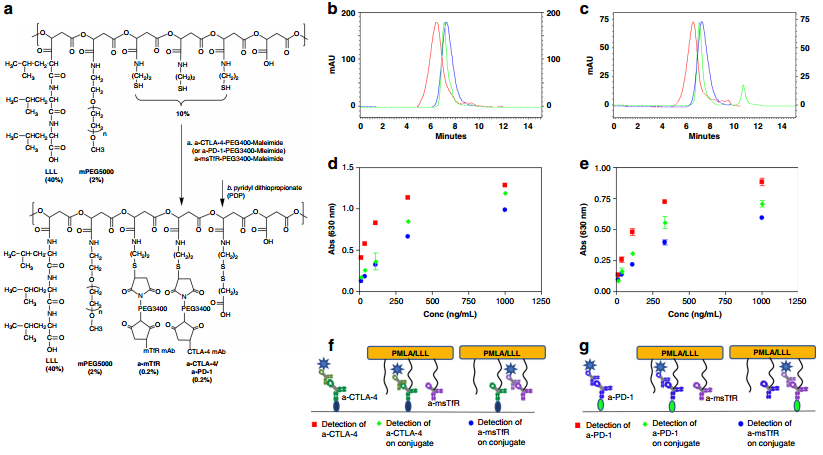
Anna Galstyan, Julia Y. Ljubimova. et al. Blood–brain barrier permeable nano immunoconjugates induce local immune responses for glioma therapy. Nature Communications. 2019
https://www.nature.com/articles/s41467-019-11719-3
14. AFM:超柔性可拉伸的石墨烯納米傳感器用于監測生物標志物
哥倫比亞大學林橋教授團隊制備了基于單分子層石墨烯的,適配體功能化的超柔性、可拉伸納米傳感器。其中,適配體可與目標生物標志物發生特異性結合,進而導致石墨烯載體的濃度發生變化,因此可以通過測量載體濃度來確定生物標志物的濃度。
實驗發現,在2.5微米厚的聚酯薄膜襯底上的納米傳感器能夠承受較大的彎曲、扭轉和拉伸變形,因此可以用于人體的組織或表面皮膚。研究進一步利用該傳感器對炎癥細胞因子生物標志物TNF-α進行檢測,發現其納米具有較高的選擇性和較低的檢測限(低至5 × 10?12 M)。因此,這一研究開發的納米傳感器有望對會發生較大機械形變的人類皮膚或組織的液體生物標志物進行有效可靠的檢測。
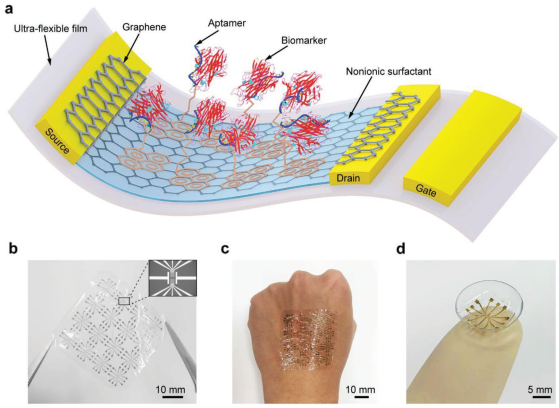
Ziran Wang, Qiao Lin. et al. An Ultra?exible and Stretchable Aptameric Graphene Nanosensor for Biomarker Detection and Monitoring. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201905202
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201905202
15. AFM:精確分子工程化的AIE光敏劑用于光動力治療
具有聚集誘導發光(AIE)特性的光敏劑(PSs)在聚集態可以高效地生成單態氧(1O2),因此它在光動力治療(PDT)領域引起了人們廣泛的研究興趣。而除了1O2生成效率高以外,其在長波長范圍內的強吸收和近紅外(NIR)發光的特性也是非常重要的,但是這對于AIE PSs來說卻很難實現,這是由于AIE分子的扭曲結構往往會導致其在短波長范圍內進行吸收和發光。
新加坡國立大學劉斌教授團隊通過精確的分子工程設計開發了一種新的AIE PSs,其在810 nm處會產生AIE效應,在300至700 nm范圍內具有很高的摩爾吸光系數,而在白光照射下則具有很好的1O2生成效率。這是由于該分子工程在TBT上引入了兩條柔性支鏈從而得到TBTC8,這就使得TBT在納米粒子(NPs)中不會產生強的分子間相互作用,因此TBTC8 NPs在1O2的生成、吸收和發光方面的性能都會更佳。體內外實驗結果也充分表明TBTC8 NPs具有良好的臨床應用前景。
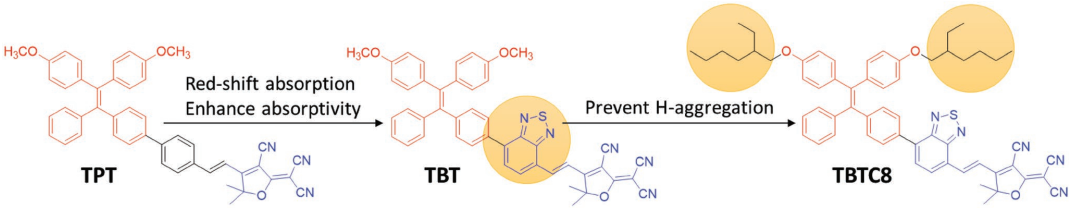
Wenbo Wu, Bin Liu. et al. Precise Molecular Engineering of Photosensitizers with Aggregation-Induced Emission over 800 nm for Photodynamic Therapy. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201901791
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201901791
16. AM:無靶向配體的受限納米顆粒可在體內將siRNA和sgRNA遞送給T細胞
T細胞可以幫助實現免疫調節,這也使得它們成為RNA治療中的重要靶點。雖然已有研究表明,負載RNA的納米顆粒可以通過基于蛋白質或適配體等靶向配體的作用來在體內靶向T細胞,但如何在無靶向配體的情況下實現向T細胞遞送RNA還具有很大挑戰性。由于T細胞可以內吞脂蛋白顆粒和包膜病毒這兩種結構類似于脂質納米粒子(LNPs)的自然材料,因此可以假設無靶向配體的LNPs也能夠將RNA遞送給T細胞。
利用這一假設,佐治亞理工學院James E. Dahlman團隊對168種納米顆粒在體內向9種細胞遞送siRNA的效果進行了定量分析。研究發現,含有受限脂類的納米材料可以形成穩定的cLNPs,而cLNPs可以將siRNA和sgRNA以低至0.5 mg kg-1的劑量遞送給T細胞。并且與之前報道的LNPs不同,cLNPs并不會優先靶向肝細胞,并且其遞送過程也是依賴于自身的化學成分,而與大小無關。
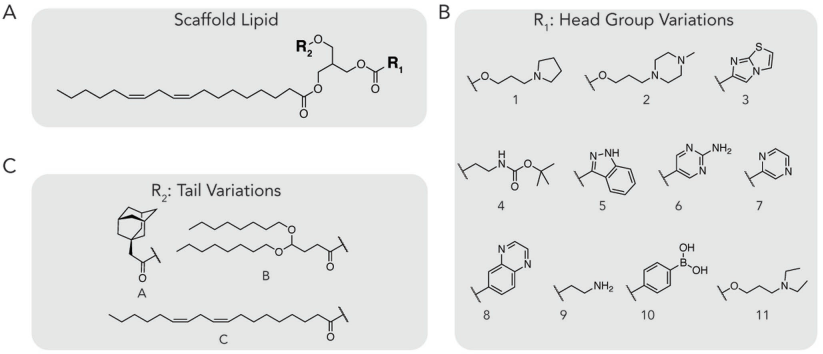
Melissa P. Lokugamage, James E. Dahlman. et al. Constrained Nanoparticles Deliver siRNA and sgRNA to T Cells In Vivo without Targeting Ligands. Advanced Materials. 2019
DOI: 10.1002/adma.201902251
https://onlinelibrary.wiley.com/doi/10.1002/adma.201902251
17. ACS Nano:熱敏原位成膠水凝膠用于治療耐藥細菌造成的感染創面
可原位成型的水凝膠是近年來發展起來的一種新型創面敷料。并且由于物理交聯的水凝膠往往是不穩定的,因此大多數原位形成的水凝膠都是通過化學交聯而成的。而交聯劑或聚合物基體的毒性則成為了一大隱患。
合肥工業大學陸楊教授和何濤教授合作報道了一種可噴涂的、原位成型水凝膠。這種熱響應水凝膠會在低溫下實現溶膠-凝膠的不可逆轉變,因此可以作為一種穩定的傷口敷料。這主要是由于其具有的無機/聚合物雙重網絡結構以及Ag@rGO納米片和PNIPAM之間的配位相互作用。實驗也在體內外證實了該材料對耐甲氧西林金黃色葡萄球菌(MRSA)具有很好的抗菌能力,可明顯促進MRSA造成感染傷口的愈合。
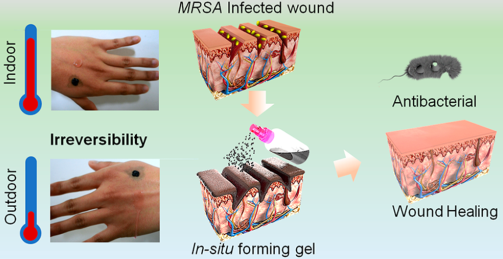
Xu Yan, Wei-Wei Fang, Yang Lu, Tao He. et al. Thermoresponsive in Situ Forming Hydrogel with Sol?Gel Irreversibility for Effective Methicillin-Resistant Staphylococcus aureus Infected Wound Healing. ACS Nano. 2019
DOI: 10.1021/acsnano.9b02845
https://pubs.acs.org/doi/10.1021/acsnano.9b02845
18. Adv. Sci.:Cu2-xS@MnS核殼納米粒子作為對光/雙氧水響應的腫瘤診療平臺
上海交通大學醫學院張志愿教授、孫樹洋教授和東華大學胡俊青教授合作,以Cu2-xS@MnS核殼納米粒子(CSNPs)為基礎,開發了一種新型的腫瘤診療平臺。其中Cu2-xS核可作為光敏劑產生光熱和活性氧(ROS),而MnS殼可用于對H2O2響應并生成O2。
實驗通過調控合成策略,得到了具有最佳光熱效應和增強的光動力(PD)效應的Cu2-xS@MnS CSNPs。體內實驗表明,Cu2-xS@MnS CSNPs可有效治療HeLa細胞來源的異種移植(CDX)和頭頸部鱗癌(HNSCC)患者來源的異種移植(PDX)模型腫瘤,同時也能作為一種T1增強的磁共振(MR)造影劑,是一種具有優異性能的響應雙刺激的診療試劑。
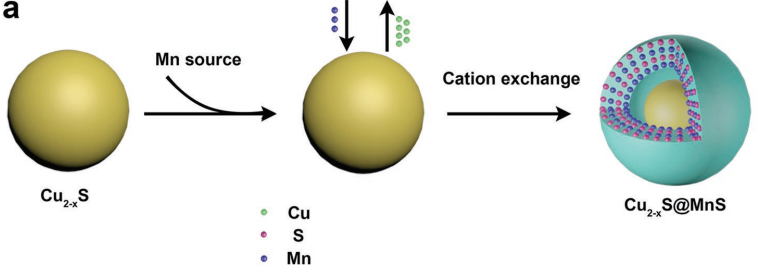
Xiaojuan Huang, Zhiyuan Zhang, Shuyang Sun, Junqing Hu. et al. Right Cu2?xS@MnS Core–Shell Nanoparticles as a Photo/H2O2-Responsive Platform for Effective Cancer Theranostics. Advanced Science. 2019
DOI: 10.1002/advs.201901461
https://onlinelibrary.wiley.com/doi/10.1002/advs.201901461
19. Angew:具有豐富缺陷位的納米酶作為增強的抑菌抗生素
納米酶具有內在的催化活性、廣譜抗菌的能力和很低的生物毒性,因此可以作為新一代的抗生素。然而,由于缺乏捕獲細菌的能力和催化活性不足,納米酶的抗菌效果還遠遠不能令人滿意。
中科院長春應化所王穎博士、任勁松研究員和曲曉剛研究員合作,首次通過一步法構建了具有粗糙表明和豐富缺陷位的納米酶,它結合細菌的能力和催化活性都有明顯增強。實驗也證明這種高效的納米酶可以在體內外更好地捕獲細菌捕,同時對耐藥性革蘭氏陰性大腸桿菌和金黃色葡萄球菌也有著顯著的抗菌效果。
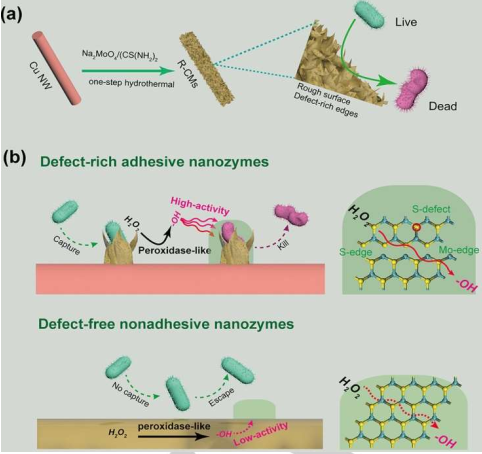
Fangfang Cao, Ying Wang, Jinsong Ren, Xiaogang Qu. et al. Defect-rich adhesive nanozymes as efficient “antibiotics” for enhanced bacterial inhibition. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201908289
https://onlinelibrary.wiley.com/doi/10.1002/anie.201908289
20. AFM:弗林蛋白酶控制Fe3O4納米顆粒的聚集和19F信號用于腫瘤的MRI
1H磁共振成像(MRI)的靈敏度很高,但是選擇性較差。而人體內源性的19F MRI信號很難被檢測,因此19F MRI就具有著很高的選擇性。中科大胡進明教授、胡兵教授、梁高林教授和中科院強磁場科學中心王俊峰研究員合作,利用點擊縮合反應制備了一種雙功能氟探針,并進一步利用該探針對Fe3O4納米顆粒(IONP)進行功能化,得到IONP@1。
實驗發現,弗林蛋白酶可以控制IONP的聚集,從而增強其T2 1H MRI信號,并激活其19F NMR/MRI信號的產生。實驗利用這一策略成功地將IONP@1用于對呋喃酶活性的檢測。此外,研究還將IONP@1應用于對斑馬魚腫瘤的精確雙模式(1H和19F) MRI,從而證明這一方法為解決常規MRI探針的選擇性和敏感性之間的矛盾提供了一種切實可行的手段,并有望在不久的將來用于對小鼠或大型嚙齒動物腫瘤進行1H和19 FMRI。
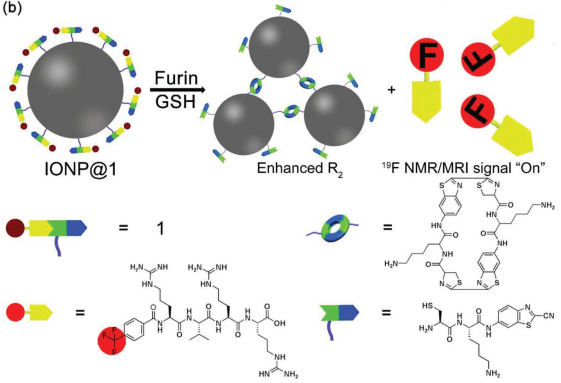
Zhanling Ding, Jinming Hu, Bing Hu, Junfeng Wang, Gaolin Liang. et al. Furin-Controlled Fe3O4 Nanoparticle Aggregation and 19F Signal “Turn-On” for Precise MR Imaging of Tumors. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201903860
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201903860
21. AFM:可被活性氧激活的脂質體復合材料用于光/化學動力學治療
腫瘤對光動力治療(PDT)和化學動力治療(CDT)會逐漸產生抗性。蘇州大學劉堅教授和中科院上海藥物研究所于海軍研究員合作報道了一種可被活性氧(ROS)激活的脂質體(RALP)。實驗設計的RALP@HOC@Fe3O4具有可被ROS裂解的連接分子,可以增強其在腫瘤的穿透和攝取效果和實現隨需釋放藥物,并可通過Fe3O4和奧沙利鉑前藥對腫瘤乏氧微環境進行調控。
其中,腫瘤細胞內的谷胱甘肽可被原藥消耗并生成具有毒性的奧沙利鉑。同時,消耗谷胱甘肽既可以避免PDT過程中ROS被過度湮滅,而且也可以調節腫瘤中的化學物種平衡以提高H2O2水平,有效緩解腫瘤的乏氧從而增強PDT。最后,RALP中的Fe (II)可以通過與H2O2發生類芬頓反應生成?OH以實現協同CDT。
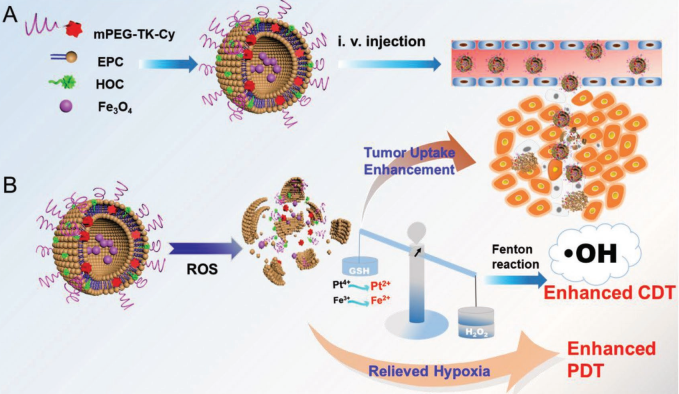
Zhihao Zhao, Jian Liu, Haijun Yu. et al. Reactive Oxygen Species–Activatable Liposomes Regulating Hypoxic Tumor Microenvironment for Synergistic Photo/Chemodynamic Therapies. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201905013











