1. AM:將輻射和細(xì)菌膜包覆的納米顆粒相結(jié)合用于開(kāi)發(fā)原位癌癥疫苗
通過(guò)隨機(jī)突變和特異性誘導(dǎo)所產(chǎn)生的新抗原是一種可被T細(xì)胞識(shí)別的腫瘤抗原。而在免疫冷性腫瘤中,腫瘤新抗原的識(shí)別能力有限,這也使得無(wú)法產(chǎn)生有效的抗腫瘤免疫反應(yīng)。而且這些冷性腫瘤對(duì)包括免疫檢查點(diǎn)抑制劑(ICIs)在內(nèi)的大多數(shù)免疫治療都響應(yīng)不佳。放射治療(RT)可以增強(qiáng)對(duì)冷腫瘤的免疫識(shí)別,從而產(chǎn)生更加多樣化的抗腫瘤T細(xì)胞反應(yīng),但單獨(dú)依靠RT還無(wú)法誘導(dǎo)產(chǎn)生全身的抗腫瘤免疫反應(yīng)。
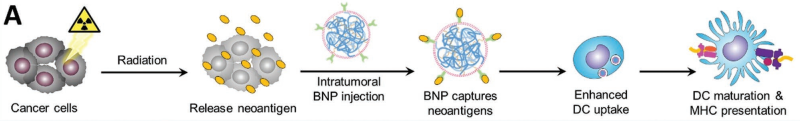
威斯康星大學(xué)宮紹琴教授和Zachary S. Morris博士合作制備了一種由免疫激活的PC7A/CpG內(nèi)核和包裹的細(xì)菌膜以及亞胺基團(tuán)組成的多功能納米顆粒(BNP)。這種BNP可在放療后捕獲腫瘤新抗原,增強(qiáng)其在樹(shù)突狀細(xì)胞(DC)中的攝取,從而刺激抗腫瘤T細(xì)胞反應(yīng)的發(fā)生。實(shí)驗(yàn)在患有同基因黑色素瘤和神經(jīng)母細(xì)胞瘤的小鼠模型上證明,BNP+RT聯(lián)合治療可通過(guò)激活樹(shù)突狀細(xì)胞和效應(yīng)T細(xì)胞顯著地抑制腫瘤生長(zhǎng),并產(chǎn)生腫瘤特異性的抗腫瘤免疫記憶。
Ravi B. Patel, Shaoqin Gong, Zachary S. Morris. et al. Development of an In Situ Cancer Vaccine via Combinational Radiation and Bacterial-Membrane-Coated Nanoparticles. Advanced Materials. 2019
DOI: 10.1002/adma.201902626
https://onlinelibrary.wiley.com/doi/10.1002/adma.201902626
2. AFM:異種靶向的納米雞尾酒藥物用于根除癌癥
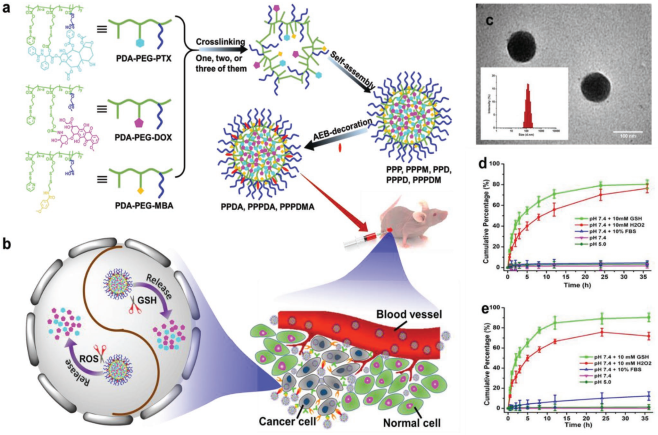
利用雞尾酒藥物去治療癌癥的臨床應(yīng)用因其嚴(yán)重的全身毒性而受到限制。南卡羅來(lái)納大學(xué)徐培盛教授團(tuán)隊(duì)制備了一種具有無(wú)跡連接物的異質(zhì)靶向納米雞尾酒藥物(PPPDMA)。得益于對(duì)谷胱甘肽和活性氧的響應(yīng)機(jī)制,在PPPDMA上負(fù)載的紫杉醇和阿霉素可以快速無(wú)痕跡地釋放到細(xì)胞質(zhì)中,這使得PPPDMA納米凝膠可以有效地殺死癌細(xì)胞并且沒(méi)有明顯的副作用產(chǎn)生。
實(shí)驗(yàn)結(jié)果表明,利用PPPDMA進(jìn)行治療可以顯著減少99%的腫瘤重量和96%的腫瘤數(shù)量,并且超過(guò)一半的治療組小鼠沒(méi)有出現(xiàn)復(fù)發(fā)腫瘤。這一工作表明,利用無(wú)痕連接劑和異種靶向策略的納米雞尾酒藥物是一種安全有效的腫瘤治療方法。
Binglin Sui, Peisheng Xu. et al. Heterotargeted Nanococktail with Traceless Linkers for Eradicating Cancer. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201906433
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201906433
3. Adv. Sci.:可恢復(fù)β淀粉樣蛋白體內(nèi)穩(wěn)態(tài)的納米材料用于預(yù)防老年癡呆
β淀粉樣蛋白(Aβ)的聚合被認(rèn)為是引起老年癡呆癥(AD)的主要原因。然而,目前用于靶向Aβ的疾病治療策略往往效果不佳,這是由于在AD的晚期階段會(huì)造成不可逆轉(zhuǎn)的損傷,因此要在Aβ的形成早期給與治療。
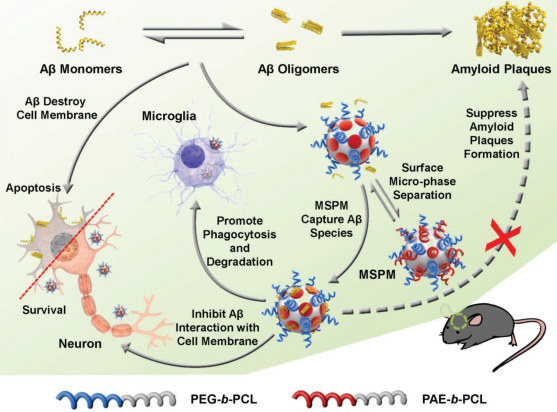
中國(guó)醫(yī)學(xué)科學(xué)院放射醫(yī)學(xué)研究所黃帆博士、南開(kāi)大學(xué)馮喜增教授和史林啟教授合作、以熱休克蛋白為靈感,設(shè)計(jì)了一種基于混合殼層聚合物膠束(MSPM)的自組裝納米材料,用于AD的預(yù)防治療。該納米材料具有疏水性的表面域,可以有選擇性地捕捉Aβ肽進(jìn)而有效地抑制Aβ聚合,從而顯著減少由Aβ介導(dǎo)產(chǎn)生的細(xì)胞毒性。并且該納米材料在吸附Aβ形成復(fù)合物后可以很容易地被小膠質(zhì)細(xì)胞吞噬,從而提高對(duì)Aβ的清除效果。因此,該納米材料可以顯著緩解由Aβ誘發(fā)的炎癥,對(duì)認(rèn)知缺陷的 APP / PS1轉(zhuǎn)基因老鼠也有很好的治療效果。
Huiru Yang, Fan Huang, Xizeng Feng, Linqi Shi. et al. Heat Shock Protein Inspired Nanochaperones Restore Amyloid-β Homeostasis for Preventative Therapy of Alzheimer’s Disease. Advanced Science. 2019
DOI: 10.1002/advs.201901844
https://onlinelibrary.wiley.com/doi/10.1002/advs.201901844
4. AM:AIEgen納米晶體的聚集誘導(dǎo)非線性光學(xué)效應(yīng)在體內(nèi)生物成像中的應(yīng)用
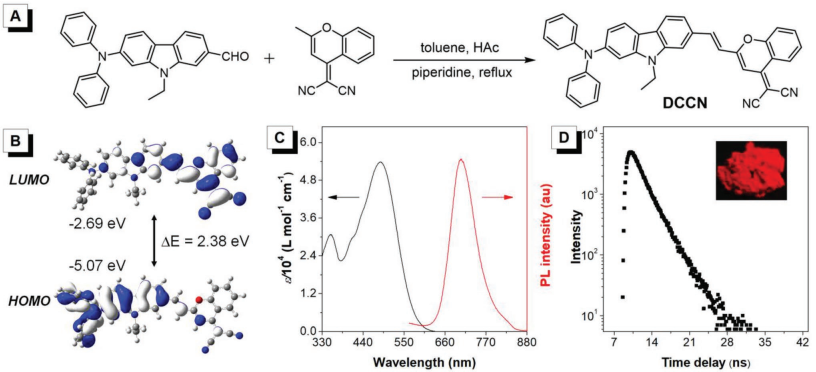
非線性光學(xué)顯微鏡因其具有獨(dú)特的光學(xué)切片、高空間成像分辨率和三維重建等功能,成為一種用于生物成像研究的有力工具。而開(kāi)發(fā)具有強(qiáng)非線性光學(xué)效應(yīng),可產(chǎn)生三次諧波的有機(jī)熒光探針,也已成為生物醫(yī)學(xué)領(lǐng)域的一個(gè)重要研究方向。浙江大學(xué)錢駿教授和香港科技大學(xué)唐本忠院士合作提出了一種基于AIE效應(yīng)的近紅外發(fā)光有機(jī)納米晶體(DCCN)的制備方法。
實(shí)驗(yàn)研究了DCCN的聚集誘導(dǎo)非線性光學(xué)效應(yīng),包括雙光子熒光(2PF)、三光子熒光(3PF)和THG等。實(shí)驗(yàn)將DCCN納米晶分別應(yīng)用于1040nm NIR-II激發(fā)下的2PF成像和1560nm NIR-II激發(fā)下的THG顯微鏡成像,成功地實(shí)現(xiàn)了對(duì)小鼠腦血管三維結(jié)構(gòu)的重建,并且THG顯微鏡成像比2PF顯微鏡具有更高的空間分辨率和亮度,可以在小鼠大腦最深的800微米處看到直徑2.7微米的小血管。
Zheng Zheng, Jun Qian, Ben Zhong Tang. et al. Aggregation-Induced Nonlinear Optical Effects of AIEgen Nanocrystals for Ultradeep In Vivo Bioimaging. Advanced Materials. 2019
DOI: 10.1002/adma.201904799
https://onlinelibrary.wiley.com/doi/10.1002/adma.201904799
5. AFM:多功能DNA聚索烴納米載體協(xié)同靶向治療耐多藥白血病
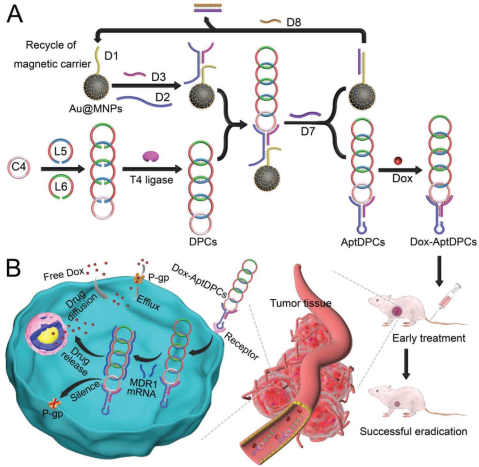
化療是目前治療癌癥的主要方式之一,但它也存在著藥物遞送效率低下、副作用嚴(yán)重以及耐多藥(MDR)等缺點(diǎn)。青島大學(xué)畢賽教授、南京大學(xué)姜立萍教授和朱俊杰教授合作報(bào)道了一種帶有適配體的多功能DNA聚索烴(AptDPCs)用于治療人類MDR白血病。
實(shí)驗(yàn)結(jié)果表明,AptDPCs可將藥物和反義寡核苷酸遞送給靶點(diǎn)藥物,進(jìn)而協(xié)同抑制MDR腫瘤的生長(zhǎng),且不會(huì)產(chǎn)生明顯的系統(tǒng)毒性。這一工作提出的基于AptDPCs的藥物遞送系統(tǒng)可以有效降低藥物的副作用,克服MDR,進(jìn)行為實(shí)現(xiàn)腫瘤治療中治療基因與化療藥物的協(xié)同但是提供了一個(gè)很有前景的新平臺(tái)。
Sha Yu, Li-Ping Jiang, Sai Bi, Jun-Jie Zhu. et al. Multifunctional DNA Polycatenane Nanocarriers for Synergistic Targeted Therapy of Multidrug-Resistant Human Leukemia. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201905659
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201905659
6. AFM:表面功能化納米顆粒通過(guò)碳水化合物相互作用靶向革蘭氏陰性細(xì)菌
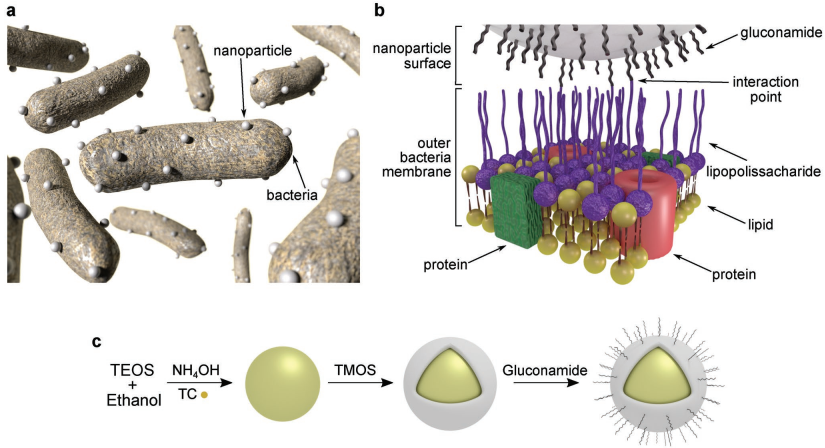
耐抗生素的病原體是現(xiàn)代人類健康所面臨的一大威脅。巴西納米技術(shù)國(guó)家實(shí)驗(yàn)室Mateus Borba Cardoso團(tuán)隊(duì)報(bào)道了一種可靶向革蘭氏陰性菌的碳水化合物包覆的二氧化硅納米顆粒。
該材料具有增強(qiáng)的結(jié)合細(xì)菌膜的能力,并且其在生物介質(zhì)中也具有高的穩(wěn)定性、不粘附非特異性蛋白,較低的細(xì)胞毒性和抗溶血活性等。實(shí)驗(yàn)也在生物分子水平上對(duì)該納米顆粒和細(xì)菌膜之間的局部相互作用進(jìn)行了研究,對(duì)其假設(shè)的機(jī)理做了充分的驗(yàn)證和說(shuō)明。
Larissa Brentano Capeletti, Mateus Borba Cardoso. et al. Gram-Negative Bacteria Targeting Mediated by Carbohydrate–Carbohydrate Interactions Induced by Surface-Modifed Nanoparticles. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201904216
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201904216
7. AM綜述:外泌體和納米技術(shù)用于精準(zhǔn)治療
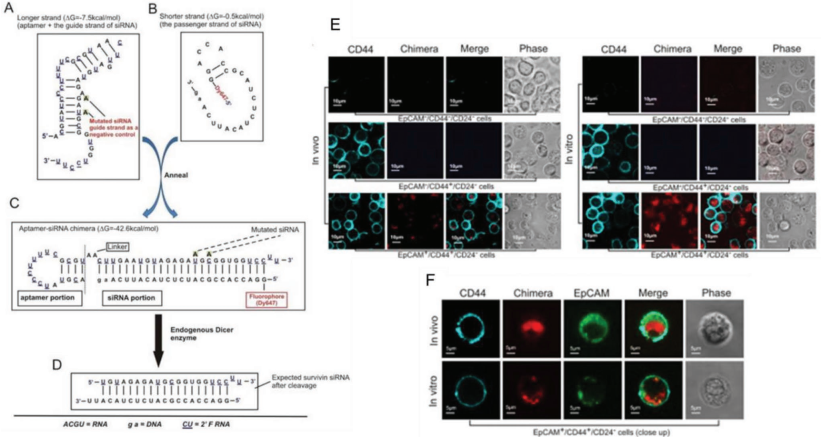
開(kāi)發(fā)基于外泌體的靶向納米藥物遞送系統(tǒng)是目前分子細(xì)胞生物學(xué)、藥物科學(xué)和納米工程等領(lǐng)域中的一個(gè)重要研究方向。外泌體是自然產(chǎn)生的尺寸為50 – 150 nm的囊泡,其在細(xì)胞間和細(xì)胞-組織間的通訊和跨物種通訊中發(fā)揮著重要的作用。同時(shí),外泌體也是一類很有前途的新型藥物遞送載體,因?yàn)樗鼈兡軌虮Wo(hù)有效載荷不受化學(xué)和酶降解的影響,并能夠逃避免疫系統(tǒng)的識(shí)別和隨后的清除。
中科院蘇州納米技術(shù)與納米仿生研究所朱毅敏研究員和迪肯大學(xué)段維教授合作,對(duì)根據(jù)適配體設(shè)計(jì)的、基于外泌體的靶向遞送系統(tǒng)的最新研究進(jìn)展進(jìn)行了綜述和總結(jié),并對(duì)這些系統(tǒng)的應(yīng)用前景和價(jià)值進(jìn)行了展望。
Phuong H. L. Tran, Yimin Zhu, Wei Duan. et al. Exosomes and Nanoengineering: A Match Made for Precision Therapeutics. Advanced Materials. 2019
DOI: 10.1002/adma.201904040
https://onlinelibrary.wiley.com/doi/10.1002/adma.201904040
8. ACS Nano:水凝膠納米貼片用于調(diào)節(jié)干細(xì)胞行為
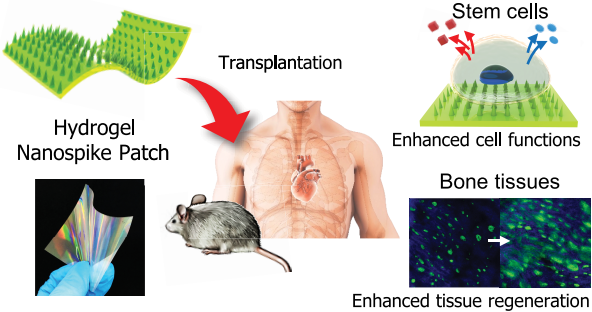
垂直排列的納米材料,如納米線和納米針等都可以作為一種有效的生物醫(yī)學(xué)平臺(tái)來(lái)對(duì)活細(xì)胞或組織進(jìn)行操作。然而,這些材料都有著剛性的力學(xué)性能和復(fù)雜的制造工藝流程,這使得它們很難與柔性的組織適應(yīng)性支架相集成,從而也限制了它們的進(jìn)一步應(yīng)用。
全南國(guó)立大學(xué)Jangho Kim和蔚山國(guó)家科學(xué)技術(shù)研究院Hoon Eui Jeong合作制備了一種具有釘狀水凝膠納米陣列結(jié)構(gòu)的高柔性貼片,并將其用于促進(jìn)干細(xì)胞的生長(zhǎng)和分化和抑制生物膜的形成。體外研究表明,該水凝膠納米貼片對(duì)干細(xì)胞膜具有強(qiáng)烈的物理刺激作用,可以在不改變細(xì)胞活力的前提下,增強(qiáng)干細(xì)胞的成骨、軟骨、脂肪分化和關(guān)鍵可溶性因子的分泌。同時(shí),該材料對(duì)革蘭氏陽(yáng)性菌和革蘭氏陰性菌也均表現(xiàn)出良好的抑菌性能。體內(nèi)研究進(jìn)一步證明,該柔性水凝膠貼片可以有效抑制小鼠的致病性細(xì)菌感染,同時(shí)也能顯著促進(jìn)受損顱骨骨組織的再生。
Sunho Park, Jangho Kim, Hoon Eui Jeong. et al. Hydrogel Nanospike Patch as a Flexible AntiPathogenic Scaffold for Regulating Stem Cell Behavior. ACS Nano. 2019
DOI: 10.1021/acsnano.9b04109
https://pubs.acs.org/doi/10.1021/acsnano.9b04109
9. Nano Lett.:DNA納米裝置用于增強(qiáng)細(xì)胞骨架活性和治療癌癥
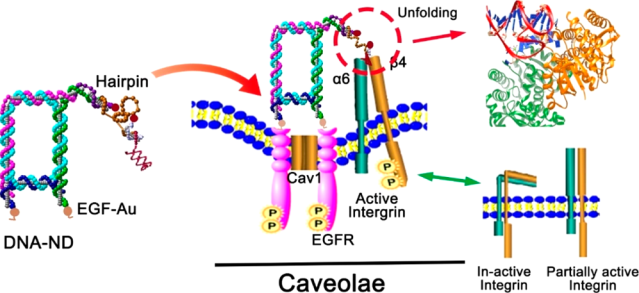
細(xì)胞表面受體(如EGFR和整合素)及其之間的相互作用在信號(hào)轉(zhuǎn)導(dǎo)和細(xì)胞骨架活化中起決定作用。南京大學(xué)夏興華教授團(tuán)隊(duì)設(shè)計(jì)了一種DNA納米器件(DNA- ND),它可以同時(shí)靶向細(xì)胞膜穴樣內(nèi)陷上的EGFR和整合素受體。當(dāng)裝置側(cè)臂上的DNA發(fā)夾結(jié)構(gòu)展開(kāi)時(shí),通過(guò)熒光和等離激元信號(hào)的變化可以檢測(cè)到EGFR-整合素受體共激活所產(chǎn)生的皮牛頓力。
實(shí)驗(yàn)發(fā)現(xiàn),EGFR-整合素受體的同時(shí)激活會(huì)導(dǎo)致細(xì)胞的信號(hào)轉(zhuǎn)導(dǎo)增強(qiáng)和發(fā)生收縮,同時(shí)生物化學(xué)通路也會(huì)啟動(dòng)并導(dǎo)致細(xì)胞分裂和內(nèi)吞及胞吐過(guò)程的改變,進(jìn)而影響細(xì)胞的增殖和凋亡。
Mirza Muhammad Faran Ashraf Baig, Xing-Hua Xia. et al. A DNA Nanodevice Simultaneously Activating the EGFR and Integrin for Enhancing Cytoskeletal Activity and Cancer Cell Treatment. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b03325
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b03325
10. Nat. Chem.:靶向光催化殺死腫瘤細(xì)胞
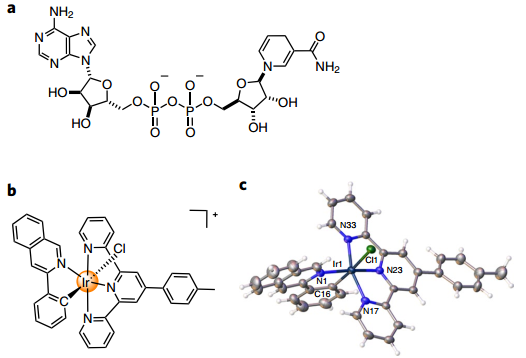
乏氧的腫瘤微環(huán)境是光動(dòng)力治療(PDT)所面臨的一個(gè)主要問(wèn)題。法國(guó)PSL大學(xué)Gilles Gasser教授、中山大學(xué)巢暉教授和英國(guó)華威大學(xué)Peter Sadler教授合作,證明了利用光催化進(jìn)行的氧化還原乏氧可以通過(guò)一個(gè)不依賴于氧的作用機(jī)制來(lái)解決這個(gè)問(wèn)題。實(shí)驗(yàn)設(shè)計(jì)了一種具有高氧化態(tài)的Ir(III)光催化劑,[Ir(ttpy)(pq)Cl]PF6,它對(duì)正常氧和乏氧癌細(xì)胞均有光毒性。研究發(fā)現(xiàn),該復(fù)合物可以通過(guò)光催化過(guò)程氧化1,4-二氫煙酰胺腺嘌呤二核苷酸(NADH)(活細(xì)胞中的重要輔酶)產(chǎn)生NAD*自由基,并且這一催化反應(yīng)在生物介質(zhì)中也具有很高的轉(zhuǎn)化頻率(TOF)。此外,該復(fù)合物和NADH也可以在乏氧條件下對(duì)細(xì)胞色素c進(jìn)行協(xié)同的光還原。
密度泛函理論計(jì)算結(jié)果表明,在復(fù)合物和NADH的加合物上發(fā)生的π堆積可以促進(jìn)光誘導(dǎo)的單電子轉(zhuǎn)移,而在癌細(xì)胞的線粒體中,復(fù)合物可通過(guò)和NADH發(fā)生的光催化過(guò)程來(lái)破壞電子轉(zhuǎn)移鏈。在光的照射下,該復(fù)合物會(huì)進(jìn)一步誘導(dǎo)NADH耗竭、細(xì)胞內(nèi)氧化還原失衡和癌細(xì)胞的免疫原性凋亡。這一研究所開(kāi)發(fā)的利用光催化誘導(dǎo)腫瘤細(xì)胞內(nèi)氧化還原狀態(tài)失衡的策略也為癌癥的光學(xué)治療提供了一種新的思路。
Huaiyi Huang?, Samya Banerjee?, Gilles Gasser, Hui Chao, Peter J. Sadler. et al. Targeted photoredox catalysis in cancer cells. Nature Chemistry. 2019
https://www.nature.com/articles/s41557-019-0328-4
11. AM綜述:磁性納米粒子在傳感領(lǐng)域的應(yīng)用研究進(jìn)展
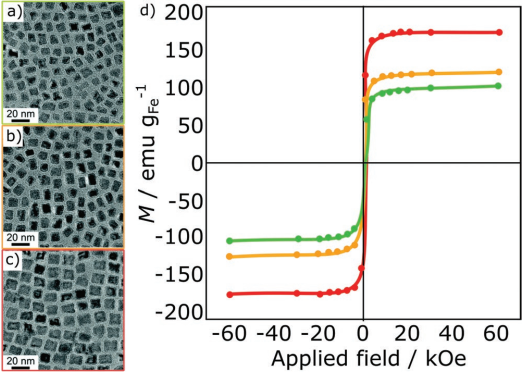
磁性納米粒子(MNPs)在傳感領(lǐng)域具有重要的應(yīng)用價(jià)值,它也為克服低檢測(cè)限和非特異性效應(yīng)等挑戰(zhàn)提供了切實(shí)可行的解決方案。
新南威爾士大學(xué)Richard D. Tilley教授和J. Justin Gooding教授合作,對(duì)用于傳感領(lǐng)域的MNPs的最新相關(guān)研究進(jìn)展進(jìn)行了綜述介紹;重點(diǎn)介紹了這些MNPs的結(jié)構(gòu)和性能以及如何將這些MNPs集成到設(shè)備中的策略;同時(shí)也對(duì)MNPs傳感器的合成進(jìn)展和面臨的主要挑戰(zhàn)進(jìn)行了介紹,并對(duì)這一領(lǐng)域未來(lái)的發(fā)展前景和方向做了說(shuō)明。
Lucy Gloag, Richard D. Tilley, J. Justin Gooding. et al. Advances in the Application of Magnetic Nanoparticles for Sensing. Advanced Materials. 2019
DOI: 10.1002/adma.201904385
https://onlinelibrary.wiley.com/doi/full/10.1002/adma.201904385
12. ACS Nano:設(shè)計(jì)功能分子以調(diào)整其細(xì)胞器靶向特異性和光動(dòng)力療效
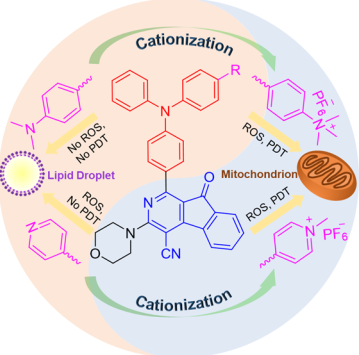
開(kāi)發(fā)高效的有機(jī)光敏劑(PSs)用于光動(dòng)力治療(PDT)是目前研究的一大熱點(diǎn)。然而,關(guān)于如何設(shè)計(jì)合成相關(guān)分子的報(bào)道卻很少。南方醫(yī)科大學(xué)鄭磊教授和香港科技大學(xué)唐本忠院士合作,以三苯胺-阿扎弗洛倫酮為核心,設(shè)計(jì)合成了一系列PSs并系統(tǒng)地研究了它們的結(jié)構(gòu)、性能和應(yīng)用關(guān)系。陽(yáng)離子化是一種通過(guò)實(shí)現(xiàn)靶向線粒體來(lái)提高PSs PDT效率的策略。
并且由于分子內(nèi)運(yùn)動(dòng)受限和系統(tǒng)間交叉得到增強(qiáng),具有聚集誘導(dǎo)發(fā)光(AIE)效應(yīng)的PSs的熒光和活性氧生成效率都有所提高。而可靶向線粒體的PSs比非線粒體靶向的脂滴也具有更高的PDT效率。并且實(shí)驗(yàn)結(jié)果表明,通過(guò)將PDT和放療相聯(lián)合還可進(jìn)一步增強(qiáng)AIE PSs殺傷癌細(xì)胞的能力。
Zhiyang Liu, Hang Zou, Lei Zheng, Ben Zhong Tang. et al. Tuning Organelle Specificity and Photodynamic Therapy Efficiency by Molecular Function Design. ACS Nano. 2019
DOI: 10.1021/acsnano.9b04430
https://pubs.acs.org/doi/10.1021/acsnano.9b04430
13. Nano Lett.:納米顆粒的尺寸會(huì)影響淋巴濾泡內(nèi)抗原的保留和表達(dá)
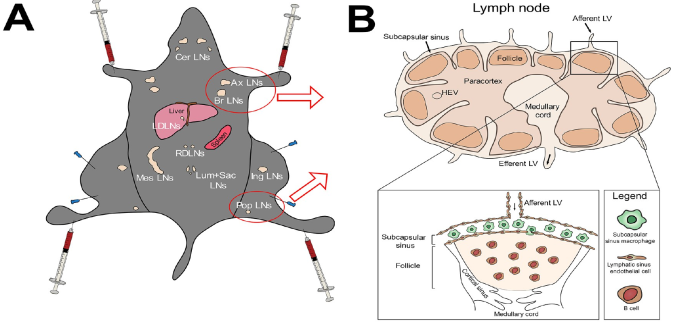
淋巴結(jié)濾泡會(huì)捕獲并保留抗原,從而誘導(dǎo)產(chǎn)生長(zhǎng)效的體液免疫。然而,淋巴結(jié)濾泡對(duì)抗原的保留效果是有限的。多倫多大學(xué)Warren C. W. Chan教授團(tuán)隊(duì)發(fā)現(xiàn),大小不同的納米顆粒載體會(huì)影響抗原在細(xì)胞內(nèi)節(jié)點(diǎn)的轉(zhuǎn)運(yùn)和特異性細(xì)胞間的相互作用。
實(shí)驗(yàn)發(fā)現(xiàn),濾泡的樹(shù)突狀細(xì)胞(FDC)網(wǎng)絡(luò)會(huì)在48小時(shí)內(nèi)清除尺寸較小的納米顆粒(5-15 nm),而較大的納米顆粒(50-100 nm)可以保留約5周。因此,相對(duì)于小尺寸納米顆粒來(lái)說(shuō),50-100 nm的納米顆粒在FDC樹(shù)突上的抗原遞送量比小尺寸的增加了175倍,而由生發(fā)中心B細(xì)胞形成的體液免疫反應(yīng)和產(chǎn)生的抗原特異性抗體則增強(qiáng)了5倍。這一研究結(jié)果表明,通過(guò)調(diào)控納米載體的尺寸大小可以調(diào)整體液免疫,從而產(chǎn)生高效的疫苗作用。
Yi-Nan Zhang, Warren C. W. Chan. et al. Nanoparticle Size Influences Antigen Retention and Presentation in Lymph Node Follicles for Humoral Immunity. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b02834
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b02834
14. Angew:DNA酶熒光傳感器用于成像活細(xì)胞中的金屬離子
利用生物正交反應(yīng)對(duì)金屬離子傳感器進(jìn)行控制進(jìn)行對(duì)活細(xì)胞中的金屬離子進(jìn)行成像,可以更好地了解金屬離子的分布和波動(dòng)情況。雖然已有研究報(bào)道可以利用光等外部刺激進(jìn)行生物正交控制,但這些刺激往往不適用于研究一些光穿透深度有限或活化量子產(chǎn)率較低的生物系統(tǒng)。
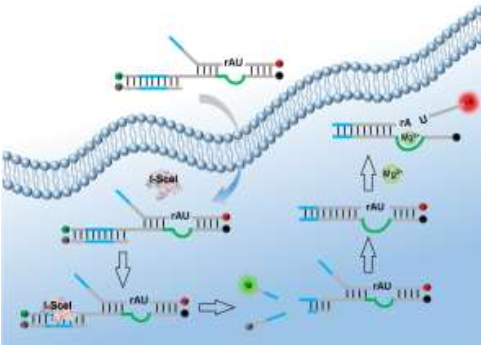
伊利諾伊大學(xué)香檳分校陸藝教授和四川大學(xué)鄭成斌教授合作,設(shè)計(jì)了一種可被內(nèi)源性生物正交激活的DNA酶熒光傳感器。其中,通過(guò)雙鏈DNA雜交而形成的識(shí)別位點(diǎn)會(huì)在一開(kāi)始阻止活性DNA酶的形成。而一旦核酸內(nèi)切酶I-SceI在細(xì)胞內(nèi)表達(dá),它就會(huì)在識(shí)別位點(diǎn)進(jìn)行剪切,使得DNA酶轉(zhuǎn)變?yōu)榛钚詷?gòu)象。而激活的DNA酶?jìng)鞲衅髂軌蛟贛g2+存在的條件下特異性催化底物鏈的裂解,釋放熒光標(biāo)記的DNA片段,產(chǎn)生Mg2+熒光信號(hào)。實(shí)驗(yàn)表明,利用這一策略可以對(duì)HeLa細(xì)胞中的Mg2+進(jìn)行成像。
Yao Lin, Chengbin Zheng, Yi Lu. et al. Enzyme-Mediated Endogenous and Bioorthogonal Control of a DNAzyme Fluorescent Sensor for Imaging Metal Ions in Living Cells. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201910343
https://onlinelibrary.wiley.com/doi/10.1002/anie.201910343
15. Small:基于聚(乙二醇)-b-聚(L-甲狀腺素)的納米制劑用于腫瘤診療
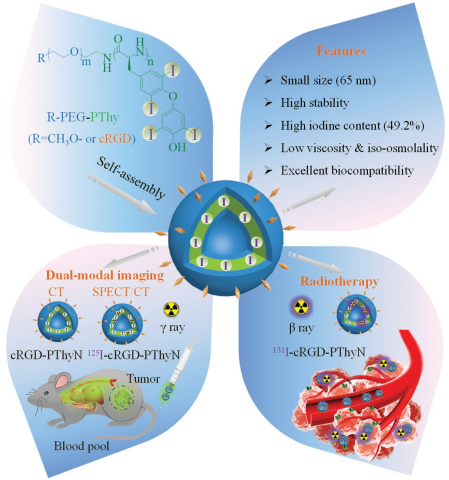
蘇州大學(xué)鐘志遠(yuǎn)教授和鄧超教授合作制備了一種基于聚(乙二醇)-b-聚(L-甲狀腺素) (PEG-PThy)嵌段共聚物肽的多功能、穩(wěn)定的納米制劑PThyN,并將其用于SPECT/CT雙模成像和靶向的腫瘤放療。與臨床使用的碘己醇、碘黃醇等造影劑相比,PThyN具有等滲性、低粘度和循環(huán)時(shí)間長(zhǎng)等特點(diǎn)。雖然PThyN在體外CT的衰減效果與碘己醇相當(dāng),但它可以極大地增強(qiáng)血管系統(tǒng)和軟組織的體內(nèi)CT成像效果。
實(shí)驗(yàn)通過(guò)使用cRGD肽對(duì)PThyN進(jìn)行表面修飾,可以實(shí)現(xiàn)對(duì)皮下B16F10黑色素瘤和原位A549肺腫瘤的增強(qiáng)CT成像。而通過(guò)碘交換反應(yīng)得到的125I標(biāo)記的PThyN則可以對(duì)腫瘤進(jìn)行SPECT/CT成像,并監(jiān)測(cè)PThyN在體內(nèi)的生物分布情況。而131I標(biāo)記的、cRGD功能化的PThyN對(duì)小鼠B16F10腫瘤也具有顯著的生長(zhǎng)抑制作用。
Xiaolei Gu, Zhiyuan Zhong, Chao Deng. et al. Nanoagents Based on Poly(ethylene glycol)-b-Poly(l-thyroxine) Block Copolypeptide for Enhanced Dual-Modality Imaging and Targeted Tumor Radiotherapy. Small. 2019
DOI: 10.1002/smll.201902577
https://onlinelibrary.wiley.com/doi/10.1002/smll.201902577
16. Nano Lett.:卵黃殼結(jié)構(gòu)的金納米星-MOF材料用于協(xié)同化學(xué)-光熱治療
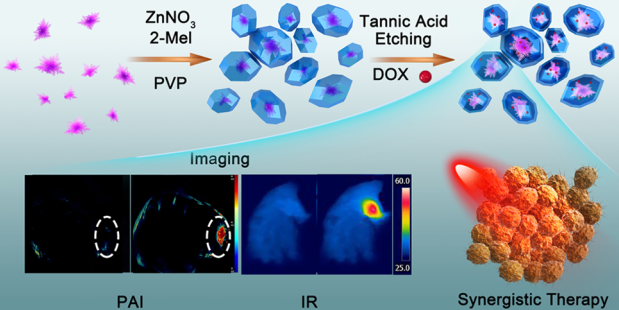
對(duì)光敏感的卵黃殼結(jié)構(gòu)納米粒(YSNs)是一種可被遠(yuǎn)程控制、對(duì)刺激敏感的診療平臺(tái),它也為實(shí)現(xiàn)腫瘤的協(xié)同治療提供了一種高效的策略。中科院長(zhǎng)春應(yīng)化所程子泳博士和林君研究員合作,以金納米星(Au star)為NIR II區(qū)的光熱“蛋黃”,以可生物降解的ZIF-8為殼層,成功構(gòu)建了一種新型的、刺激響應(yīng)型多功能YSNs。實(shí)驗(yàn)將化療藥物鹽酸阿霉素(DOX)包封入腔內(nèi),其在微酸性腫瘤微環(huán)境中會(huì)因ZIF-8降解過(guò)程而表現(xiàn)出藥物的可控釋放行為。
在1064 nm激光照射下,金納米星@ZIF -8 (Au@MOF)納米顆粒由于具有光熱和釋放藥物的特性,因此它表現(xiàn)出顯著的協(xié)同抗癌作用。此外,在近紅外區(qū)有強(qiáng)吸收的Au@MOF也具有近紅外熱成像和光聲(PA)成像的性能。
Xiaoran Deng, Ziyong Cheng, Jun Lin. et al. Yolk?Shell Structured Au Nanostar@Metal?Organic Framework for Synergistic Chemo-photothermal Therapy in the Second Near-Infrared Window. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b01716
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b01716
17. AM:納米技術(shù)用于多模態(tài)成像指導(dǎo)的精準(zhǔn)外科手術(shù)治療
手術(shù)切除是目前大多數(shù)實(shí)體瘤患者最主要和最有效的治療方法。然而,患者在手術(shù)后往往還會(huì)出現(xiàn)復(fù)發(fā)和轉(zhuǎn)移。近年來(lái),隨著微創(chuàng)外科技術(shù)的飛速發(fā)展,新興的納米技術(shù)也被逐漸用于微創(chuàng)、精準(zhǔn)、智能化腫瘤外科手術(shù)應(yīng)用。
美國(guó)NIH陳小元教授、中南大學(xué)文宇教授和熊力教授合作綜述了納米技術(shù)在成像指導(dǎo)的手術(shù)治療(IGS)和手術(shù)輔助的協(xié)同治療中的應(yīng)用,充分揭示了納米技術(shù)在多模態(tài)IGS輔助的精準(zhǔn)腫瘤協(xié)同治療中應(yīng)用優(yōu)勢(shì);簡(jiǎn)要介紹了NMs對(duì)手術(shù)靶點(diǎn)的作用機(jī)理,這種基于分子成像技術(shù)的多模態(tài)成像為實(shí)現(xiàn)高分辨率、深組織穿透的可視化手術(shù)提供了一種實(shí)用的方法,并且多功能NMs也可將手術(shù)與輔助治療(如化療、免疫治療、光療)相結(jié)合,充分消除殘余病灶;最后對(duì)開(kāi)發(fā)與外科應(yīng)用相關(guān)的診療NMs所面臨的關(guān)鍵問(wèn)題和臨床轉(zhuǎn)化前景進(jìn)行了詳細(xì)討論。
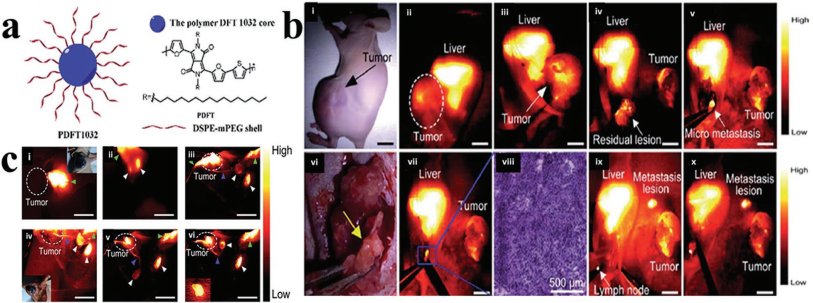
Cong Wang, Yu Wen, Li Xiong, Xiaoyuan Chen. et al. Advanced Nanotechnology Leading the Way to Multimodal Imaging-Guided Precision Surgical Therapy. Advanced Materials. 2019
DOI: 10.1002/adma.201904329
https://onlinelibrary.wiley.com/doi/full/10.1002/adma.201904329
18. AFM:類病毒pH響應(yīng)型聚合物納米顆粒用于在胞內(nèi)遞送抗腫瘤藥物
實(shí)現(xiàn)被細(xì)胞內(nèi)化和內(nèi)體逃逸仍然是許多抗腫瘤治療藥物,特別是大分子藥物所面臨的主要挑戰(zhàn)。已有研究表明,病毒藥物載體可有效地在細(xì)胞內(nèi)進(jìn)行遞送,但其可負(fù)載的載荷種類卻很有限。赫爾辛基大學(xué)Shiqi Wang博士、Hélder A. Santos教授和Wei Li博士合作開(kāi)發(fā)了一種類病毒的新型聚合物納米顆粒(ADMAP)。該聚合物具有可以實(shí)現(xiàn)核內(nèi)體逃逸的衣殼蛋白,而乙酰化右旋糖酐則作為類病毒的核心用于負(fù)載貨物。
實(shí)驗(yàn)結(jié)果表明,在核內(nèi)體的pH條件下(5.0),ADMAP顆粒可以成功地破壞核內(nèi)體膜的穩(wěn)定性,并協(xié)同釋放藥物載荷,其與游離的抗癌藥物相比具有更高的治療效果。而在進(jìn)一步結(jié)合腫瘤穿透肽后也可以增強(qiáng)其在三維腫瘤球體中的抗腫瘤作用。
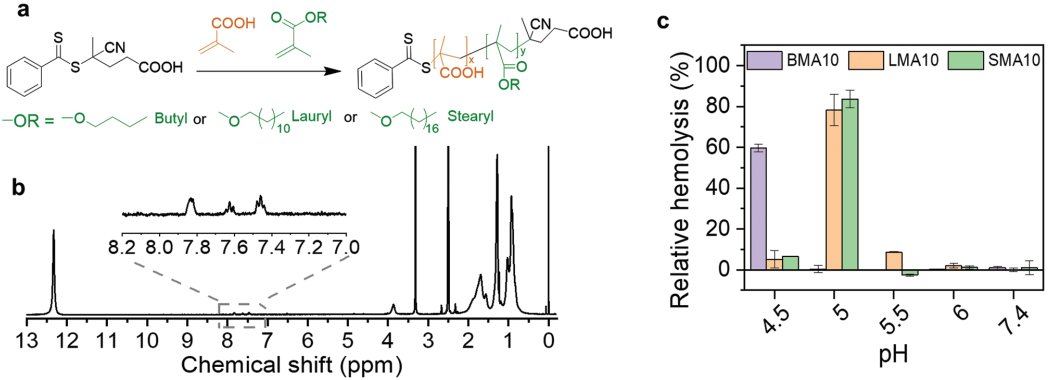
Saowanee Wannasarit, Shiqi Wang, Hélder A. Santos, Wei Li. et al. A Virus-Mimicking pH-Responsive Acetalated Dextran-Based Membrane-Active Polymeric Nanoparticle for Intracellular Delivery of Antitumor Therapeutics. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201905352
https://onlinelibrary.wiley.com/doi/10.1002/adfm.201905352
19. Angew:對(duì)近紅外光響應(yīng)的H2S活化納米診療平臺(tái)
開(kāi)發(fā)對(duì)近紅外光響應(yīng)的納米平臺(tái)為實(shí)現(xiàn)精確的癌癥藥物隨需釋放提供了新的方法。華東理工大學(xué)趙春常教授、中科院上海應(yīng)用物理研究所諸穎博士和上海交通大學(xué)樊春海教授合作,利用H2S介導(dǎo)的反應(yīng)原位生成了一種近紅外光熱試劑并將其用于成像和光控藥物釋放,該試劑具有靶向治療具有豐富H2S的癌癥的能力。
實(shí)驗(yàn)結(jié)果表明,該納米平臺(tái)可被H2S激活并產(chǎn)生NIR II發(fā)射,也能被紅外光控制以釋放藥物喜樹(shù)堿-11。實(shí)驗(yàn)在HCT116荷瘤小鼠模型上證明該納米平臺(tái)可顯著抑制腫瘤生長(zhǎng),副作用也很低。因此,這一研究所開(kāi)發(fā)的納米診療平臺(tái)也為實(shí)現(xiàn)NIR II成像指導(dǎo)的精確醫(yī)學(xué)提供了新的思路。
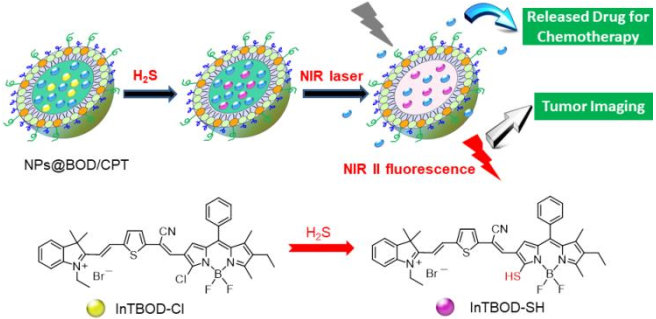
Ben Shi, Ning Ren, Ying Zhu, Chunhai Fan, Chunchang Zhao. et al. A Theranostic Nanoplatform with Hydrogen Sulfide-Activatable NIR Responsiveness for Imaging-Guided On-Demand Drug Release. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201909883
https://onlinelibrary.wiley.com/doi/10.1002/anie.201909883
20. JACS:利用多功能分子前藥靶向治療腫瘤
上海大學(xué)Jonathan L. Sessler教授、高麗大學(xué)Sung-Gil Chi教授和Jong Seung Kim教授合作構(gòu)建了一種分子結(jié)構(gòu)(K1),用于實(shí)現(xiàn)向異質(zhì)腫瘤遞送活性前藥。K1依賴于兩種腫瘤微環(huán)境的條件(GSH和H2O2)去觸發(fā)誘導(dǎo)前藥激活,其在體外氧化應(yīng)激和還原性應(yīng)激條件下會(huì)釋放活性藥物SN- 38。
實(shí)驗(yàn)表明,COX-2陽(yáng)性侵襲性結(jié)腸癌細(xì)胞(SW620和LoVo)會(huì)特異性攝取K1,而與游離的SN-38相比,K1的抗癌活性有明顯增強(qiáng)。同時(shí),K1還可以下調(diào)各種癌癥生存信號(hào)通路(p38 AKT, IL-6、VEGF和TNF-α)并上調(diào)抗炎響應(yīng)(IL-10)。與對(duì)照組SN-38和DMSO相比,K1在體內(nèi)治療腫瘤時(shí)也具有更好的療效,且在給藥劑量下沒(méi)有產(chǎn)生明顯的毒性作用。
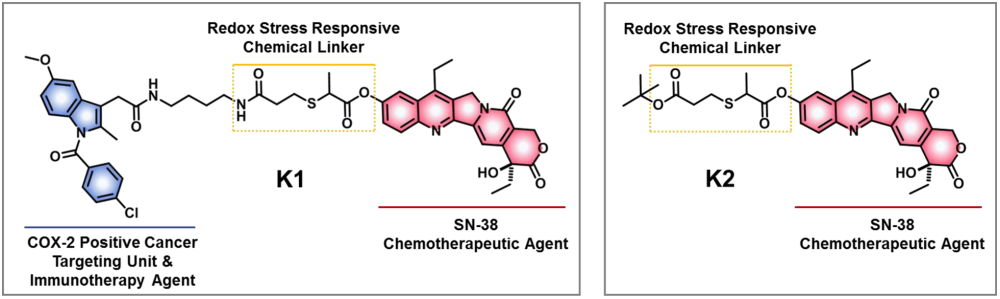
Amit Sharma, Jonathan L. Sessler, Sung-Gil Chi, Jong Seung Kim. et al. Targeting Heterogeneous Tumors Using a Multifunctional Molecular Prodrug. Journal of the American Chemical Society. 2019
DOI: 10.1021/jacs.9b07171
https://pubs.acs.org/doi/10.1021/jacs.9b07171
21. ACS Nano:膠原酶納米顆粒可增強(qiáng)藥物在胰腺腫瘤內(nèi)的穿透性
胰腺導(dǎo)管腺癌(PDAC)中發(fā)生的細(xì)胞外基質(zhì)(ECM)過(guò)表達(dá)會(huì)限制藥物進(jìn)入腫瘤,并與預(yù)后不良有關(guān)。以色列理工學(xué)院Avi Schroeder教授團(tuán)隊(duì)證明了利用基于蛋白水解酶納米顆粒進(jìn)行預(yù)處理可以分解致密的PDAC膠原基質(zhì),從而增加藥物在胰腺腫瘤中的穿透。實(shí)驗(yàn)制備了一種封裝有膠原酶的、尺寸為100nm的脂質(zhì)體,它可以保護(hù)膠原酶以免過(guò)早地失活,并延長(zhǎng)其在靶點(diǎn)部位的釋放速率。
膠原蛋白是PDAC基質(zhì)的主要成分,小鼠的病變胰腺中膠原蛋白含量為12.8±2.3%,而健康小鼠為1.4±0.4%。實(shí)驗(yàn)通過(guò)靜脈注射納米顆粒,發(fā)現(xiàn)其在8 h后會(huì)到達(dá)胰腺,使纖維化組織水平降低到5.6±0.8%。研究結(jié)果證明,通過(guò)膠原酶預(yù)處理會(huì)提高藥物進(jìn)入胰腺的效率,從而改善對(duì)PDAC的治療效果。并且這種降解ECM的方法也不會(huì)增加循環(huán)腫瘤細(xì)胞的數(shù)量和轉(zhuǎn)移。
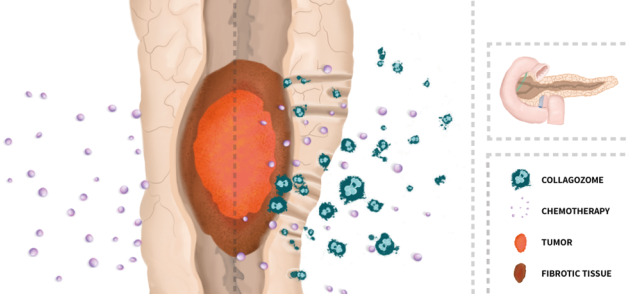
Assaf Zinger, Avi Schroeder. et al. Collagenase Nanoparticles Enhance the
Penetration of Drugs into Pancreatic Tumors. ACS Nano. 2019
DOI: 10.1021/acsnano.9b02395
https://pubs.acs.org/doi/10.1021/acsnano.9b02395
22. Nano Lett.:磁性納米復(fù)合材料用于對(duì)腫瘤的藥物釋放進(jìn)行定量監(jiān)測(cè)
對(duì)體內(nèi)的藥物釋放進(jìn)行監(jiān)測(cè)可以為指導(dǎo)用藥提供準(zhǔn)確可靠的信息。磁性粒子成像(MPI)是以超順磁性納米粒子作為對(duì)比劑和唯一信號(hào)源的一種成像模式,具有很高的組織穿透深度和可量化的信號(hào)強(qiáng)度,因此是一種很好的用于監(jiān)測(cè)體內(nèi)藥物釋放的理想仿生。
斯坦福大學(xué)醫(yī)學(xué)院Bryan Ronain Smith教授團(tuán)隊(duì)設(shè)計(jì)了一種超順磁性的核殼納米復(fù)合材料,并利用其對(duì)化療藥物DOX進(jìn)行負(fù)載,從而進(jìn)行雙藥遞送和MPI的定量示蹤。該納米復(fù)合材料在弱酸性的微環(huán)境(pH = 6.5)下會(huì)發(fā)生降解進(jìn)而持續(xù)釋放DOX,并且Fe3O4納米團(tuán)簇也會(huì)逐漸分解并引起MPI信號(hào)變化。研究結(jié)果發(fā)現(xiàn),該納米復(fù)合材料誘導(dǎo)的MPI信號(hào)變化與阿霉素的釋放速率呈線性相關(guān)(R2 = 0.99),并在細(xì)胞水平和腫瘤小鼠模型上證明了這一結(jié)論。
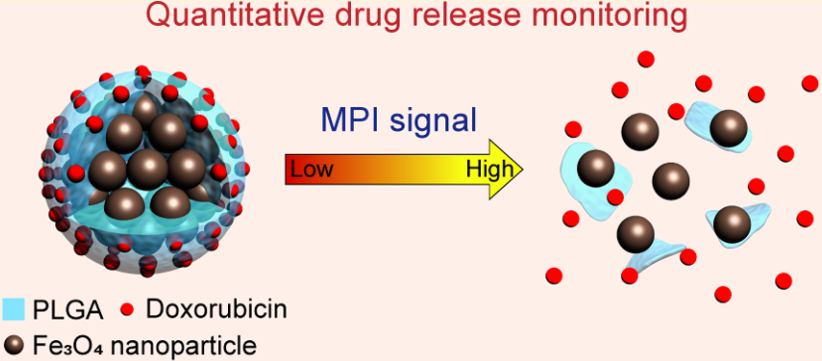
Xingjun Zhu, Jianfeng Li, Bryan Ronain Smith. et al. Quantitative Drug Release Monitoring in Tumors of Living Subjects by Magnetic Particle Imaging Nanocomposite. Nano Letters. 2019
DOI: 10.1021/acs.nanolett.9b01202











