1. Anal. Chem.:對(duì)腫瘤內(nèi)的甲基乙二醛進(jìn)行成像以監(jiān)測(cè)乙二醛酶1的活性
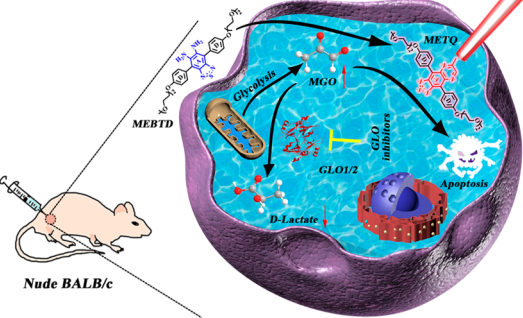
準(zhǔn)確檢測(cè)腫瘤內(nèi)的甲基乙二醛(MGO)及其解毒劑乙二醛酶1 (GLO1)對(duì)于理解其在腫瘤發(fā)生和發(fā)展中的作用來(lái)說(shuō)至關(guān)重要。然而,目前可對(duì)腫瘤內(nèi)源性的MGO和GLO1進(jìn)行原位熒光檢測(cè)的探針還尚未見(jiàn)報(bào)道。中科院上海藥物研究所丁春勇研究員、華東師范大學(xué)徐志愛(ài)教授和張文教授合作開(kāi)發(fā)了一種近紅外(NIR)熒光探針MEBTD用于檢測(cè)腫瘤內(nèi)的MGO。
與之前報(bào)道的MGO熒光探針相比,MEBTD具有近紅外發(fā)光、高選擇性、低檢測(cè)限和很高的熒光開(kāi)關(guān)信號(hào)比。實(shí)驗(yàn)結(jié)果表明,該探針可以通過(guò)對(duì)腫瘤內(nèi)的MGO進(jìn)行實(shí)時(shí)原位成像來(lái)檢測(cè)GLO1的活性和監(jiān)測(cè)GLO1抑制劑的治療效果。此外,MEBTD也可以在體內(nèi)對(duì)由GLO1抑制劑誘導(dǎo)產(chǎn)生的MGO進(jìn)行可視化成像。這一研究所開(kāi)發(fā)的MEBTD也是首個(gè)可用于對(duì)活體動(dòng)物腫瘤內(nèi)的MGO進(jìn)行特異性成像的近紅外熒光探針,其在腫瘤診療領(lǐng)域也有著廣闊的應(yīng)用前景。
Chunyong Ding, FengyangWang, Yijing Dang, Zhiai Xu, Wen Zhang. et al. Imaging Tumorous Methylglyoxalby an Activatable Near-Infrared
Fluorescent Probe forMonitoring Glyoxalase 1 Activity. Analytical Chemistry. 2019
DOI:10.1021/acs.analchem.9b03600
https://pubs.acs.org/doi/10.1021/acs.analchem.9b03600
2. Theranostics:共負(fù)載親/疏水性藥物的免疫刺激載體用于聯(lián)合治療
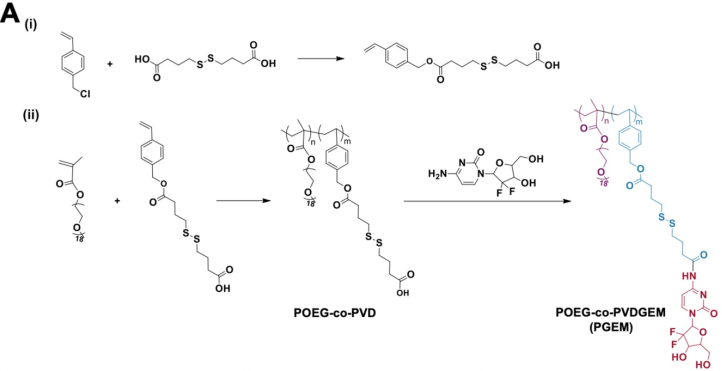
開(kāi)發(fā)可以有效穿透間質(zhì)致密的腫瘤的小型納米材料是癌癥納米醫(yī)學(xué)所面臨的一大挑戰(zhàn),而如何實(shí)現(xiàn)利用小尺寸載體親/疏水性抗癌藥物進(jìn)行有效地共負(fù)載則是一個(gè)更大的難題。匹茲堡大學(xué)Jingjing Sun博士和Song Li教授合作設(shè)計(jì)了一種新型的、對(duì)氧化還原響應(yīng)的吉西他濱(GEM)共軛聚合物PGEM,并將其作為一種小型的納米載體來(lái)共遞送親水性GEM和疏水性紫杉醇(PTX)。
實(shí)驗(yàn)對(duì)PTX/PGEMNPs的體外理化和生物學(xué)特性進(jìn)行了表征,并評(píng)估了PGEM載體在多種小鼠腫瘤模型中選擇性共傳遞GEM和PTX的效率和PTX/PGEM納米顆粒治療后腫瘤免疫微環(huán)境的變化。結(jié)果表明,PGEM聚合物可以負(fù)載多種疏水試劑,具有很高的載藥能力和良好的穩(wěn)定性。并且該小尺寸載體比相對(duì)較大的藥物載體在腫瘤的積累和穿透方面更為有效。PGEM載體不僅很好地保留了GEM的藥理活性,還能增強(qiáng)T細(xì)胞的免疫響應(yīng),在于PTX相結(jié)合后可顯著提高對(duì)多種小鼠腫瘤模型和結(jié)腸癌PDX模型的抗腫瘤活性。因此這一研究不僅提供了一種能夠高效負(fù)載多種親/疏水藥物的小型載體平臺(tái),而且也為增強(qiáng)載體的腫瘤穿透性和提高抗腫瘤免疫治療提供了一個(gè)新的策略。
Jingjing Sun, YichaoChen, Song Li. et al. High Loading of Hydrophobic and Hydrophilic Agents viaSmall Immunostimulatory Carrier for Enhanced Tumor Penetration andCombinational Therapy. Theranostics. 2019
DOI: 10.7150/thno.38287
https://www.thno.org/v10p1136.htm
3. Theranostics:嵌合肽超分子納米顆粒用于靶向遞送miRNA-9治療胰腺癌
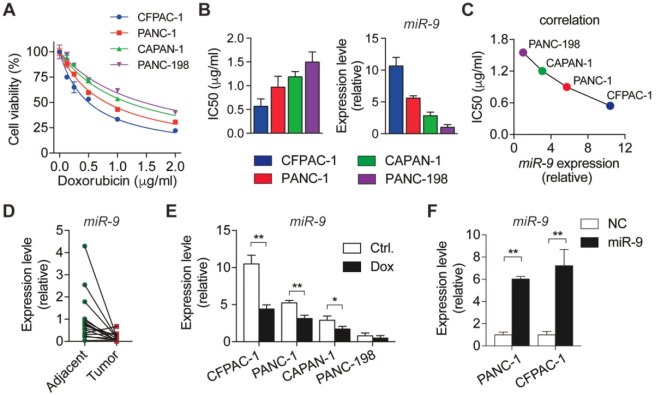
胰腺導(dǎo)管腺癌(PDAC)是一種預(yù)后不良的高致死率疾病。目前已有許多研究對(duì)MicroRNAs (miRNAs)在疾病特別是癌癥中的作用進(jìn)行深入研究,這也使得miRNAs成為疾病診療領(lǐng)域的一種全新工具和靶標(biāo)。浙江同德醫(yī)院陳偉教授和柴可群教授合作構(gòu)建了一種新型嵌合肽超分子納米顆粒遞送系統(tǒng)PL-1/miR-9,并將其用于靶向網(wǎng)蛋白-1 (PL-1)的、對(duì)PDAC特異性的miR-9的體內(nèi)外遞送。
結(jié)果表明,PL-1/miR-9納米復(fù)合物可以通過(guò)下調(diào)eIF5A2的表達(dá)來(lái)抑制自噬和誘導(dǎo)細(xì)胞凋亡,進(jìn)而顯著提高阿霉素的抗癌作用。并且miR-9可通過(guò)與eIF5A2的3'-未翻譯區(qū)(3'-UTR)結(jié)合,進(jìn)而直接靶向eIF5A2轉(zhuǎn)錄物,從而降低eIF5A2在PDAC細(xì)胞中分泌蛋白和表達(dá)水平。因此PL-1/miR-9納米復(fù)合物可以作為一種高效的腫瘤靶向抗癌策略,為協(xié)同治療PDAC提供了一個(gè)新的治療靶點(diǎn)。
Ying Wu, Yuexiao Tang,Shangzhi Xie, Kequn Chai, Wei Chen. et al. Chimeric peptide supramolecularnanoparticles for plectin-1 targeted miRNA-9 delivery in pancreatic cancer. Theranostics.2019
DOI: 10.7150/thno.38327
https://www.thno.org/v10p1151.htm
4. Chem. Soc. Rev.:利用組裝策略構(gòu)建的有機(jī)造影劑及其生物成像應(yīng)用
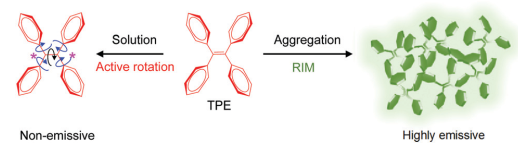
大量的研究結(jié)果表明,通過(guò)組裝構(gòu)建的超分子有機(jī)材料是一類非常適合用于生物醫(yī)學(xué)成像領(lǐng)域的造影劑,進(jìn)而為疾病的診斷提供了許多高效的新方法。香港科技大學(xué)唐本忠院士和梨花女子大學(xué)Juyoung Yoon教授合作綜述了近年來(lái)用于熒光和光聲成像的組裝型有機(jī)染料,對(duì)這類材料的設(shè)計(jì)策略和制備研究進(jìn)展進(jìn)行了詳細(xì)介紹;并對(duì)該領(lǐng)域面臨的挑戰(zhàn)難題及發(fā)展前景進(jìn)行了展望。
Hong-Bo Cheng, YuanyuanLi, Ben Zhong Tang, Juyoung Yoon. Assembly strategies of organic-based imaging agentsfor fluorescence and photoacoustic bioimaging applications. Chemical SocietyReviews. 2019
DOI:10.1039/C9CS00326F
https://pubs.rsc.org/en/content/articlelanding/2020/cs/c9cs00326f#!divAbstract
5. Chem. Sci.:光調(diào)控的適配體傳感器用于實(shí)時(shí)監(jiān)測(cè)活細(xì)胞線粒體內(nèi)ATP的變化
熒光適配體傳感器在用于小分子代謝物的細(xì)胞內(nèi)成像方面具有良好的應(yīng)用潛力。這類代謝物在不同亞細(xì)胞位置上的分布往往不同,其濃度和位置也會(huì)隨時(shí)間波動(dòng),因此對(duì)這些代謝物進(jìn)行時(shí)空控制監(jiān)測(cè)的難度也很大。中科院蘇州納米所裴仁軍研究員、伊利諾伊大學(xué)香檳分校陸藝教授和南京大學(xué)郭子建院士合作報(bào)道了一種可被光調(diào)控的功能化適配體傳感器,它能夠利用修飾的DQAsomes去靶向線粒體,進(jìn)而可對(duì)活細(xì)胞線粒體內(nèi)的ATP進(jìn)行時(shí)空監(jiān)測(cè)。
由于具有光調(diào)控的性能,該適配體傳感器在到達(dá)線粒體之前不會(huì)被激活,而在光的照射下則會(huì)激活其傳感性能。研究表明,該傳感器的檢測(cè)限為3.7 mM,并具有高選擇性,可以檢測(cè)由Ca2+或寡霉素誘導(dǎo)產(chǎn)生的線粒體內(nèi)ATP濃度變化。
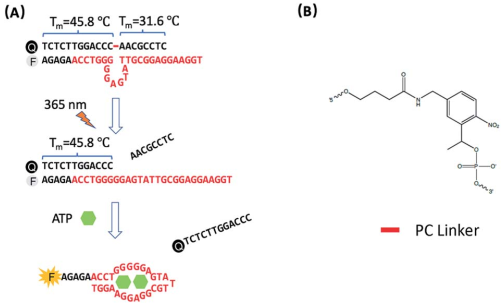
Shanni Hong, Zijian Guo,Renjun Pei, Yi Lu. et al. A photo-regulated aptamer sensor for spatiotemporallycontrolled monitoring of ATP in the mitochondria of living cells. ChemicalScience. 2019
DOI: 10.1039/C9SC04773E
https://pubs.rsc.org/en/content/articlelanding/2020/sc/c9sc04773e#!divAbstract
6. Anal. Chem.:具有光學(xué)可調(diào)羥基的紅色熒光團(tuán)用于對(duì)硝基還原酶進(jìn)行成像
熒光分子成像因其具有諸多的優(yōu)點(diǎn)而受到越來(lái)越多的關(guān)注。湖南大學(xué)袁林教授團(tuán)隊(duì)通過(guò)調(diào)節(jié)分子平面度和控制分子內(nèi)的扭曲電荷轉(zhuǎn)移效應(yīng),采用保護(hù)和去保護(hù)羥基的方法,通過(guò)逐步修飾的策略成功地制備出一種具有光學(xué)可調(diào)羥基的多功能長(zhǎng)波長(zhǎng)熒光團(tuán)LDOH-4,它具有良好的化學(xué)和光學(xué)性能。
實(shí)驗(yàn)基于這一策略設(shè)計(jì)了一種硝基還原酶激活的TP熒光探針LDO-NTR,它不僅能在體外敏感地識(shí)別NTR并使其響應(yīng)信號(hào)大大增強(qiáng)(超過(guò)310倍),而且還能在乏氧腫瘤小鼠模型體內(nèi)對(duì)NTR進(jìn)行雙光子成像。因此這一研究所開(kāi)發(fā)的具有光學(xué)可調(diào)羥基的長(zhǎng)波長(zhǎng)熒光團(tuán)也有望成為生物化學(xué)和生物醫(yī)學(xué)領(lǐng)域的檢測(cè)新工具。
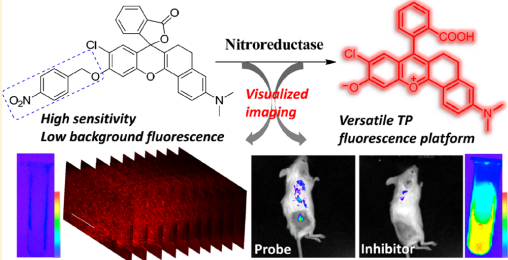
Rong Peng, Jie Yuan, DanCheng, Lin Yuan. et al. Evolving a Unique Red-Emitting Fluorophore with anOptically Tunable Hydroxy Group for Imaging Nitroreductase in Cells, in Tissues,and in Vivo. Analytical Chemistry. 2019
DOI:10.1021/acs.analchem.9b04564
https://pubs.acs.org/doi/10.1021/acs.analchem.9b04564
7. Chem. Rev.:肽基疫苗的研究進(jìn)展和面臨的挑戰(zhàn)
疫苗對(duì)傳染病的管理和預(yù)防具有重要的意義。而作為一種預(yù)防而非治療癌癥、阿爾茨海默病等慢性疾病的方法,開(kāi)發(fā)針對(duì)這類疾病的疫苗也引起了研究人員相當(dāng)大的興趣。阿爾伯特愛(ài)因斯坦醫(yī)學(xué)院Jonathan R. Lai教授團(tuán)隊(duì)綜述討論了肽基疫苗在三個(gè)疾病領(lǐng)域(傳染病、阿爾茨海默病和癌癥)的應(yīng)用;討論了影響疫苗有效性的因素以及設(shè)計(jì)調(diào)整這些因素的策略;對(duì)經(jīng)過(guò)臨床實(shí)驗(yàn)的疫苗以及新型疫苗進(jìn)行了檢測(cè),并探討了這一領(lǐng)域當(dāng)前所面臨的挑戰(zhàn)和相應(yīng)的解決措施。
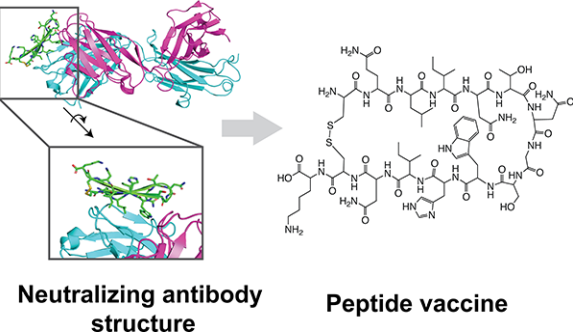
Ryan J. Malonis, Ryan J.Malonis. et al. Peptide-Based Vaccines: Current Progress and Future Challenges.Chemical Reviews. 2019
DOI: 10.1021/acs.chemrev.9b00472
https://pubs.acs.org/doi/10.1021/acs.chemrev.9b00472
8. Anal. Chem.:DNA包覆的銀納米片用于檢測(cè)細(xì)胞分裂周期內(nèi)的內(nèi)源性H2S
生化傳感對(duì)于充分了解各種生理和病理事件來(lái)說(shuō)是必不可少的。硫化氫(H2S)是體內(nèi)重要的內(nèi)源性氣體遞質(zhì),其濃度水平與其在細(xì)胞分裂周期不同階段的生物學(xué)功能密切相關(guān)。湖南大學(xué)符婷博士和合工大劉洪林教授合作報(bào)告了一種在細(xì)胞分裂的不同階段檢測(cè)H2S的簡(jiǎn)便策略。實(shí)驗(yàn)開(kāi)發(fā)了一種由雙鏈DNA (dsDNA)穩(wěn)定的銀納米片(AgNF@dsDNA)熒光納米傳感器,其傳感原理是利用H2S對(duì)AgNF@dsDNA進(jìn)行選擇性刻蝕以生成Ag2S。
起初,AgNFs會(huì)通過(guò)表面能量轉(zhuǎn)移來(lái)起到熒光猝滅劑的作用;而在蝕刻作用發(fā)生后,修飾的熒光團(tuán)的熒光得以恢復(fù),并且兩個(gè)熒光團(tuán)之間也會(huì)產(chǎn)生高效的熒光共振能量轉(zhuǎn)移(FRET)。FRET的信號(hào)變化也成功地使該傳感器能夠?qū)罴?xì)胞在G1、S、G2時(shí)內(nèi)源性H2S的變化進(jìn)行半定量成像。結(jié)果表明,該納米傳感器具有良好的線性響應(yīng)濃度范圍(1-10μM)。而通過(guò)對(duì)細(xì)胞分裂周期內(nèi)的內(nèi)源性H2S進(jìn)行熒光成像,也可以將G0與G1等細(xì)胞周期區(qū)分開(kāi)來(lái)。因此,這一研究也為利用納米傳感技術(shù)以對(duì)細(xì)胞分裂周期的不同階段進(jìn)行生物成像和傳感奠定了良好的基礎(chǔ)。
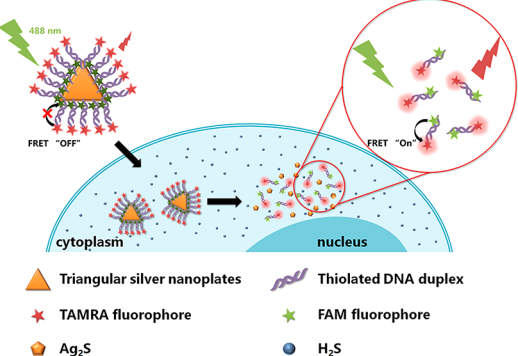
Sitao Xie, Ting Fu,Honglin Liu. et al. DNA-Capped Silver Nanoflakes as Fluorescent Nanosensor for HighlySensitive Imaging of Endogenous H2S in Cell Division Cycles. AnalyticalChemistry. 2019
DOI:10.1021/acs.analchem.9b02527
https://pubs.acs.org/doi/10.1021/acs.analchem.9b02527
9. Anal. Chem.:碳點(diǎn)作為熒光/比色探針用于實(shí)時(shí)檢測(cè)次氯酸和抗壞血酸
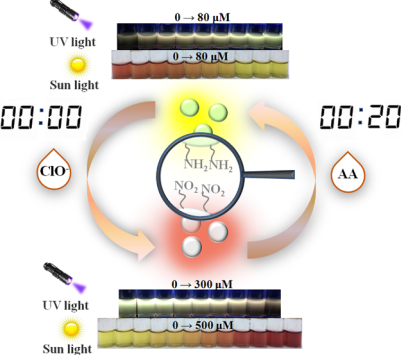
次氯酸根(ClO?)和抗壞血酸(AA)與氧化應(yīng)激相關(guān)疾病密切相關(guān),因此開(kāi)發(fā)可以靈敏、快速地對(duì)ClO?和AA進(jìn)行檢測(cè)的傳感器具有重要的意義。蘭州大學(xué)任翠領(lǐng)教授團(tuán)隊(duì)合成了一種可以對(duì)ClO?和AA產(chǎn)生快速、可逆和動(dòng)態(tài)的熒光/比色響應(yīng)的新型碳點(diǎn)材料(RD-CDs)。
在熒光的模式下,該納米傳感器對(duì)ClO?和AA具有高選擇性和低檢測(cè)限等優(yōu)點(diǎn),這使得該傳感器可以動(dòng)態(tài)地檢測(cè)活細(xì)胞中的ClO?和AA,并可在熒光顯微鏡下對(duì)它們進(jìn)行監(jiān)測(cè);在比色的模式下,該傳感器可以利用紫外-可見(jiàn)光對(duì)ClO?和AA進(jìn)行檢測(cè),濃度范圍分別為5-200μM和1-30μM。由此證明在熒光和比色兩種模式下,RD-CDs都可以很好地對(duì)細(xì)胞和體液中ClO?和AA的濃度進(jìn)行測(cè)定。
Zhenni Wei, Cuiling Ren.et al. Carbon Dots as Fluorescent/Colorimetric Probes for Real-Time Detectionof Hypochlorite and Ascorbic Acid in Cells and Body Fluid. AnalyticalChemistry. 2019
DOI:10.1021/acs.analchem.9b03272
https://pubs.acs.org/doi/10.1021/acs.analchem.9b03272
10. Acc. Chem. Res.:利用順磁性金屬和19F磁共振成像對(duì)生物活性進(jìn)行傳感
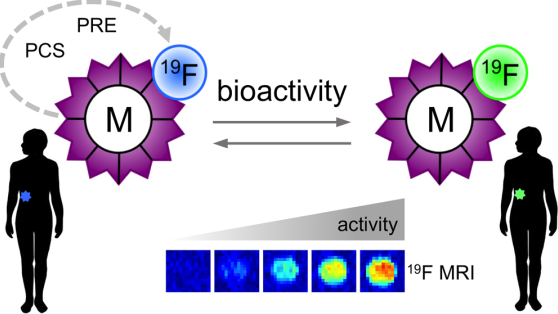
氟磁共振成像(19FMRI)是一種很有前途的生物成像技術(shù),目前已有許多研究開(kāi)發(fā)了一系列用于這種成像方式的造影劑,包括小分子全氟化碳化合物、富含氟的大分子、納米顆粒以及順磁性金屬等。其中,順磁性金屬與氟化試劑的結(jié)合也為控制19F原子核的弛豫和化學(xué)位移提供了一個(gè)新的方法。19F核磁共振成像試劑的一個(gè)重要應(yīng)用是被設(shè)計(jì)成響應(yīng)型材料,進(jìn)而可以用于檢測(cè)生物活性,如酶活性、氧化還原活性和離子活性等。而順磁性試劑就非常適合用于這種對(duì)活性的傳感,因?yàn)榻饘購(gòu)?fù)合物可以被設(shè)計(jì)成對(duì)特定的生物活動(dòng)響應(yīng),進(jìn)行給出相應(yīng)的19F響應(yīng)變化。
德州大學(xué)奧斯汀分校Emily L. Que教授團(tuán)隊(duì)重點(diǎn)介紹了該團(tuán)隊(duì)所利用順磁性金屬來(lái)調(diào)節(jié)19F信號(hào)以制備的活性探針;討論了利用不同元素價(jià)態(tài)之間的轉(zhuǎn)換來(lái)對(duì)生物活動(dòng)做出響應(yīng)從而提供不同的19F信號(hào)的應(yīng)用;并對(duì)19F磁共振分子成像所面臨的主要難題和解決措施進(jìn)行了詳細(xì)探討。
Da Xie, Meng Yu, EmilyL. Que. et al. 19F Magnetic Resonance Activity-Based Sensing UsingParamagnetic Metals. Accounts of Chemical Research. 2019
DOI:10.1021/acs.accounts.9b00352
https://pubs.acs.org/doi/10.1021/acs.accounts.9b00352
11. Anal. Chem.:CsPbBr3量子點(diǎn)用于對(duì)大鼠腦微透析液中硫化氫的敏感熒光傳感
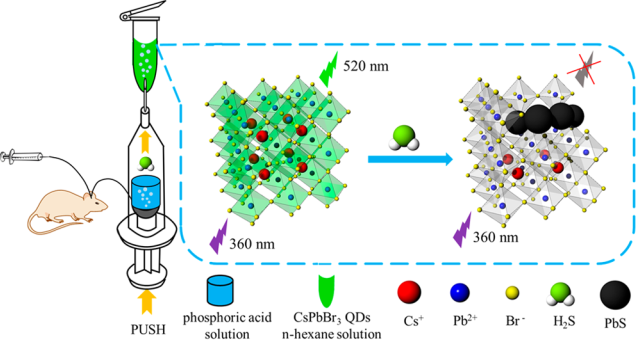
鈣鈦礦量子點(diǎn)在水溶液中的不穩(wěn)定和不溶性阻礙了其在極性溶劑中的應(yīng)用。硫化氫(H2S)是一種劇毒氣體污染物,也是存在于多種生理過(guò)程中的內(nèi)源性氣體信號(hào)分子。廈門大學(xué)董諾博士、福州大學(xué)羅芳博士和林振宇教授合作設(shè)計(jì)了一種簡(jiǎn)單的將H2S從水溶液中分離的裝置,并以CsPbBr3量子點(diǎn)(CsPbBr3 QDs)作為檢測(cè)探針,開(kāi)發(fā)了一種新型、可快速檢測(cè)H2S的熒光傳感器。
實(shí)驗(yàn)將H2S加入到磷酸溶液中后可以使得H2S從水溶液中逸出,從而進(jìn)入含有CsPbBr3QDs的正己烷溶液中并導(dǎo)致CsPbBr3 QDs的熒光發(fā)生猝滅。實(shí)驗(yàn)表明,該系統(tǒng)的熒光強(qiáng)度與H2S的濃度存在線性關(guān)系(0?100 μM),其檢出限為0.18μM,并在檢測(cè)大鼠腦微透析液中的H2S時(shí)表現(xiàn)出很好的效果。
Chaoqun Chen, Qing Cai,Fang Luo, Nuo Dong, Zhenyu Lin. et al. Sensitive Fluorescent Sensor forHydrogen Sulfide in Rat Brain Microdialysis via CsPbBr3 QuantumDots. Analytical Chemistry. 2019
DOI: 10.1021/acs.analchem.9b04387
https://pubs.acs.org/doi/10.1021/acs.analchem.9b04387
12. Chem. Sci.:近紅外納米探針用于對(duì)治療反應(yīng)進(jìn)行動(dòng)態(tài)評(píng)估
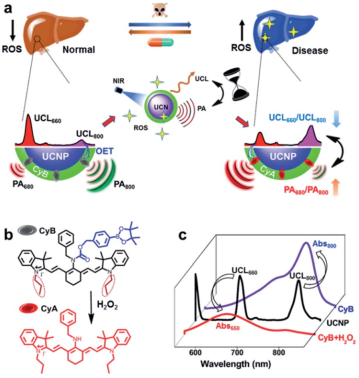
藥物干預(yù)治療需要對(duì)病理狀態(tài)進(jìn)行及時(shí)、動(dòng)態(tài)和準(zhǔn)確的評(píng)估。傳統(tǒng)的臨床技術(shù)依賴于對(duì)生物組織和血液進(jìn)行檢測(cè),但由于其具有諸多的局限性而受到很大的限制。新加坡南洋理工大學(xué)邢本剛教授團(tuán)隊(duì)創(chuàng)新性地將上轉(zhuǎn)換納米晶體和對(duì)自由基響應(yīng)的發(fā)色團(tuán)進(jìn)行組合,從而將可穿透深層組織的多光譜光聲斷層成像(MSOT)和近紅外(NIR)光學(xué)成像技術(shù)結(jié)合起來(lái)。
在治療的過(guò)程中,藥物刺激產(chǎn)生的活性氧(ROS)會(huì)與探針之間發(fā)生特異性反應(yīng)從而導(dǎo)致吸收移位,進(jìn)而這一變化被MSOT捕獲。同時(shí)與MSOT相比,由自由基引發(fā)的多光譜上轉(zhuǎn)換發(fā)光(UCL)響應(yīng)則呈現(xiàn)出相反的趨勢(shì)。這種反向比值雙模態(tài)成像結(jié)果也提供了一個(gè)很好的交叉參照系統(tǒng),從而保證了最大的傳感特異性和靈敏度,因此該系統(tǒng)能夠在體內(nèi)進(jìn)行精確的疾病治療評(píng)估。
Zhimin Wang, XiangzhaoAi, Bengang Xing. et al. NIR nanoprobe-facilitated cross-referencing manifestationof local disease biology for dynamic therapeutic response assessment. ChemicalScience. 2019
DOI: 10.1039/C9SC04909F
https://pubs.rsc.org/en/content/articlelanding/2020/sc/c9sc04909f#!divAbstract
13. Nat. Rev. Cancer.:大腦免疫學(xué)和針對(duì)腦腫瘤的免疫治療
膠質(zhì)瘤是最常見(jiàn)的惡性原發(fā)性腦腫瘤,其致死率也和很高。過(guò)去5年來(lái),許多工作對(duì)中樞神經(jīng)系統(tǒng)(CNS)內(nèi)的免疫系統(tǒng)解剖學(xué)、遺傳學(xué)和功能進(jìn)行了研究,這些工作也為實(shí)現(xiàn)成功的腦瘤免疫治療提供了很多的幫助。
杜克大學(xué)醫(yī)學(xué)中心John H. Sampson團(tuán)隊(duì)對(duì)腦免疫學(xué)和針對(duì)腦腫瘤的免疫治療相關(guān)研究進(jìn)行了綜述,這類研究對(duì)于治療中樞神經(jīng)系統(tǒng)內(nèi)發(fā)生的多種腫瘤來(lái)說(shuō)也具有重要的意義。而由于成功的治療往往需要進(jìn)行有效的特異性遞送,因此惡性膠質(zhì)瘤在遺傳和免疫水平上存在的巨大異質(zhì)性仍然是該領(lǐng)域所需解決的一個(gè)巨大的挑戰(zhàn)。
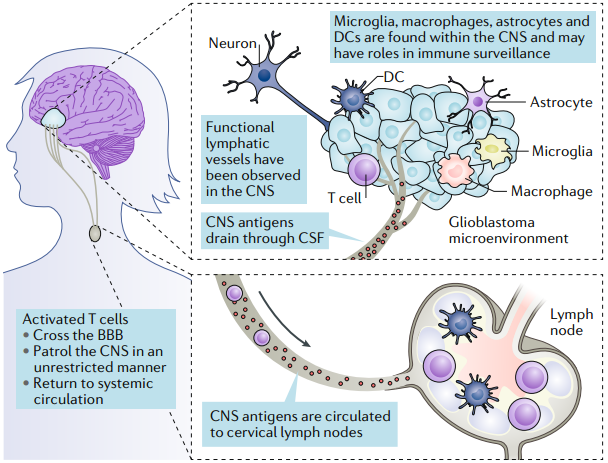
John H. Sampson. et al.Brain immunology and immunotherapy in brain tumours. Nature Review Cancer. 2019
https://www.nature.com/articles/s41568-019-0224-7
14. Angew:聯(lián)硒化物-培美曲塞組裝體用于癌癥的多模態(tài)治療
免疫治療是一種很有前途的治療癌癥的新方法。然而,目前在臨床上可使用的藥物還很有限,大多數(shù)免疫治療的抗腫瘤療效也有待提高。清華大學(xué)Shiqian Gao博士和許華平教授合作制備了一種聯(lián)硒化物-培美曲塞組裝體材料,它可以將基于自然殺傷(NK)細(xì)胞的癌癥免疫療法與放療和化療結(jié)合為一體。
該組裝體是由培美曲塞和含有胞嘧啶的聯(lián)硒化物通過(guò)氫鍵共同組裝而成。研究發(fā)現(xiàn),在γ射線的輻照下下,氫鍵會(huì)發(fā)生裂解從而釋放培美曲塞。同時(shí),聯(lián)硒化物也可被氧化為硒酸以抑制人白細(xì)胞抗原E (HLA-E)在癌細(xì)胞中的表達(dá),進(jìn)而激活NK細(xì)胞的免疫應(yīng)答。因此這一工作通過(guò)將腫瘤的免疫治療與放療、化療相結(jié)合,為腫瘤治療提供了一種新的聯(lián)合治療策略。
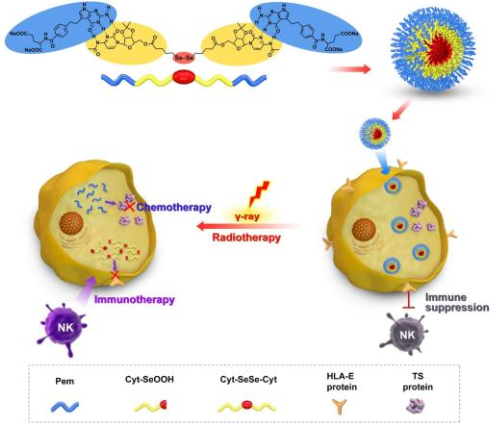
Tianyu Li, ShuojiongPan, Shiqian Gao, Huaping Xu. et al. Diselenide-Pemetrexed Assemblies forCombined Cancer Immuno-, Radio-, and Chemotherapies. Angewandte ChemieInternational Edition. 2019
DOI:10.1002/anie.201914453
https://onlinelibrary.wiley.com/doi/10.1002/anie.201914453
15. Anal. Chem.:智能熒光探針用于癌癥診斷和成像體內(nèi)腫瘤淋巴系統(tǒng)
深圳大學(xué)屈軍樂(lè)教授和楊志剛博士合作設(shè)計(jì)并合成了一種基于分子內(nèi)扭轉(zhuǎn)電荷轉(zhuǎn)移(TICT)的多功能近紅外熒光探針(L),并將其用于癌癥診斷和通過(guò)不同的發(fā)射信號(hào)以對(duì)小鼠淋巴結(jié)進(jìn)行成像。研究發(fā)現(xiàn),相對(duì)于正常細(xì)胞來(lái)說(shuō),該探針能夠優(yōu)先識(shí)別癌細(xì)胞。
并且在生理介質(zhì)下,該探針可以在遠(yuǎn)/近紅外區(qū)對(duì)HAS/BSA實(shí)現(xiàn)熒光的開(kāi)關(guān)響應(yīng),這是由于探針可以與HSA/BSA發(fā)生1:1螯合所導(dǎo)致的。得益于引流腫瘤淋巴系統(tǒng)中積累的白蛋白可以與L形成白蛋白-L熒光復(fù)合物,因此該探針能夠通過(guò)熒光的策略去成像腫瘤小鼠模型體內(nèi)的引流淋巴系統(tǒng)和前哨淋巴結(jié)。
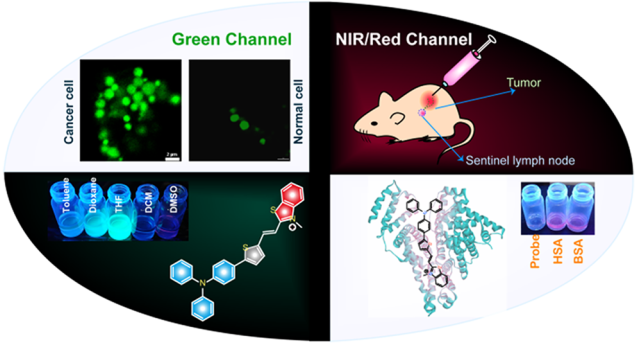
Soham Samanta, MeinaHuang, Junle Qu, Zhigang Yang. et al. Solo Smart Fluorogenic Probe forPotential Cancer Diagnosis and Tracking in Vivo Tumorous Lymphatic Systems viaDistinct Emission Signals. Analytical Chemistry. 2019
DOI:10.1021/acs.analchem.9b04834
https://pubs.acs.org/doi/10.1021/acs.analchem.9b04834
16. Nat. Nanotech.:納米技術(shù)對(duì)微生物群落進(jìn)行干預(yù)以治療癌癥
研究表明,微生物群落是癌癥發(fā)展的重要參與者和驅(qū)動(dòng)者。利用傳統(tǒng)的方法(如抗生素,益生菌和微生物群移植)來(lái)調(diào)控微生物已被證明可以提高癌癥的治療效果,但這類方法也存在諸多的局限性,所以需要開(kāi)發(fā)新型技術(shù)以解決相應(yīng)的問(wèn)題。考慮到納米技術(shù)在癌癥診療領(lǐng)域取得的成功,因此利用納米技術(shù)去調(diào)控微生物群落和腫瘤微環(huán)境的相互作用也有望為癌癥治療提供新的有效策略。
北卡羅萊納大學(xué)教堂山分校Aaron C. Anselmo?教授和黃力夫教授合作對(duì)應(yīng)用納米技術(shù)來(lái)調(diào)控微生物群以治療癌癥的相關(guān)研究工作進(jìn)行了綜述;并對(duì)這一新興領(lǐng)域面臨的挑戰(zhàn)和未來(lái)的發(fā)展前景進(jìn)行了論述和展望。
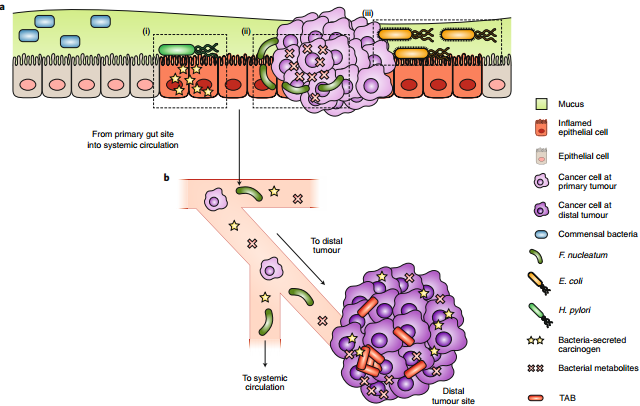
Wantong Song, Aaron C.Anselmo, Leaf Huang. et al. Nanotechnology intervention of the microbiome forcancer therapy. Nature Nanotechnology. 2019
https://www.nature.com/articles/s41565-019-0589-5
17. Nano Lett.:含有水凝膠的持久發(fā)光納米顆粒用于對(duì)腫瘤轉(zhuǎn)移進(jìn)行成像
轉(zhuǎn)移是癌癥發(fā)病和造成死亡的主要原因。天津大學(xué)仰大勇教授團(tuán)隊(duì)制備了一種包含水凝膠(PL-gel)的持久發(fā)光納米顆粒(PLNPs),并將其用于靶向、持續(xù)和無(wú)自身熒光的腫瘤轉(zhuǎn)移成像。PLNPs具有可再生的持久近紅外(NIR)發(fā)光,可以實(shí)現(xiàn)無(wú)背景干擾的深層組織穿透成像。
實(shí)驗(yàn)將PLNPs與4-羧基苯基硼酸(CPBA)相結(jié)合以生成PLNPs-CPBA,該CPBA可特異性識(shí)別轉(zhuǎn)移性乳腺癌細(xì)胞(MBA-MD-231 cells),并可通過(guò)受體介導(dǎo)的內(nèi)吞作用對(duì)癌細(xì)胞進(jìn)行特異性標(biāo)記。而被PLNPs-CPBA標(biāo)記的癌細(xì)胞不會(huì)影響其遷移和侵襲的能力,并具有很好的成像性能和高的存活率。實(shí)驗(yàn)將PLNPs-CPBA進(jìn)一步包裹于藻朊酸鹽中以形成PL-gel,該凝膠可用于持續(xù)釋放PLNPs-CPBA和標(biāo)記腫瘤細(xì)胞的,并且PLNPs-CPBA懸浮液相比,PL-gel表現(xiàn)出更強(qiáng)的可再生持久發(fā)光。實(shí)驗(yàn)結(jié)果表明,PL-gel可以對(duì)腫瘤的轉(zhuǎn)移進(jìn)行無(wú)背景干擾、無(wú)創(chuàng)和高選擇性成像。
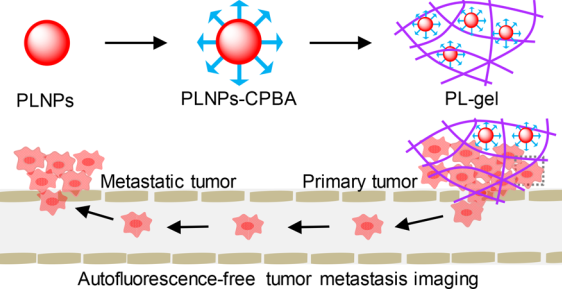
Huaixin Zhao, ChunxiaLiu, Dayong Yang. et al. Persistent Luminescent Nanoparticles ContainingHydrogels for Targeted, Sustained, and Autofluorescence-Free Tumor Metastasis Imaging.Nano Letters. 2019
DOI:10.1021/acs.nanolett.9b03755
https://pubs.acs.org/doi/10.1021/acs.nanolett.9b03755
18. Angew:芳香腈與氨基硫醇的縮合反應(yīng)可在細(xì)胞內(nèi)形成納米顆粒以表征酶活性
6-羥基-2-氰基苯并噻唑(CBT)與半胱氨酸之間的縮合反應(yīng)已被證明具有多種應(yīng)用性能,可以實(shí)現(xiàn)位點(diǎn)特異性的蛋白標(biāo)記和體內(nèi)癌癥成像等。斯坦福大學(xué)醫(yī)學(xué)院饒江宏教授團(tuán)隊(duì)在改變芳香腈和氨基硫醇上的取代基后并對(duì)它們的反應(yīng)活性和形成納米顆粒的能力進(jìn)行了測(cè)試。
實(shí)驗(yàn)通過(guò)結(jié)構(gòu)-活性關(guān)系的研究,確定了形成納米顆粒的最低結(jié)構(gòu)要求,并利用這一縮合反應(yīng)在活細(xì)胞內(nèi)構(gòu)建了熒光探針來(lái)對(duì)半胱天冬酶-3/7和β-半乳糖苷酶的活性進(jìn)行成像。
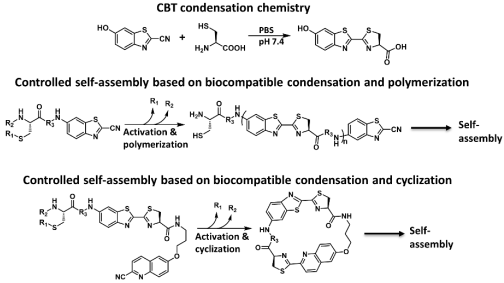
ZixinChen, Min Chen, Yunfeng Cheng, Jianghong Rao. et al. Exploring CondensationReaction Between Aromatic Nitriles and Amino Thiols to Form Nanoparticles inCells for Imaging the Activity of Protease and Glycosidase. Angewandte ChemieInternational Edition. 2019
DOI:10.1002/anie.201913314
https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.201913314
19. Angew:靶向溶酶體的鐵(III)激活銥(III)前藥用于腫瘤診療
中山大學(xué)陳禹博士和巢暉教授合作制備了一種新型的、鐵(III)激活的、溶酶體靶向的銥(III)前體藥(鐵銥)用于胃癌。該復(fù)合物含有m-亞胺兒茶酚基團(tuán),可選擇性地與細(xì)胞內(nèi)游離的鐵(III)結(jié)合并被其氧化,由此可以釋放鐵(II)并在酸性條件下水解胺鍵,生成氨基聯(lián)吡啶銥絡(luò)合物和2-羥基苯醌。
這一系列反應(yīng)具有三方面的性能:鐵(II)可以催化類芬頓反應(yīng)以產(chǎn)生羥基自由基;苯醌類化合物可以干擾呼吸鏈;從原藥到氨基銥復(fù)合物的轉(zhuǎn)化可以使得其磷光和毒性顯著增加。這些性能使得具有高的鐵(III)含量和酸度的癌細(xì)胞對(duì)鐵銥復(fù)合物更加敏感,由此證明它是一種具有高選擇性和高效的診療試劑。
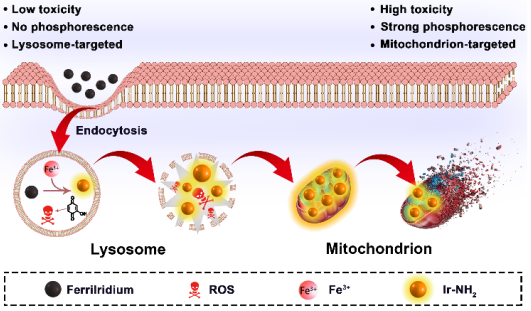
Shi Kuang, Yu Chen, HuiChao. et al. FerriIridium: A Lysosome-Targeting Iridium(III) Prodrug for Iron(III)-ActivatedChemotherapy in Gastric Cancer Cells. Angewandte Chemie International Edition.2019
DOI: 10.1002/anie.201915828
https://onlinelibrary.wiley.com/doi/10.1002/anie.201915828
20. Nanoscale Horiz.綜述:納米技術(shù)用于免疫成像
免疫成像是一個(gè)正在迅速發(fā)展的領(lǐng)域。隨著免疫治療取得顯著的系列進(jìn)展,對(duì)腫瘤免疫治療的反應(yīng)進(jìn)行評(píng)估就尤為重要。它可以將患者分為有響應(yīng)者和無(wú)響應(yīng)者,同時(shí)可以幫助識(shí)別炎癥并更好地了解免疫系統(tǒng)的作用,進(jìn)而改善免疫成像和免疫治療。
已有研究表明,納米材料可以為免疫成像提供很多的新型策略,進(jìn)而實(shí)現(xiàn)多功能性的多模態(tài)成像。密歇根州立大學(xué)Bryan Ronain Smith教授團(tuán)隊(duì)綜述了將納米技術(shù)與免疫成像技術(shù)相結(jié)合的相關(guān)研究,并對(duì)其在臨床中的應(yīng)用前景進(jìn)行展望。
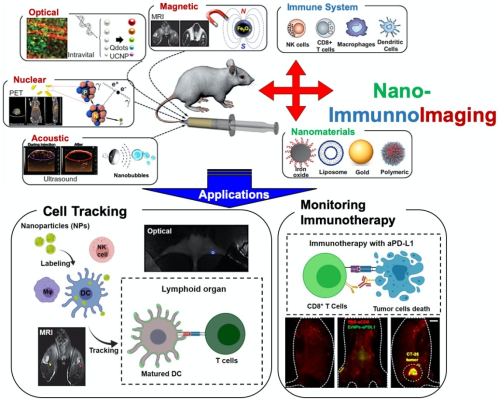
Ping Wang, Taeho Kim,Bryan Ronain Smith. et al. Nano-Immunoimaging. Nanoscale Horizons. 2019
DOI:10.1039/C9NH00514E
https://pubs.rsc.org/en/content/articlelanding/2019/nh/c9nh00514e#!divAbstract
21. Adv. Drug. Deli.Rev.:針對(duì)巨噬細(xì)胞的藥物遞送
巨噬細(xì)胞在抵抗外來(lái)病原體、傷口愈合和調(diào)節(jié)組織穩(wěn)態(tài)方面起著重要的作用。而它們具有多樣性功能的原因在于其具有的表型可塑性,這也使得巨噬細(xì)胞能夠以緊密協(xié)調(diào)的方式對(duì)來(lái)微小的變化做出響應(yīng)。但是當(dāng)這種協(xié)調(diào)被破壞時(shí),巨噬細(xì)胞也可以促進(jìn)許多疾病的發(fā)展,包括癌癥、心血管疾病和自身免疫性疾病等。這些疾病的中心環(huán)節(jié)往往是異常的巨噬細(xì)胞極化。
由于巨噬細(xì)胞扮演著關(guān)鍵的角色,因此將其作為藥物遞送的靶點(diǎn)也受到了研究人員的廣泛關(guān)注。哈佛大學(xué)Samir Mitragotri教授團(tuán)隊(duì)綜述討論了巨噬細(xì)胞在各種炎癥疾病中的作用;總結(jié)了用于調(diào)節(jié)巨噬細(xì)胞的相關(guān)藥物和針對(duì)于巨噬細(xì)胞的藥物遞送系統(tǒng);并對(duì)靶向巨噬細(xì)胞的給藥系統(tǒng)的未來(lái)發(fā)展方向進(jìn)行了論述。
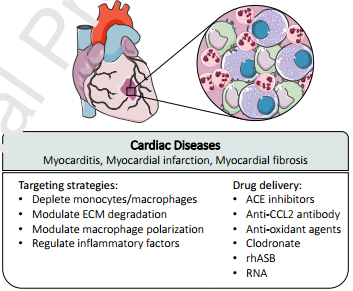
Wei He, SamirMitragotri. et al. Drug delivery to macrophages: A review of targeting drugsand drug carriers to macrophages for inflammatory diseases. Advanced DrugDelivery Reviews. 2019
https://www.sciencedirect.com/science/article/pii/S0169409X1930239X











