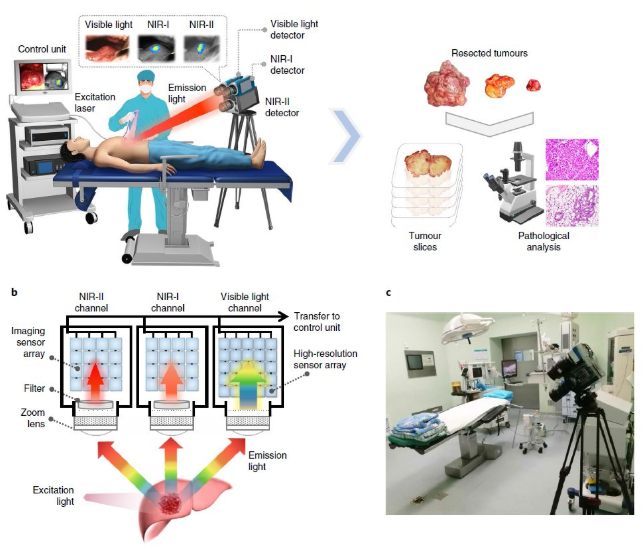
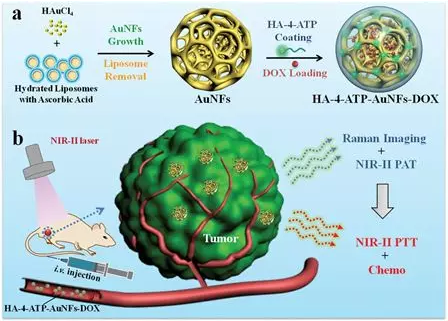
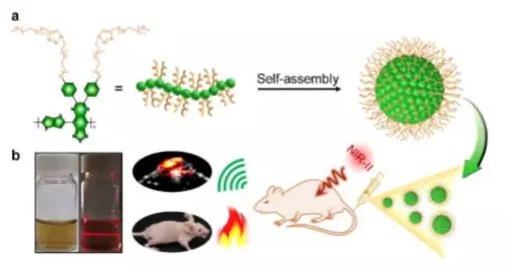
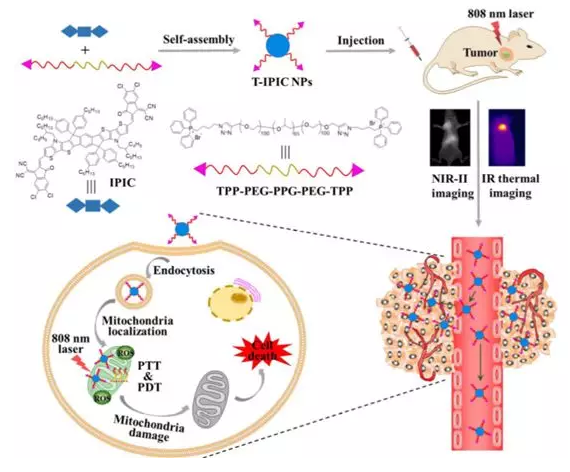
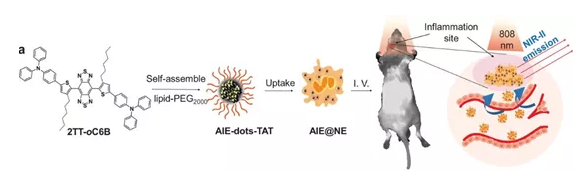
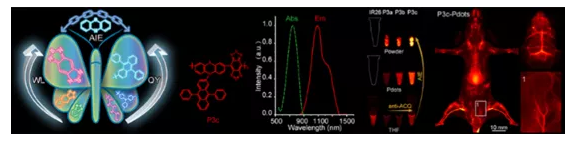
近紅外二區激光(NIR-II�����,1000-1700 nm)操作簡便,在活體組織中具有更少的組織吸收和散射以及更低組織自發熒光特性,可以大大提高組織穿透深度和空間分辨率���,在生物醫學領域中具有廣闊的應用前景。2019年12月23日,中科院自動化研究所田捷研究員和斯坦福大學Sanjiv Sam Gambhir, Zhen Cheng等人報道了一種集成可見光和NIR-I/II多光譜成像儀�����,并在不同的紅外窗口下對其在人體和動物研究中的成像性能進行了表征�����。還報道了23例肝癌患者注射ICG后的可見光�、NIR-I和NIR-II多光譜成像的首次人體研究�����,并比較了每例患者的NIR-I窗口和NIR-I窗口的成像性能�����,評價NIR-I和NIR-II引導手術在臨床上的應用潛力�����。有鑒于此�,本文匯總了近一個月來與NIR-II在生物醫學中的應用相關的研究成果�����。1. 介孔金納米骨架用作近紅外二區的拉曼光生成像和光化學癌癥診療丨AFM在第二近紅外(NIR-II)生物窗口中具有可調表面局部等離子體共振(LSPR)波長的金基納米結構在光熱診療領域越來越受到關注���,但是目前進展卻有限�����。有鑒于此,廈門大學Lei Ren團隊及其合作者使用脂質體作為模合成具有大介孔(≈40nm)的新型金納米框架(AuNFs)用作多模式成像��。所得的AuNFs在近紅外二區表現出強吸收�����,可以用于深部腫瘤的光熱治療(PTT)和光聲(PA)成像��。將阿霉素(DOX)搭載到透明質酸功能化的AuNFs的介孔中后,所得的AuNFs 對CD44過表達的腫瘤細胞表現出靶向能力��。將具有拉曼活性的-氨基硫酚(4-ATP)偶聯到AuNFs后��,可用于拉曼光生成像����。Wang J, Sun J, Wang Y,et al. Gold Nanoframeworks with Mesopores for Raman–Photoacoustic Imaging and Photo-Chemo Tumor Therapy in the SecondNear-Infrared Biowindow [J]. Adv. Funct. Mater. 2020, 1908825DOI: 10.1002/adfm.201908825https://onlinelibrary.wiley.com/doi/10.1002/adfm.2019088252. 石墨烯量子點用于成像指導的近紅外II區光熱治療丨Biomaterials石墨烯量子點(GQDs)因其具有良好的生物相容性和快速的可清除性能����,被認為是一種新興的用于癌癥光熱治療(PTT)的納米材料����。然而��,目前的GQDs一般都是在較短波長(<1000 nm)下的有光吸收,這也限制了其在用于近紅外II(1000-1700 nm, NIR-II)光熱治療時的治療效果�����。南京大學聶蓉蓉����、中科院合肥物質科學研究院陳乾旺和王輝合作報道了一種在NIR-II區(1070 nm)有強吸收的9T-GQDs。該9T-GQDs是以苯酚為單前體�����,通過調節過氧化氫在9T強磁場下的分解����,利用一步溶劑熱處理所合成的。該9T-GQDs的尺寸分布均勻(3.6 nm)��,熒光可調諧 (量子產率16.67%)��,光熱轉換效率高(33.45%)�。體內外實驗結果表明�����,9T-GQDs能有效殺傷腫瘤細胞���,進而抑制腫瘤生長����,并且能在活體小鼠中對腫瘤實現增強的近紅外成像�����,從而表明它是一種性能優異的NIR-II區光學診療納米平臺。Hongji Liu, RongrongNie, Qianwang Chen, Hui Wang. et al. Magnetic-induced graphene quantum dots forimaging-guided photothermal therapy in the second near-infrared window.Biomaterials. 2019https://www.sciencedirect.com/science/article/pii/S014296121930818X3. 用于近紅外II光觸發的有機半導體聚合物兩親物丨Biomaterials開發具有高光熱穩定性、高光熱轉換效率(PCE)和良好生物相容性的近紅外II (NIR-II)光響應性納米制劑對光聲成像引導的光熱療法(PTT)具有重要意義��。盡管有機半導體聚合物納米粒子(OSPNs)在PA成像引導的PTT中具有優勢�����,但常用的基于納米沉淀法或再沉淀法制備的OSPNs在第一近紅外(NIR-I)窗口的有限吸收和亞穩態納米結構影響了其在體內的光熱性能��。在此,香港中文大學邊黎明研究團隊聯合香港城市大學李振聲和Wang Lidai研究團隊設計并合成了一種新型的近紅外吸收有機半導體聚合物兩親物(OSPA),以增強OSPNs的結構穩定性。OSPA具有顯著的光學性質�、低毒性和合適的尺寸�����,不僅可以有效地標記和殺死近紅外-II照射下的癌細胞,而且在靜脈注射時也能在活體小鼠的腫瘤組織中蓄積���,使得高效的近紅外-II光觸發光療可以針對腫瘤進行治療。綜上所述,本研究開發的OSPA在制造多功能納米平臺以實現多模態治療方面具有廣闊的前景����。Chao Yin, Xiaozhen Li,GuohuaWen, et al. Organic semiconducting polymer amphiphile fornear-infrared-II light-triggered phototheranostics. Biomaterials, 2019.https://doi.org/10.1016/j.biomaterials.2019.1196844. 高性能全能光熱療法--單劑量注射和808 nm激光照射的NIR-II熒光成像引導線粒體靶向治療丨Biomaterials目前的光熱療法仍面臨各種障礙�,導致治療過程復雜����、時間延長,增加了不必要的副作用和對患者的全身毒性。在此基礎上�,南京郵電大學范曲立研究團隊聯合南京理工大學唐衛華研究團隊設計并制備了基于單組分有機分子的線粒體靶向光熱納米粒子�����。經單光束808nm激光照射后�����,獲得了在水中高達2.2%熒光量子產率的第二近紅外(NIR-II)熒光信號�����,可用于近紅外熒光成像����,有效定位腫瘤及實時監測治療過程���。此外�����,在808nm激光照射下���,該納米粒子還表現出極高的光熱轉換效率(39.6%)和單線態氧產量(2.3%����,幾乎是臨床近紅外染料吲哚菁綠的12倍)�,既能產生強熱,又能產生豐富的單線態氧,從而導致線粒體功能障礙和進一步的細胞凋亡。體外和體內研究均表明����,這種納米制劑具有顯著的腫瘤治療效果���,這是由808nm激光觸發的高性能NIR-II熒光成像引導線粒體靶向光療所致。值得注意的是����,在體內治療過程中僅需采用單劑量注射和808nm激光照射�。綜上所述�����,在這項工作中開發的光療納米顆粒將為癌癥治療開辟一個新維度�。Qi Wang, Jingzeng Xu,Renyong Geng, et al. High performance one-for-all phototheranostics: NIR-IIfluorescence imaging guided mitochondria-targeting phototherapy with asingle-dose injection and 808nmlaser irradiation. Biomaterials, 2019.https://doi.org/10.1016/j.biomaterials.2019.1196715. 結構異構化使明亮的NIR-II-AIEgen用于腦炎癥成像丨AFM近紅外第二窗口(NIR-II)缺少高量子產率(QY)的有機熒光團已成為生物成像領域的瓶頸��。近日�,香港科技大學唐本忠院士課題組與南開大學丁丹教授合作�,提出了一個簡單的策略來解決這個問題:基于聚集誘導發射的分子設計原理的結構異構化。結合主鏈畸變和轉子扭曲�,生成的NIR-II熒光團2TT-oC6B在1030nm處顯示出發射峰�����,在納米顆粒中顯示出11%的QY,是目前報道的最高值之一����?���?刂品肿幼C實扭曲的主鏈和扭曲的轉子在確定NIR-II熒光團的熒光性質方面起著同樣重要的作用����。為了使靶向能力達到深入定位的疾病,中性粒細胞(NEs)被用來穿透腦組織并在炎癥部位積聚�����。在此�����,研究人員發現攜帶2TT-oC6B納米顆粒的NEs可以穿透血腦屏障,并通過完整的頭皮和顱骨看到深層炎癥。值得注意的是,明亮的2TT-oC6B有助于顯著增強腦炎癥部位30.6的信號背景比�。Shunjie Liu, Chao Chen,Yuanyuan Li, et al. Constitutional Isomerization Enables Bright NIR‐II AIEgen for Brain‐Inflammation Imaging.Advanced Functional Materials, 2019.DOI:10.1002/adfm.201908125https://onlinelibrary.wiley.com/doi/full/10.1002/adfm.2019081256. 雙增強NIR-IIa熒光半導體聚合物點在小鼠顱骨腦成像中的應用丨AngewNIR-IIa區域(1300-1400 nm)的熒光探針由于減少了生物組織中的光子散射和自體熒光而顯著改善了成像效果����。然而�����,這一區域的有機熒光團在很大程度上未被開發���。在此�,南方科技大學吳長峰研究團隊通過雙重熒光增強機制開發了NIR-IIa聚合物點(Pdots)�。首先�,使用吩噻嗪的聚集誘導發射來減少聚合物在凝聚態的非輻射衰減途徑���。其次��,通過不同水平的空間位阻使熒光猝滅最小化����,以進一步增強熒光�����。所得的Pdots在水溶液中的熒光QY約為1.7%��,與原始聚合物在四氫呋喃(THF)溶液中的熒光QY相比增強了約21倍。用NIR-IIa Pdots進行的小動物成像在穿透深度和信噪比方面也表現出顯著改善���,已通過活體小鼠腦血管的頭顱和頭皮熒光成像證實了這一點����。這項研究表明,NIR-IIa Pdots在體內熒光成像方面具有廣闊的應用前景。Zhe Zhang, XiaofengFang, Zhihe Liu, et al. Semiconducting Polymer Dots with Dually Enhanced NIR‐IIa Fluorescence for Through‐Skull MouseBrain Imaging. Angew. Chem. Int. Ed., 2019.https://doi.org/10.1002/anie.201914397