

第一作者:Chunzhen Yang
通訊作者:Alexis Grimaud
通訊單位:法國國家科學研究院固體化學與能源實驗室
研究亮點:
1. 提出了一種陽離子插層策略,打破OER過渡金屬氧化物催化劑的活性和穩定性之間線性關系
2. 堿性電解質中的水合鉀離子被嵌入層狀α-Li1IrO3的晶體結構中,形成的水鈉錳礦相催化劑表現出高活性和高穩定性
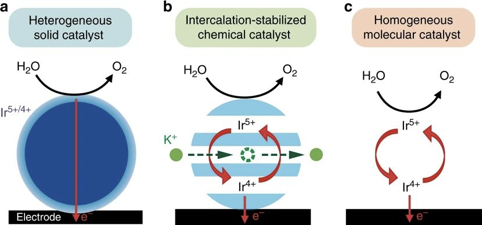
水的電荷補償化學氧化
OER催化劑制約著電解水技術的發展
可再生能源的廣泛利用要求研究人員設計開發性能更好的電化學存儲設備,如電解槽,需要在提高電解槽的性能的同時,盡量降低其成本,而實現這一目標的基礎是通過開發新的催化劑來改善電極處的電化學反應。然而,電極處的電化學反應相對比較復雜,涉及離子和電子在固體/液體界面的轉移。目前,在設計高效且無貴金屬的析氫反應催化劑方面已經取得了很大進展,但是另一半反應,即析氧反應(OER),進展較為緩慢。的確,在OER過程中伴隨著較大的動力學損失,對于迄今為止報道的性能最佳的催化劑,通常要獲得10 mA/cm-2的電流密度所需的過電位一般大于300 mV。
對高活性、高穩定性OER催化劑的迫切需求
過渡金屬氧化物是一種非常具有前景的OER電催化劑。最近的實驗結果和理論研究指出,增加過渡金屬-氧間的共價鍵會加快OER動力學,但會引起表面不穩定的問題。研究多種過渡金屬氧化物后發現,降低電荷轉移能會觸發氧配體的氧化還原活性,導致晶格氧按照所謂的晶格氧析出機理進入OER。這種參與降低了過渡金屬氧化物的配位,從而破壞了催化劑的表面穩定性。此外,當過渡金屬氧化物的導帶或費米能級在工作pH值下低于O2/H2O的氧化還原能級時,就產生了催化劑氧化水的驅動力。然而,由于缺乏電荷平衡機制,這種反應活性經常被動態陽離子溶解/再沉積過程和表面不穩定性所抵消。因此,當把催化劑的費米能級降低到水氧化的可逆電位以下,就會增加催化劑與水的反應活性,而這是以犧牲其長期穩定性為代價的。因此,同時提高OER催化劑的活性和穩定性仍是一項較大的挑戰。
有鑒于此,法國國家科學研究院固體化學與能源實驗室的Alexis Grimaud等人合作,提出了一種能夠同時提高OER過渡金屬氧化物催化劑的活性和穩定性的化學策略。制備的OER催化劑可以將費米能級降低到可逆水氧化電位以下。陽離子插層策略在增加催化劑活性的同時確保了高穩定性。
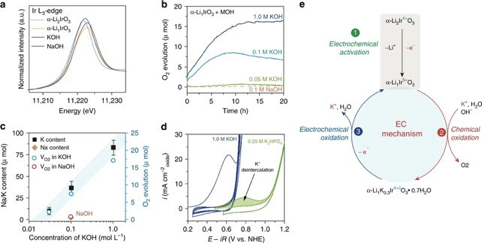
圖1 水鈉錳礦形成過程中水的化學氧化
要點1 為什么選擇α-Li2IrO3
他們選擇了具有開放二維晶體結構的過渡金屬層狀氧化物α-Li2IrO4,研究其電化學行為發現,當在有機溶劑中循環時,層狀的α-Li2IrO3化合物在~3.5 V和4.1 V處顯示出兩個連續的氧化反應,分別變為α-Li1IrO3和α-Li0.5IrO3。當在pH值為13的堿性溶液中使用α-Li2IrO3作為OER催化劑時,在第一個循環中,在~1.23 V(vs RHE)處觀察到不可逆的氧化峰,對應于α-Li1IrO3的形成。最初的氧化之后,在0.1 M KOH中觀察到較大的OER活性,在10 mA cm-2的下,過電勢低至290 mV。從這些數據可以看出,α-Li2IrO3是在堿性條件下報道的最具活性的晶體OER催化劑之一。
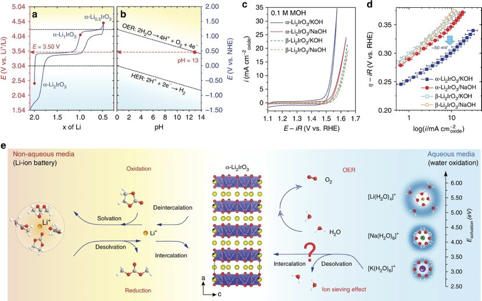
圖2. 電化學活性
要點2 K+插層活性相的發現過程
發現:在NaOH和KOH之間未觀察到電化學活性表面積或粒徑的顯著增加,這排除了增加活性位點以增強的OER性能的解釋,說明在OER電位下可能原位形成了一個新的活性相。
制備:通過結構轉變,對無水有機電解質中的α-Li1IrO3進行了電化學制備,然后使其與KOH反應,觀察到形成具有O3型層狀結構的新相,表明α-Li1IrO3與堿性溶液發生化學反應。研究發現,晶體結構(α-Li1IrO3)和堿性陽離子(K+)之間的相互作用對于觸發相變并增強催化劑的OER活性非常重要。
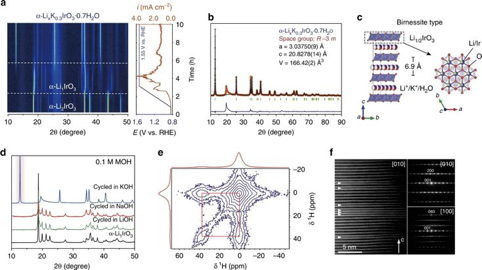
圖3 水合含K+水鈉錳礦相的表征
要點3 水氧化過程和析氧條件
水氧化過程:與KOH反應后,水和鉀會同時插入到氧化的α-Li1IrO3層狀化合物中,插入過程與堿性電解質的電荷轉移過程同時發生。與KOH溶液接觸時,α-Li1IrO3(即氧化劑)與作為還原劑的OH-的化學反應會自發生成氣態氧。KOH的濃度有兩個作用:首先,它增加了析氧的動力學;其次,由該化學反應產生的氣態氧的量與KOH濃度直接相關
析氧的條件:高濃度的OH-,具有較小流體動力學半徑和溶劑化能的堿性陽離子,以及開放的晶體學結構,這是插層鉀和還原α-Li1IrO3所必需的。
對照試驗:當用Na+進行類似的測量時,未測量到OER活性增強。OER的動力學取決于K+的濃度,這是引發比層狀相具有更大活性的水鈉錳礦相重整所必需的。增加OH-的濃度主要會影響受質子傳遞限制區域的動力學,而增加K+的濃度會影響質子傳遞受限區域的動力學。
OER中間體的計算研究:電荷平衡機制和水鈉錳礦相的形成引起了OER中間體能量的變化,導致OER動力學發生變化。
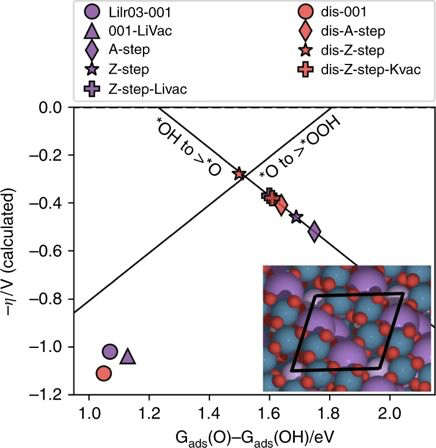
圖4 OER過電勢(η)與Gads(O)–Gads(OH)的函數
要點4 電化學和結構穩定性
結構穩定性:在KOH中經過300次循環后,催化劑的表面保持完美的結晶狀態,沒有形成無定形表面。因此,電荷平衡過程允許保持水鈉錳礦相的結構完整性。
性能穩定性:在0.1 M KOH中,電流密度為10 mA cm-2時氧化物在40 h內仍能保持OER性能。
因此,電荷平衡機制除了促進具有更高OER性能的水鈉錳礦相的形成之外,對于穩定銥基催化劑的結構和性能穩定也至關重要。
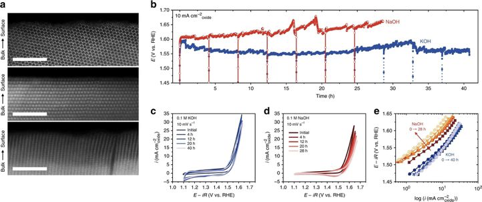
圖5 鉀嵌入過程中結構和OER性能穩定性表征
小結
總而言之,通過選擇開放的晶體學結構并結合使用具有較小流體動力學半徑的堿性陽離子,在催化劑與水發生化學反應期間將電解質嵌入層狀氧化銥的晶體學結構中,實現總體電荷平衡。形成的水鈉錳礦相表現出優異的OER性能,同時在長時間循環后仍保持完美穩定的結構和性能。因此,該工作不僅為先前對其他層狀化合物的研究提供了不同的認識,而且提出了一種打破OER催化劑的活性/穩定性之間線性關系的通用策略。
參考文獻:
Yang, C., Rousse, G., Louise Svane, K. et al. Cation insertion to break the activity/stability relationship for highly active oxygen evolution reaction catalyst. Nat. Commun., 11, 1378 (2020).
DOI:10.1038/s41467-020-15231-x
https://doi.org/10.1038/s41467-020-15231-x











