
第一作者:Suman Bose
通訊作者:Daniel G. Anderson
通訊單位:麻省理工學院,波士頓兒童醫院
以細胞為基礎的療法有可能徹底改變慢性疾病的治療方法,一些經過設計的細胞可以檢測病理狀況,同時作為活體工廠來生產和運送治療藥物。比如,在嚙齒動物模型中,含有合成基因回路的移植細胞可減輕過敏反應,治愈糖尿病和治療帕金森病;近期的干細胞技術也已經能夠無限制地產生功能性胰腺β細胞。然而,這些基于細胞的療法轉化到臨床的主要障礙是缺乏將這些細胞移植到患者體內的安全有效的技術手段。
移植的治療細胞會使得宿主產生免疫反應。細胞包載技術(圖1)作為一種允許細胞移植而無慢性免疫抑制的方法已經被廣泛研究。在這種免疫隔離體系內,移植的細胞受到膜的保護,膜的孔徑應設計為既能夠選擇性地阻斷有害的免疫成分,又能保證氧氣、營養物質和分泌的治療因子的輸送,這樣便可以既保持移植細胞的生物活性,又能使得被包載的細胞不被清除和受到免疫攻擊。最佳的細胞包載裝置還能夠對環境做出快速響應,例如響應血糖變化分泌胰島素等等。
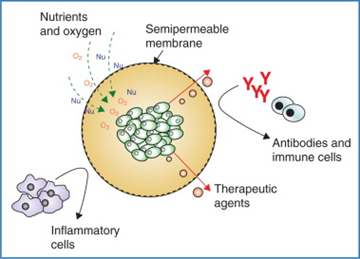
圖1. 細胞包載技術示意圖。自Principles of Regenerative Medicine
早些時候,研究人員就制備出一種用聚合物纖維加固的藻酸鹽凝膠,作為可回收的包載裝置。這些毫米級的裝置雖然具有高養分滲透性的優點,但是硬度的缺乏導致它們難以維持一定形態,此外還有移植體逸出的風險。由耐用的聚合物材料制備的裝置則可以克服這些限制,并在植入體的形狀和結構方面提供更大的靈活性。然而,它們在開發方面一直面臨著挑戰:一個是可以維持免疫屏障功能的膜孔徑的上限尚不清楚,另一個是植入體的異物反應可能導致纖維化和細胞分離。這其中,纖維化引起的缺氧仍然是細胞包載裝置的主要障礙。盡管現存的很多策略都在嘗試解決這些問題,但細胞維護和與外部環境接觸的要求限制了它們的臨床潛力。因此,開發出不會導致纖維化的細胞包載裝置尤為必要。
為了解決以上問題,麻省理工學院著名教授Daniel G. Anderson等人開發了一種生物相容性的細胞包載裝置,可以在生物體內長期遞送和維持治療細胞。研究人員依次改善了膜的特性和生物相容性,以提高裝置的性能。該膜具有一定的孔徑大小,以維持其細胞屏障功能。另外,研究人員還運用表面涂層修飾技術,將抗纖維化分子連接到裝置上,并證明了該表面涂層可以長期減輕纖維化反應。最后,研究人員證明了該裝置應用于包載人類細胞系和大鼠胰島的功效。相關研究成果發表在最近的Nature Biomedical Engineering上,題為“Aretrievable implant for the long-term encapsulation and survival of therapeuticxenogeneic cells.”
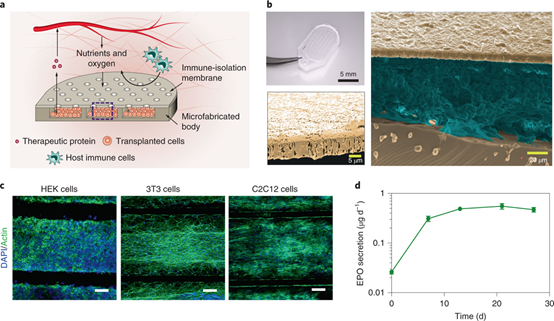
圖2. 可植入的細胞包載裝置概述及其體外實驗
研究亮點:
1. 該研究制備的細胞包載裝置,可以通過調節膜的孔徑大小來選擇性地調節免疫細胞的滲透。
2. 該裝置的生物相容性THPT表面涂層在防止纖維化和維持細胞活性和功能方面發揮極其重要的作用
要點1:細胞包載裝置的設計以及膜孔徑大小的確定
該細胞包載裝置包括一個附著在多孔聚合物薄膜上的細胞儲蓄池(圖2a)。它先由柔軟的硅彈性體(聚二甲基硅氧烷(PDMS))鑄成,再將聚碳酸酯化學結合到裝置上。組裝好的裝置通過進入端口裝載細胞,并使用紫外線固化型粘合劑密封。細胞儲蓄池的深度為150μm(類似于毛細管之間的距離),可將細胞精確定位在靠近膜的位置,從而確保營養物的最佳擴散。而硅彈性體則可防止膜塌陷,并在設備裝載過程中幫助微腔均勻填充細胞。碳酸酯膜具有一定的機械強度,可以制成帶有不同尺寸和分布孔徑的薄膜。該設備很靈活,可以安全植入軟組織。
研究人員將這種裝置運用于多種細胞實驗,包括人類胚胎腎細胞(HEK293)、小鼠成纖維細胞(3T3)和成肌細胞(C2C12)(圖2b,c)。SEM和共聚焦成像顯示包載的細胞緊密堆積在細胞池內部,且存活性良好。由于植入的人類細胞可以在嚙齒動物中引起排異反應,因此研究人員又將HEK293T細胞轉化為可以分泌小鼠促紅細胞生成素(EPO)的HEKepo細胞,并包載于該裝置內,以測試其在具有免疫功能的小鼠中的實用性。EPO是一種驅動骨髓中紅細胞生成的激素,也是評估治療細胞活性的有用激素之一。研究人員將封裝在裝置中的HEKepo細胞培養4周,同時定期測量EPO的分泌率(圖2d)。在開始的兩周內,EPO分泌增加,隨后達到穩定狀態,每天穩定狀態速率為0.4-0.6μg,達到治療效果。
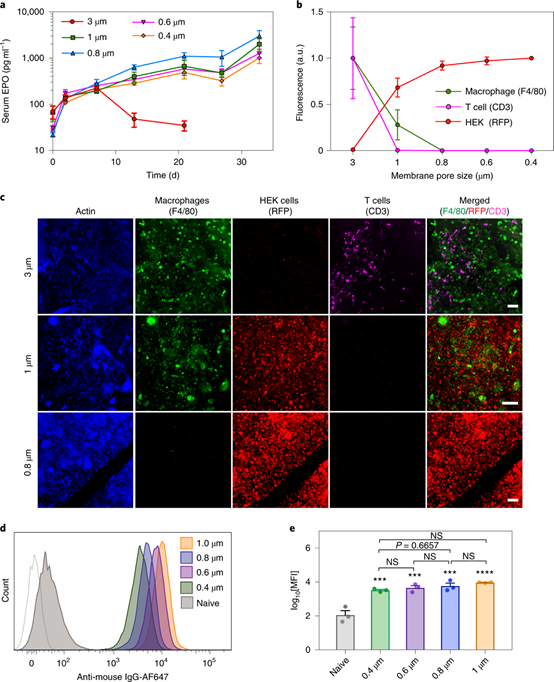
圖3. 膜孔徑調節免疫細胞滲透和異種移植體的存活
膜的孔徑大小是控制免疫隔離并最終影響裝置功能的關鍵參數,但可以維持免疫屏障功能的膜孔徑的上限尚不清楚。于是,研究人員使用具有3、1、0.8、0.6和0.4μm幾種不同孔徑的碳酸酯膜制造裝置,包載HEKepo細胞,并移植到具有免疫功能的BALB / c小鼠腹膜腔內,每周監測血清中的EPO濃度。結果表明,在移植后2 天,所有動物的血清EPO水平均翻了一番以上,并在第一周持續增加(圖3a)。這說明這些裝置在體內發揮了良好的功能,可以使被包載的細胞存活和生長,并成功遞送了EPO。持續觀察結果顯示,孔徑為3μm的裝置在一周后出現故障,這是因為這么大的孔徑導致大量巨噬細胞和T細胞的滲入,并完全喪失了移植體(圖3b,c)。相比之下,孔徑小于0.8μm的設備則沒有滲入免疫細胞,并且可以看到大量的HEKepo細胞聚集體。更有趣的是,孔徑為1μm的膜能阻止T細胞進入,但允許巨噬細胞滲入裝置內部,盡管與滲入的巨噬細胞直接接觸,但HEKepo細胞是完整的。這說明,可以通過調節膜的孔徑大小來選擇性地調節免疫細胞的滲透,孔的面積在1到1.25μm2之間,可以允許選擇性巨噬細胞的滲透但阻斷T細胞。
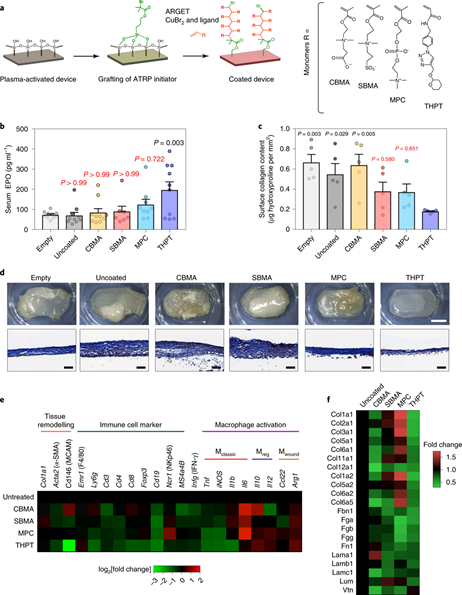
圖4 |減少異物反應
要點2:生物相容性THPT表面涂層發揮重要作用
植入裝置的生物相容性是影響體內功能的重要特征。為了減少移植體的異物反應,研究人員為裝置設計了一種具有生物相容性表面涂層。他們測試了幾種兩性離子聚合物涂層(圖4a),并最終用小分子四氫吡喃苯基三唑(THPT)充當抗纖維化涂層,與兩性離子聚合物接枝在裝置上。結果證明THPT涂層的功能性和滲透性良好:研究人員將空裝置與包載HEKepo細胞的有涂層和無涂層的裝置植入C57BL / 6小鼠體內,發現THPT涂層組在4周之內達到了最高的血清EPO水平(195.7pg ml -1),明顯高于未涂層的(69.84 pg ml -1)或空設備(72.3 pg ml-1)(圖4b)。研究人員測試了THPT涂層在體內環境下的長期穩定性,結果表明THPT涂層能夠在體內至少保留4周。
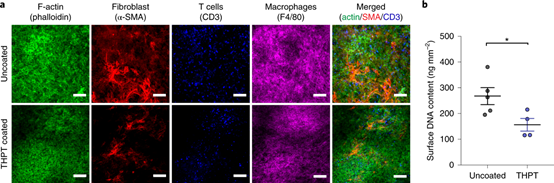
圖5 | THPT涂層可減少植入裝置上的細胞生長
接下來,研究人員又研究了THPT涂層如何提高被包載細胞的存活率,他們發現,在未涂層和兩性離子涂層的裝置上產生了中度至重度纖維化以及組織的過度生長,而用THPT涂層的裝置則很干凈,僅發現外圍薄薄的膠原蛋白(圖4c,d)。因此,THPT涂層具有最佳的抗纖維化作用,使得膠原堆積減少了70%(圖4c)。其他實驗也證實,THPT涂層會降低促炎性細胞因子的分泌(圖5a,b),并減少細胞向該裝置的聚集,最終導致纖維化反應的減輕。
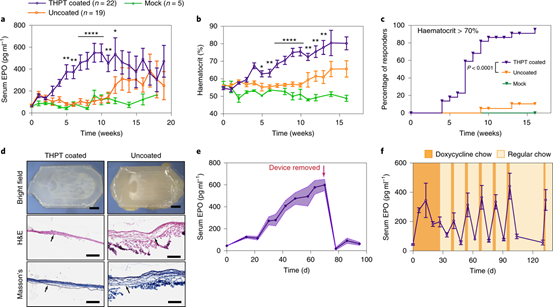
圖6 |植入小鼠腹腔內
研究人員將包載HEKepo細胞的有THPT涂層和無涂層的裝置植入C57BL / 6小鼠腹腔內,用沒有細胞的THPT涂層裝置作為對照,發現THPT組的血清EPO水平在最初的10周中穩定增加,并且一直保持較高水平(圖6a),說明THPT涂層裝置可以成功維持移植體的功能超過4個月。同時,THPT組的血細胞比容值明顯高于無涂層組(圖6b),表明THPT涂層設備的性能穩定。為了更好地評估裝置在維持高血紅細胞生成和治療貧血方面的功效,研究人員設定了將血細胞比容維持在超生理水平(> 70%)的治療目標,這只能通過持續遞送EPO 來實現。與無涂層組相比,THPT組顯示顯著改善的治療效果:到研究結束時,超過95%的動物達到了治療目的(圖6c)。在研究結束時(130 d)研究人員對裝置進行回收檢查,發現無涂層組已被嚴重纖維化,而THPT組仍保持相對干凈(圖6d),這表明THPT涂層可為纖維化提供持久的保護。
實驗完成后,研究人員用手術取出裝置。涂有THPT的裝置可以很容易地找到并安全取回,且在回收的裝置中細胞仍然存活和增殖。相反,無涂層的裝置對內臟器官廣泛粘附,并不容易安全移除。去除THPT涂層之后血清EPO急劇下降,并在1周內恢復到術前水平(圖6e)。
以上這些數據都表明,THPT涂層對于包載移植體的功能和存活都至關重要。
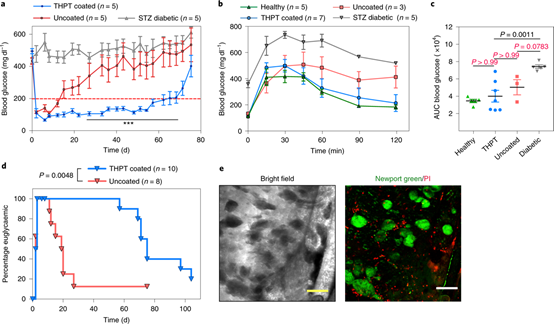
圖7 | 包載大鼠胰島并移植到糖尿病小鼠體內
要點3 此細胞包載裝置成功應用于人類細胞和大鼠胰島
研究人員將此新開發的裝置應用于包載幾種常用細胞。首先,他們將能夠被強力霉素誘導的HEKepo細胞包載在有THPT涂層的裝置內,移植到C57BL / 6小鼠腹腔中,并保留130 天。結果顯示移植體中的細胞始終對強力霉素有響應,表明被包載的細胞能夠保持長期穩定的活性,并且可長期調節性遞送治療性蛋白質。
其次,研究人員又將從Sprague–Dawley大鼠中分離出的胰島包載在有THPT涂層和無涂層的裝置中,經過處理后移植到鏈脲佐菌素(STZ)誘導的糖尿病C57BL / 6小鼠腹腔中,并測量血糖以監測胰島功能。結果表明,THPT涂層組維持正常血糖的時間明顯延長。THPT組動物的血糖水平和治愈分數明顯好于接受無涂層組(圖7a,d)。而且,THPT組顯示出與健康動物相似的出色的血糖分布(圖7b,c),而無涂層的設備的血糖分布較差,在研究的120分鐘內未達到正常血糖。
小結
綜上所述,該研究制備了一種可取出的具有多孔聚合物膜的植入體,作為異種細胞包載裝置,通過調節膜的孔徑大小可以選擇性調節免疫細胞的滲透。生物相容性的THPT涂層可有效防止纖維化,對于裝置的長期功能和細胞存活而言十分重要。長期體內實驗結果表明,該裝置可以包載轉基因的人類細胞和大鼠胰島,并發揮良好功效。這種生物相容性裝置的研究方案為多種醫療設備,例如導管、乳房植入物、傳感器和藥物輸送裝置等方面的應用提供了可能性。
參考文獻:
Bose, S., Volpatti, L.R., Thiono, D. et al. Aretrievable implant for the long-term encapsulation and survival of therapeuticxenogeneic cells. Nat. Biomed. Eng. 2020.
https://doi.org/10.1038/s41551-020-0538-5
作者簡介

通訊作者:Daniel G. Anderson, 納米治療和生物材料領域的領先研究人員,麻省理工學院著名教授。他于加州大學圣克魯斯分校獲得數學和生物學學士學位,并于加州大學戴維斯分校獲得分子遺傳學博士學位。他的研究專注于開發新的醫學材料和智能生物材料,其工作帶動了許多領域的進步,包括醫療設備、細胞療法、藥物遞送、基因療法和材料科學,至今發表了400多篇論文和專利。這些研究工作的產品已經商業化或正在進行臨床研發,為制藥、生物技術和消費產品領域的公司奠定了基礎。同時,他還是Living Proof,Olivo Labs,Crispr Therapeutics(CRSP),Sigilon Therapeutics,Verseau Therapeutics和VasoRx等公司的創始人。











