目前,肥胖在全世界呈流行趨勢,肥胖不僅會影響體型形象,對人類身體、心理健康同樣有不可忽視的影響。肥胖是指體重明顯超重和皮下脂肪層過厚,是體內脂肪積累過多而導致的一種不健康的狀態。有關肥胖的定義,比較普遍的認為肥胖是一種常見的、明顯的、復雜的代謝失調癥,是一種可以影響整個有機體正常功能的生理過程。有關研究已查明許多疾病與肥胖有關。比如,Ⅱ型糖尿病、心血管病、骨關節病、高血壓、免疫功能受損、癌癥等。隨著體重增加,患病的概率也在上升。肥胖研究正得到越來越多的關注,在此,奇物論編輯部收集了部分關于肥胖的研究成果,供大家學習交流。(PS: 馬上就要回學校了,還是趕緊減減身上的肉(我知道大家都有的),跟對象、同學、導師見面時,讓他們知道你在家是有學習的!而且跟他們說你每天都在關注奇物論最新前沿!!)
1.Nature Commun.: 無線光遺傳學可通過刺激非典型脂肪的生熱作用來預防肥胖 冷刺激和隨后激活的β-腎上腺素能受體(β-AR)會有效刺激脂肪組織的生熱作用并增加全身能量消耗,β3-AR激動劑作為一種能刺激脂肪組織產熱的減肥藥物,已經得到了廣泛的研究。但是,β3-AR途徑的全身激活不可避免地會增加血壓,這是心血管疾病的重要危險因素,因此限制了其在肥胖癥治療中的應用。為了在不受外部刺激的嚴格時空控制下激活脂肪生熱,于此,加州大學舊金山分校Shingo Kajimura和斯坦福大學Ada S. Y. Poon等人報道了一種可植入的無線光遺傳學設備,該設備繞過β-AR途徑并選擇性觸發脂肪細胞中的Ca2+循環。1)皮下脂肪組織中的無線光遺傳學刺激有效地激活了Ca2+循環脂肪的生熱作用,并增加了人體的能量消耗,而沒有冷刺激。2)明顯地,光誘導的脂肪生熱足以保護小鼠免受飲食誘導的體重增加。本研究提供了第一個概念證明,即通過激活非典型的生熱作用,脂肪特異性的冷模擬可以預防肥胖。
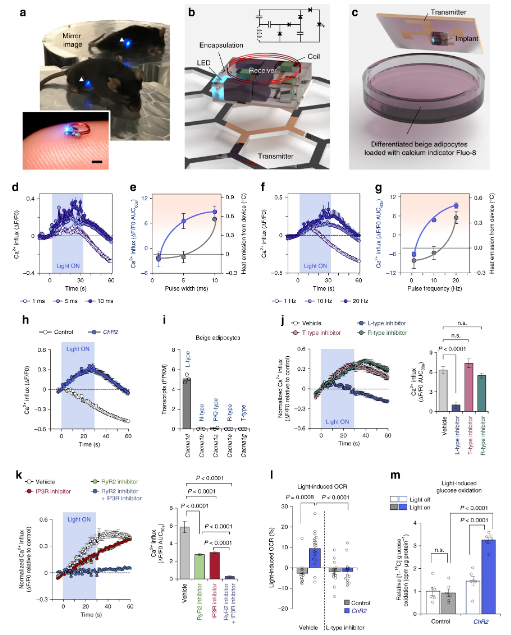
Tajima,K., et al. Wireless optogenetics protects against obesity via stimulation ofnon-canonical fat thermogenesis. Nat Commun 11, 1730 (2020).
https://doi.org/10.1038/s41467-020-15589-y2.Nature Commun.:植入自動力的迷走神經刺激裝置用于控制體重刺激體內迷走神經在調節食物攝入量和治療肥胖癥方面具有重要的應用前景。Yao等人展示了一個可植入的迷走神經刺激系統,它無需電池的并可以對胃的運動產生自發的反應。該迷走神經刺激系統由附著在胃表面的柔性生物納米發生器組成,它可以產生兩相電脈沖來響應胃的蠕動。該裝置產生的電信號可以刺激迷走神經傳入纖維來實現減少進食和控制體重的目的。這一策略在大鼠模型上得到了成功的驗證。在100天內,大鼠的平均體重被控制在350克左右,比空白對照組低了38%。這項工作通過一個智能化自動力的系統將神經刺激與器官功能聯系起來,并實現了高度有效的體重控制。
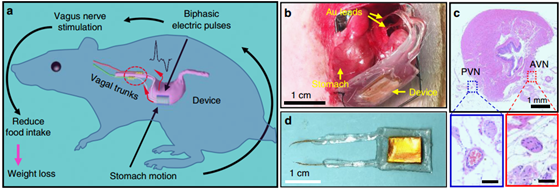
Yao,G., et al. Effective weight control via an implanted self-powered vagus nervestimulation device. Nature Communications, 2018
https://doi.org/10.1038/s41467-018-07764-z3.Nature:GDF15調節二甲雙胍對體重和能量平衡的影響二甲雙胍是世界上處方最廣泛的抗糖尿病藥物,也可有效預防高危人群中的2型糖尿病。60%以上的這種作用歸功于二甲雙胍持續降低體重的能力。二甲雙胍降低體重的分子機制尚不清楚。近日,英國劍橋大學Stephen O’Rahilly、Anthony P. Coll等研究人員,發現GDF15介導二甲雙胍對體重和能量平衡的影響。在兩項獨立的隨機對照臨床試驗中,研究人員發現二甲雙胍可提高GDF15的循環水平(最近發現GDF15通過腦干限制性受體來減少食物攝入并降低體重)。在野生型小鼠中,口服二甲雙胍可增加循環中的GDF15,而GDF15的表達主要在遠端腸和腎臟中增加。在野生型小鼠中,二甲雙胍阻止了對高脂飲食的體重增加,但在缺乏GDF15或其受體GFRAL的小鼠中卻沒有。在肥胖、高脂飲食的小鼠中,二甲雙胍減輕體重的作用被GFRAL拮抗劑抗體所逆轉。二甲雙胍對依賴GDF15的能量攝入和能量消耗都有影響。在沒有GDF15作用的情況下,二甲雙胍保持了降低循環葡萄糖水平的能力。總之,二甲雙胍可提高GDF15的循環水平,這對于其對能量平衡和體重的有益作用是必需的,而GDF15作為其化學預防劑的主要貢獻者。
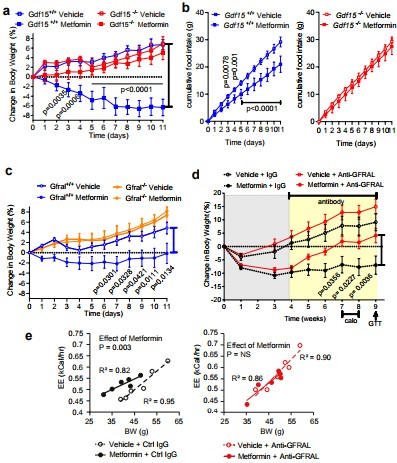
AnthonyP. Coll, Michael Chen, Pranali Taskar, et al. GDF15 mediates the effectsof metformin on body weight and energy balance. Nature, 2019.
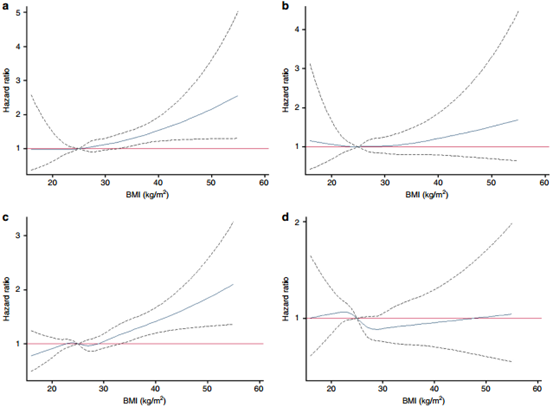
DOI: 10.1038/s41586-019-1911-yhttps://www.nature.com/articles/s41586-019-1911-y4. Nature Commun.:肥胖度比身體大小更能預測癌癥風險身體大小和體重分布二者誰會造成更大的癌癥風險目前還尚不清楚。Barberio等人研究了身體大小和形狀與患癌癥風險之間的關系。研究人群包括來自艾伯塔省明日項目的26,607名參與者。該實驗研究包括兩種主要的體型和大小測量方法:一是體重指數(BMI),二是腰圍(WC)。結果發現肥胖的男性和女性(BMI為30 kg / m-2)罹患全癌的風險比正常體重的女性分別高出33%和22,并且在性別特異性的WC結果中也觀察到類似的全癌風險的增加。這表明尤其是在女性中,中心型肥胖似乎比體型更能預測罹患癌癥的風險。Barberio,A.M., Alareeki, A. et al. Central body fatness is a stronger predictor ofcancer risk than overall body size. Nature Communications, 2019.https://doi.org/10.1038/s41467-018-08159-w5.Cell Metabolism:肥胖患者中谷氨酰胺促進炎癥發生雖然肥胖和相關的代謝并發癥與白色脂肪組織(WAT)炎癥有關,但其原因尚不清楚。近日,瑞典卡羅林斯卡醫學院MikaelRydén的研究小組,發現在肥胖患者中,谷氨酰胺與人類白色脂肪組織的炎癥有關。研究人員提出猜想:細胞所處代謝環境可能是導致肥胖的一個重要決定因素。為了驗證此猜想,研究人員比較了81名肥胖和非肥胖婦女白色脂肪組織(WAT)釋放的代謝物。研究發現谷氨酰胺在肥胖人群中下調并且與惡性WAT表型負相關。體內和體外實驗都表明,谷氨酰胺降低了脂肪細胞和WAT中促炎基因的轉錄和蛋白水平以及WAT中巨噬細胞的浸潤。人脂肪細胞的代謝組學和生物功能分析表明,谷氨酰胺減弱了糖酵解作用,降低了尿苷二磷酸N-乙酰葡糖胺(UDP-GlcNAc)的水平。UDP-GlcNAc是O-連接β-N-乙酰葡萄胺(O-GlcNAc)的翻譯后修飾的底物,O-GlcNAc轉移酶介導該反應。在人脂肪細胞中進行的功能性研究實驗將谷氨酰胺的減少、核蛋白的O-GlcNAcy化和促炎性轉錄反應聯系起來。該研究揭示了谷氨酰胺代謝與肥胖患者中WAT炎癥有關。3)高谷氨酰胺在體外可以減少人脂肪細胞的糖酵解和炎癥反應;4)核O-GlcNAc糖基化(O-GlcNAcylation) 將谷氨酰胺與脂肪組織炎癥聯系起來。
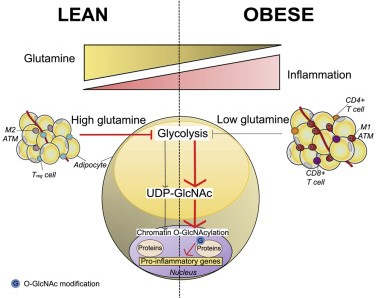
PaulPetrus, et al. Glutamine Links Obesity to Inflammation in Human WhiteAdipose Tissue. Cell Metabolism, 2019.DOI: 10.1016/j.cmet.2019.11.019https://www.cell.com/cell-metabolism/fulltext/S1550-4131(19)30663-16.Cell Metabolism:脂肪酸氧化對肥胖相關乳腺癌的影響盡管肥胖對癌癥的發展至關重要,但肥胖對抗腫瘤免疫反應的負面影響在很大程度上仍是未知的。近日,美國希望之城綜合癌癥中心Hua Yu、Saul Priceman、Chunyan Zhang的研究團隊合作,發現STAT3激活誘導的CD8陽性T效應細胞脂肪酸氧化對肥胖促進的乳腺癌生長至關重要。研究人員發現,由CD8陽性T效應細胞中激活的STAT3驅動的脂肪酸氧化(FAO)增加對于肥胖相關的乳腺癌進展至關重要。自發性乳腺癌的肥胖小鼠中的T細胞Stat敲除或用FAO抑制劑治療會降低FAO,增加糖酵解和CD8陽性T效應細胞功能,從而抑制乳腺癌的發展。此外,CD8陽性T細胞中的PD-1結合可激活STAT3以增加FAO,從而抑制CD8陽性T效應細胞的糖酵解和功能。最后,富含乳腺脂肪細胞和脂肪組織的瘦素通過激活STAT3-FAO和抑制糖酵解,下調CD8陽性T細胞效應子的功能。研究人員發現,由瘦素和PD-1通過STAT3驅動的脂肪酸氧化增加在抑制CD8陽性T效應細胞糖酵解和促進肥胖相關的乳腺癌發生中起關鍵作用。

ChunyanZhang, et al. STAT3 Activation-Induced Fatty Acid Oxidation in CD8+ TEffector Cells Is Critical for Obesity-Promoted Breast Tumor Growth. CellMetabolism, 2019.DOI: 10.1016/j.cmet.2019.10.013https://www.cell.com/cell-metabolism/fulltext/S1550-4131(19)30604-77.Nature Med.:MRAP2基因突變與貪吃型肥胖有關G蛋白偶聯受體輔助蛋白MRAP2與嚙齒動物的能量控制有關,特別是黑素皮質素-4受體。盡管已在肥胖癥患者中報道過了一些MRAP2突變,但它們對肥胖的功能影響仍然難以捉摸。近日,法國里爾大學AmlieBonnefond、Philippe Froguel等研究人員合作,發現MRAP2功能缺失突變是伴隨高血糖和高血壓的貪吃型肥胖的病因。通過對9418名個體的MRAP2基因進行大規模測序,研究人員確定了23種罕見的雜合變異體,它們與成年人和兒童的肥胖風險增加有關。每個變體的功能評估表明,功能喪失的MRAP2變體對單基因性貪吃肥胖癥、高血糖癥和高血壓具有致病性。這與其他單基因產生的饑餓型肥胖形成了鮮明對比,包括黑色素皮質素4受體缺乏。MRAP2中功能喪失突變所產生的的多種代謝作用可能是由于的各種組織中(包括胰島在內)MRAP2調節的不同G蛋白偶聯受體的失效所致。
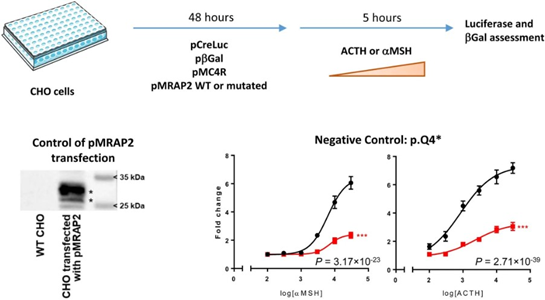
MorganeBaron, et al. Loss-of-function mutations in MRAP2 are pathogenic in hyperphagicobesity with hyperglycemia and hypertension. Nature Medicine, 2019.DOI: 10.1038/s41591-019-0622-0https://www.nature.com/articles/s41591-019-0622-0B類G蛋白偶聯受體是治療慢性疾病的主要靶點,包括糖尿病和肥胖癥。活性受體的結構揭示,肽激動劑深入受體核心,導致細胞外環3和跨膜螺旋6和7的頂端向外移動,跨膜螺旋1向內移動,細胞外環2重組和跨膜螺旋6細胞內側向外移動,導致G蛋白相互作用和激活。近日,澳大利亞莫納什大學Denise Wootten、Patrick M. Sexton和日本東京大學Radostin Danev等研究人員,解析了可與胰高血糖素樣肽1(GLP-1)受體結合的非肽激動劑TT-OAD2的結構。該結構揭示了一個未知的非肽激動劑結合口袋,其中細胞外環和跨膜螺旋的重組不依賴深跨膜結構域口袋中的直接配體相互作用。不同于肽激動劑,TT-OAD2表現出偏向激活作用類似于G蛋白活化動力學和信號傳導。在該結構內,TT-OAD2突出到受體核心之外,與脂質或去垢劑相互作用,可能為該類化合物臨床療效的獨特激活動力學提供了解釋。這項工作改變了人們對驅動B類受體激活機制的認知。
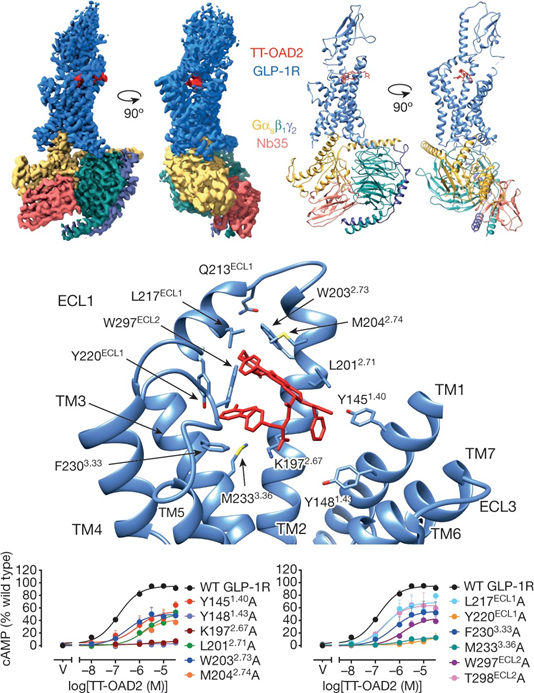
PeishenZhao, et al. Activation of the GLP-1 receptor by a non-peptidic agonist.Nature, 2020.DOI: 10.1038/s41586-019-1902-zhttps://www.nature.com/articles/s41586-019-1902-z9.Cell Metabolism:小鼠孤束核中的降鈣素受體神經元通過非厭惡性飲食抑制調控能量平衡為了了解控制食物攝入的后腦途徑,美國密歇根大學Martin G. Myers Jr.、英國劍橋大學Clemence Blouet等研究人員,研究了NTS中含降鈣素受體(CALCR)神經元的作用。NTS Calcr的敲除取消了CALCR激動劑對食物攝入的長期抑制,但并未消除厭惡反應。類似地,激活Calcr NTS神經元減少了食物攝入和體重,但是(不同于相鄰的Cck NTS細胞)未能促進厭惡,這表明Calcr NTS神經元介導了對食物攝入的非平均抑制。雖然Calcr NTS和Cck NTS神經元均通過投射到PBN減少了進食,但Cck NTS細胞激活了厭惡性CGRP PBN細胞,而Calcr NTS細胞則激活了獨特的非CGRP PBN細胞。因此,Calcr NTS細胞抑制了通過非厭惡性、非CGRP PBN靶標的攝食。此外,沉默Calcr NTS細胞可抑制腸肽和營養素對食物攝入的抑制,增加食物攝入并促進肥胖。因此,CalcrNTS神經元定義了一個后腦系統,其參與生理能量平衡并抑制食物攝入而無需激活厭惡系統。
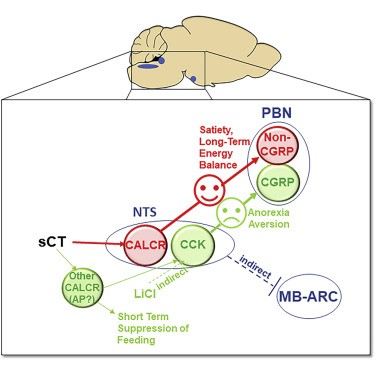
WenwenCheng, et al. Calcitonin Receptor Neurons in the Mouse Nucleus TractusSolitarius Control Energy Balance via the Non-aversive Suppression of Feeding.Cell Metabolism, 2020.DOI: 10.1016/j.cmet.2019.12.012https://www.cell.com/cell-metabolism/fulltext/S1550-4131(19)30677-110.Science Advances:利用干細胞分化為白色/米色脂肪細胞的胞外小泡進行細胞重編程干細胞來源的細胞外小泡(EVS)為再生醫學的干細胞治療提供了替代方法。有鑒于此,韓國漢陽大學的YongWoo Cho、韓國成均館大學的Dong-Gyu Jo等研究人員,將分化過程中產生的干細胞EV開發為通過誘導組織特異性分化而用作無細胞治療系統。1)人脂肪干細胞(HASCs)在向白色和米色成脂分化(分別為D-EV和BD-EV)過程中,通過切向流過濾分離出EV。D-EV和BD-EV分別能成功誘導HASCs分化為白色脂肪細胞和米色脂肪細胞。2)將D-EV與膠原/甲基纖維素水凝膠復合移植到BALB/c小鼠背部,在注射部位產生大量脂滴。BD-EV治療通過脂肪組織褐化減輕飲食誘導的小鼠肥胖。3)此外,BD-EV治療可改善高脂飲食誘導的肝臟脂肪變性和糖耐量。miRNAs負責觀察到的BD-EV效應。這些結果表明,在干細胞分化為白色脂肪細胞或米色脂肪細胞的過程中分泌的EVS可以促進細胞重編程。
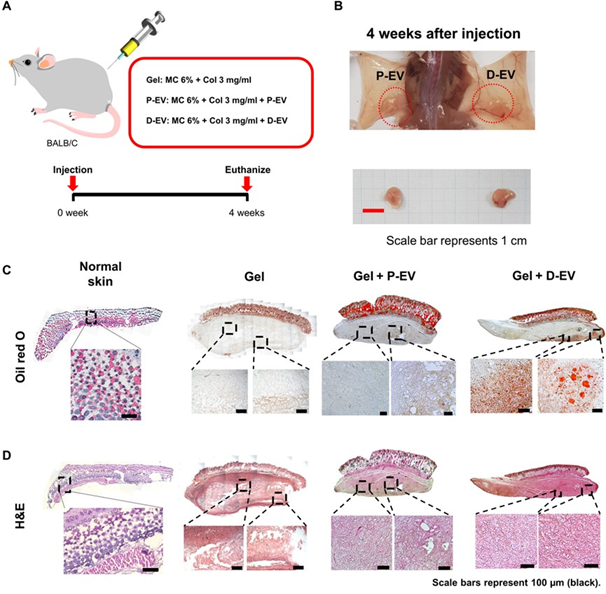
YounJae Jung, et al. Cell reprogramming using extracellular vesicles fromdifferentiating stem cells into white/beige adipocytes. Science Advances, 2020.DOI:10.1126/sciadv.aay6721https://advances.sciencemag.org/content/6/13/eaay6721?rss=111.Cell Metabolism:糖誘導的肥胖和胰島素抵抗與果蠅壽命縮短無關高糖飲食會導致口渴、肥胖和代謝異常,從而導致包括2型糖尿病在內疾病以及壽命縮短。然而,肥胖和水失衡對健康和生存的影響是復雜的。有鑒于此,英國MRC倫敦醫學科學研究所Helena M. Cochemé等研究人員,發現糖誘導的肥胖和胰島素抵抗與果蠅壽命縮短無關。1)高糖會導致果蠅成年期脫水,補充水分可以充分挽救它們的壽命。相反,代謝缺陷與水無關,這表明糖誘導的肥胖與體內胰島素抵抗(且壽命減少)之間無關。2)高糖飲食可促進尿酸(嘌呤分解代謝的最終產物)的積累,以及腎結石的形成,腎結石的形成會因脫水和生理酸化而加劇。重要的是,調節尿酸的產生以水依賴的方式影響壽命。3)此外,在人類隊列中的代謝組學分析表明,飲食中糖的攝入強烈地預測了嘌呤的循環水平。這一模型解釋了獨立于肥胖和胰島素抵抗的高糖飲食的病理生理學,并強調了嘌呤代謝是延長壽命的靶標。
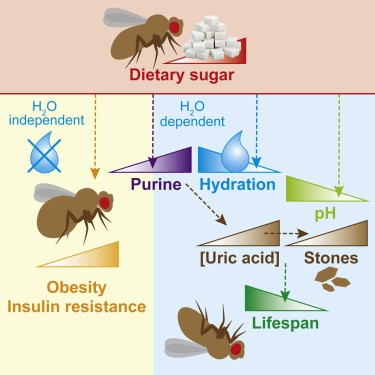
Esthervan Dam, et al. Sugar-Induced Obesity and Insulin Resistance Are Uncoupled fromShortened Survival in Drosophila. Cell Metabolism, 2020.DOI:10.1016/j.cmet.2020.02.016https://www.cell.com/cell-metabolism/fulltext/S1550-4131(20)30075-912. Nature Med.:肥胖對腫瘤發展和PD-1檢查點阻斷治療期間T細胞功能的影響免疫療法成功地改變了傳統的癌癥治療的模式。但是,由于只有百分之一的病人對免疫療法有好的反應,因此及時評估治療的結果是非常必要的。肥胖癥現在也十分流行,它被認為是造成某些惡性腫瘤的主要危險因素之一。而人們對于肥胖癥對免疫反應的影響以及在其癌癥免疫治療方面的作用知之甚少。Wang等人證明了在多個物種和腫瘤模型中,肥胖會導致免疫衰老、腫瘤發展和PD-1介導的T細胞功能障礙的增加。然而矛盾的是,肥胖也與PD-1/PD-L1阻斷治療在荷瘤小鼠和臨床癌癥患者中的療效增加有關。這些發現可以有助于人們增強對肥胖引起的免疫功能障礙及其對癌癥的影響的理解。這些數據表明肥胖對癌癥的影響是兩面的:會導致更高水平的免疫功能障礙和腫瘤發展;但也有更強的抗腫瘤療效產生。
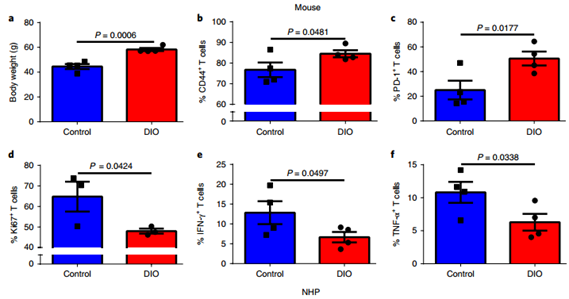
Wang,Z.M., et al. Paradoxical effects of obesity on T cell function during tumorprogression and PD-1checkpoint blockade. Nature Medicine, 2018.https://www.nature.com/articles/s41591-018-0221-5肥胖是胰腺導管腺癌(PDAC)的主要危險因素,但是,肥胖如何以及何時促進PDAC的進展尚不清楚。有鑒于此,美國耶魯大學醫學院的Mandar Deepak Muzumdar等研究人員,發現內分泌-外分泌信號促進肥胖相關的胰腺導管腺癌。1)利用原發小鼠模型,研究人員證明了肥胖在PDAC早期發展中具有因果關系和可逆作用,并表明肥胖顯著增強了腫瘤的發生,而遺傳或飲食誘導的減肥則阻止了癌癥的發展。2)人類和鼠樣品的分子分析確定了肥胖的微環境影響,即促進腫瘤發生,而不是產生新的驅動基因突變,這些影響包括與肥胖相關腫瘤中胰島細胞的顯著適應性。3)具體來說,研究人員確定了響應肥胖的肽激素膽囊收縮素(Cck)在β細胞中的異常表達,并表明胰島Cck促進致癌Kras驅動的胰腺導管腫瘤發生。該研究認為,PDAC的進展是由局部肥胖相關的腫瘤微環境變化驅動的,并且在PDAC的發展中提示了胰島素以外的內分泌-外分泌信號傳導。Katherine Minjee Chung, et al. Endocrine-Exocrine Signaling Drives Obesity-Associated Pancreatic Ductal Adenocarcinoma. Cell, 2020.DOI:10.1016/j.cell.2020.03.062https://www.cell.com/cell/fulltext/S0092-8674(20)30395-0