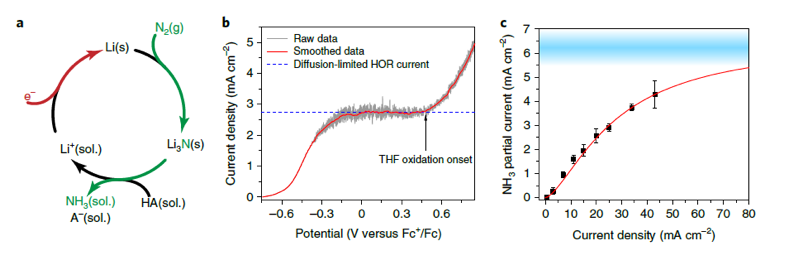
非水溶劑中的電化學轉化反應在合成及能量儲存領域均有重要應用��。受限于在非水溶劑中低的溶解度和擴散速率�����,非極性的氣體反應物,如N2���、H2等在非水溶劑中的反應效率較低。已知傳統的氣體擴散電極通過加強電極附近的氣-液接觸來增加氣體反應物在電解質中的擴散速率�。然而�,由于碳纖維載體(如碳布等)和非水電解質之間不存在疏水排斥作用�����,氣體擴散電極在非水溶劑中的應用受到極大阻礙�。
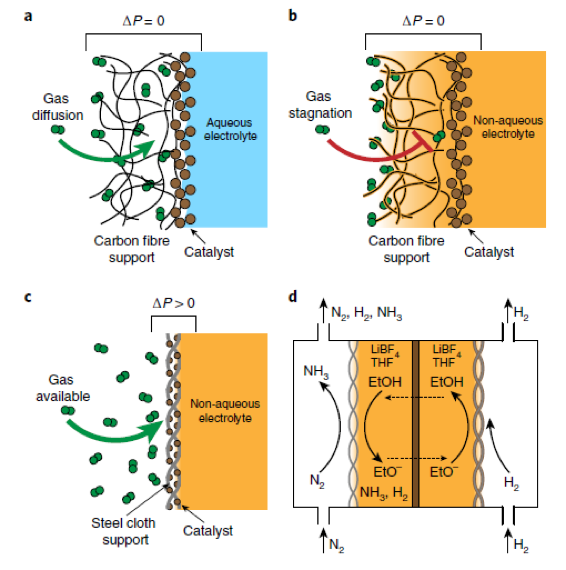
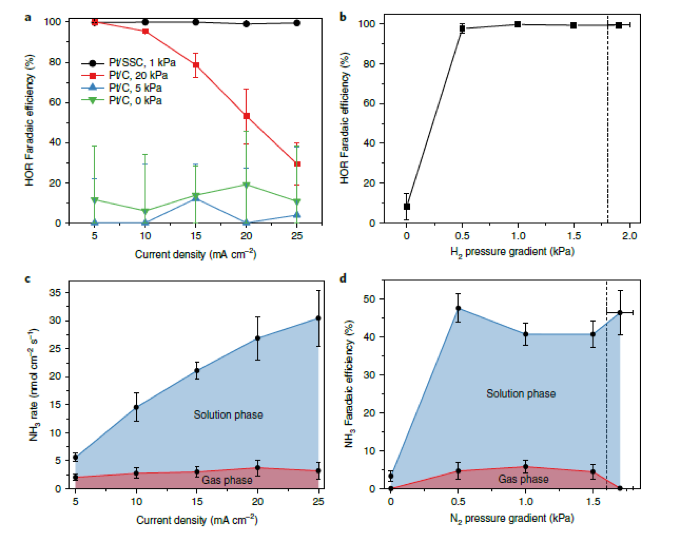
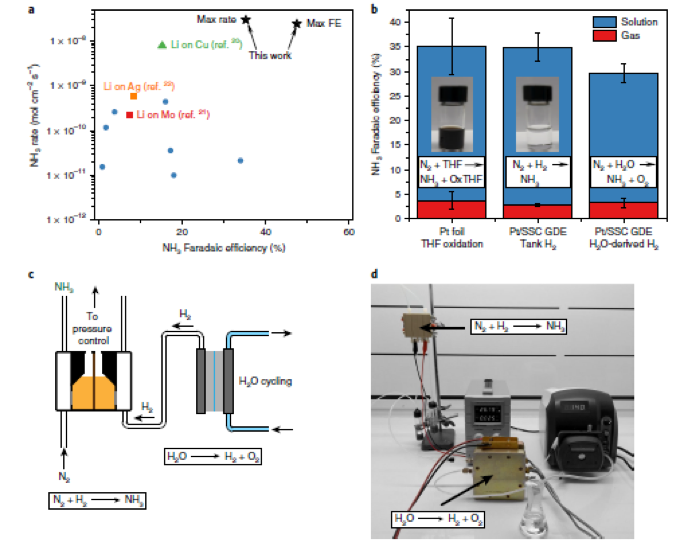
針對這一問題,近日���,美國麻省理工學院Karthish Manthiram教授在四氫呋喃電解液中,利用網狀不銹鋼基底克服了反應底物氣體擴散速率低的問題�,實現了伴隨H2氧化的固氮反應��。具體而言,作者構筑了Li介導的固氮體系��,固氮反應的電流密度高達8.8 ± 1.4 mA cm-2����,對應的法拉第效率為35 ± 6%。在兩種不同的非水溶劑電解質中,H2氧化反應的法拉第效率基本一致���,電流密度為25 mA cm-2。最后,作者將耦合了固氮反應體系和H2氧化反應體系,成功利用N2和電解水產生的H2合成NH3�。電化學合成較熱化學合成更具吸引力���,因為前者利用外加電壓跨越反應熱力學能壘,避免了高溫高壓的苛刻條件���,使得合成反應能在較為溫和的條件下進行。已知氮元素是生命體合成核酸�����、蛋白質等生物分子所必需的元素��,生命體的新陳代謝過程高度依賴于將N2轉化成NH3的固氮反應�。工業生產通常利用哈伯-博施法固氮���,其反應條件苛刻�,不僅需要高溫(300-500 °C)、高壓(200-300 bar)的環境�����,而且要以蒸汽重整產生的H2為反應原料��;會耗費大量的能源�,與生物固氮大相徑庭��。近年來�����,有研究者指出可通過水分解等反應提供H2,克服哈伯-博施法伴隨的高能耗問題���。然而,由于固氮需要高溫高壓的反應環境�,可以利用這些方法的固氮反應器依舊缺乏���。已知以N2和H2O為原料��,利用電化學方法合成氨理論上只需要1.17 V(vs. NHE)的電勢�����,不僅反應條件溫和���,而且有利于規?;磻?。盡管電化學反應在合成領域具有無可比擬的優勢,但是對電極通常需要消耗不可再生的反應底物,這極大地限制了其應用范圍����。具體而言����,還原反應在能量存儲和某些合成領域具有重要應用����,但是其對應的氧化反應通常是溶劑的氧化和陽極的消耗。對于水溶液體系而言,溶劑氧化是可行的���;但對于非水溶劑體系,有機溶劑的氧化和陽極的消耗會大幅降低反應的原子經濟性�����,使得反應難以持續進行。具體到N2還原����,已知Li介導的固氮反應產NH3速率快����,對應的法拉第效率高�����。如圖1a所示,在反應過程中,金屬Li與N2會在自然條件下自發反應生成氮化鋰�;氮化鋰則會進一步質子化產生NH3和鋰鹽�����;最后鋰鹽被還原至金屬Li完成整個催化循環反應。目前,該反應的可行性已得到諸多研究者的證實���。值得注意的是,盡管Li介導的固氮反應法拉第效率高��,但由于缺乏合適的反應體系���,連續的產氨過程尚未實現�����。連續產氨過程要求上述3個反應能同時發生�,一般而言�����,需要以溶解了Li鹽的THF為電解質�����,以乙醇為質子源;相應的陰極反應如圖1a所述,陽極反應則可能涉及THF的氧化����,還有待進一步研究���。總而言之����,溶劑(例如THF)的氧化分解是Li介導的固氮反應用于實際生產生活的最大阻礙���。理論上而言����,在陽極進行H2氧化反應以產生熱力學可控的質子可以避免上述問題��。此外�����,在采用犧牲陽極的電化學合成體系中,陽極附近的H2氧化反應是可持續的�����,能促進高附加值的目標化學品的持續合成���。不幸的是�����,在非水溶劑體系中��,H2的溶解度和擴散速率嚴重阻礙了其氧化速率(圖1b)����;類似的現象也見于非極性氣體N2的相關反應(圖1c中的固氮反應)����。圖1:(a)Li介導的固氮反應的反應機理��,(b, c)H2與N2的擴散速率對固氮反應的影響使用氣體擴散電極(GDEs)是解決該問題的一種行之有效的方法:反應氣體�����、電解質和催化劑會緊密接觸,最小化氣體分子需要擴散的距離(圖2a)�,進而使得反應氣體的擴散速率大幅提升��。截至目前,GDEs已被用于H2燃料電池��、CO/CO2還原等領域��。在上文提及的研究領域����,電解質通常是水溶液或含水的聚合物材料��,GDEs載體則通常經過疏水處理�,以防止電解質滲透并浸潤其纖維結構�����。如果電解質的主要成分是非水溶劑��,如THF,那么GDEs載體與電解質之間的疏水作用將會蕩然無存��,電解質會進入GDEs載體的纖維結構中湮沒催化劑(圖2b)��;如此一來�,反應氣體需要擴散的距離大幅增加��,反應的有效電流密度隨之降低�����。作者指出�,雖然當前的研究提出了一些解決上述問題的可能策略,但是在非水溶劑中利用GDEs增強氣-液接觸(反應氣體-電解質),進而提升電化學合成效率的相關研究還鮮有報道���。基于上述研究背景,作者計劃通過控制電極載體的疏水性與電解質的滲透效果來達到與GDEs類似的效果���。具體而言,作者將催化劑負載于網狀不銹鋼基底上;通過壓力差來調節電解液的滲透效果。作者首先將該體系用于H2氧化反應���,發現當以鍍Pt的網狀基底作陽極,以THF和碳酸亞丙酯為電解液,H2氧化反應的電流密度高達25 mA cm-2�����。隨后��,作者利用原位電鍍的方法向網狀基底上鍍Li���,并將其作為陽極用于電催化固氮反應��,最終固氮反應的電流密度高達8.8 ± 1.4 mA cm-2,對應的法拉第效率為35 ± 6%。最后作者還進一步將鍍Pt的電極和鍍Li的電極耦合起來�����,實現溫和條件下的固氮反應����。如圖3a所示,作者首先嘗試采用商品化的Pt/碳布電極(Pt/C)進行H2氧化。結果表明,當水溶液充當電解液時��,Pt/C具有優良的H2氧化性能�;一旦以THF溶液為電解液,H2氧化反應得到顯著抑制����。針對這一問題��,作者隨后通過改變壓力加速了H2的擴散,一定程度上提升了H2氧化反應的法拉第效率��。具體而言��,當壓力為20 ± 4kpa時�,H2能擴散通過Pt/C電極���,對應的H2氧化反應的電流密度為~12 mA cm-2�。已知Pt/碳布電極的纖維結構、碳布和非水溶劑電解液間的相互作用會使電極溺水,不利于氣體底物的高效反應��?��?紤]到金屬網不會因為毛細作用吸收電解液���,因此���,作者將鍍Pt的網狀不銹鋼電極(Pt/SSCs)用于H2氧化反應����。結果如圖3a所示,在THF溶液為電解液的反應體系中���,Pt/SSCs介導的H2氧化反應的法拉第效率接近100%。這一現象不能簡單歸因于電化學活性面積的影響�����,因為理論上而言Pt/C與Pt/SSCs都會被電解液浸沒�,電流密度都會服從一維傳輸。而Pt/SSCs打破了這一規律����,意味著在電極附近存在能促進氣體擴散的氣-液界面層。此外�,作者還測定了不同的壓力下Pt/SSCs介導的H2氧化反應的法拉第效率�����,發現法拉第效率基本都接近100%。值得一提的是��,當采用的最高的電流�����、最低的氣體流量時����,H2的單程轉化率高達80%�,遠高于工業生產中哈伯-博施法對應的H2的單程轉化率(25-35%)。為了說明Pt/SSCs的普適性��,作者還進一步以1M LiBF4的碳酸亞丙酯與碳酸二甲酯(9:1)的混合溶液為電解液�����,發現H2氧化反應對應的法拉第效率無明顯變化�,說明在非水溶劑中�,SSCs具有氣體擴散電極類似的性質。作者在以SSCs作為陽極成功克服H2氧化反應中H2擴散速率的限制后����,嘗試進一步將SSCs作為陰極用于N2還原反應����?���?紤]到N2在THF中的擴散速率有限(上文的圖1c)�,作者計劃通過增加流動來提升N2還原反應的速率。具體而言��,作者將鍍Li的SSCs作為氣體擴散電極��,克服N2擴散速率低的問題���。如圖3c所示����,作者發現在高電流下,N2還原反應的速率顯著高于圖1c中有擴散限制時(Pt/SSCs作陰極)的速率��,表明鍍Li的SSCs陰極可用于連續的固氮反應���。如圖3c所示���,在1 cm2的電極表面�����,經過290 s極化后���,NH3總產量為8.7 ± 1.4 μmol��,相應的電解液和捕集阱中的NH3濃度分別為4.5 ± 0.6 mM 以及 0.46 ± 0.22 mM。在長效實驗中,130 min共計產氨量達102 μmol�,相應的法拉第效率為18.9 %�����。此外,作者還觀察到經過2 min左右的誘導期后��,氨的產量隨著反應時間的延長而增加��,表明2 min后Li介導的固氮反應達到循環穩定狀態。為了證實NH3是經由N2還原途徑生成,作者進行了系列對照組實驗。具體而言�,當用Ar取代N2時���,無NH3生成����;當以14N2與15N2的混合氣體為反應氣體時�����,會得到等比例的同位素標記的NH3�。作者在氣相和液相中均檢測到了產生的NH3(圖3c, d)�����。此外���,作者還進一步發現當無壓力作用于SSCs時��,該反應體系會轉換至電極溺水狀態,N2還原效率會受到顯著抑制(圖3d)���。由上述實驗結果可知,作者分別將鍍Pt的SSCs與鍍Li的SSCs用作陽極和陰極�����,成功實現高效的H2氧化反應和N2還原反應���?��;诖?����,作者計劃進一步耦合上述兩種體系,實現溫和條件下的固氮反應��。如圖4b所示����,作者在陰極附近檢測到了大量的NH3生成。且隨著反應時間的延長��,該體系展示出Pt/SSCs陽極在THF溶液中進行H2氧化反應的優點:避免了THF溶劑的氧化。乙醇作為質子供體���,在陰極進行N2還原反應,自身轉化為乙醇鈉�����;生成的乙醇鈉后續會在陽極參與H2氧化反應����,重新得到乙醇,完成循環��。值得一提的是�����,雖然本文構筑的電化學固氮體系在規模上小于工業生產的哈伯-博施體系���;但是其反應條件更為溫和�,反應所需的H2經過電解H2O產生���,避免了蒸汽重整伴隨的高能耗問題���。通過耦合電化學固氮反應器和電解水反應器(圖4c, d)��,作者以N2、H2O及可再生的電能為原料�����,成功實現了溫和條件下的合成氨���;利用商業化的裝置實現了法拉第效率高達30 ± 2%的固氮反應���。電化學合成能利用外加電壓跨越反應熱力學能壘�����,避免了高溫高壓的苛刻條件��,使得合成反應能在較為溫和的條件下進行,受到了研究者的廣泛青睞�。此項工作中���,作者將催化劑負載于網狀不銹鋼基底上�,通過壓力差來調節電解液的滲透效果����。首先將該體系用于H2氧化反應,發現當以鍍Pt的網狀基底作陽極時���,H2氧化反應的電流密度高達25 mA cm-2。隨后�,利用原位電鍍的方法向網狀基底上鍍Li�,并將其作為陽極用于電催化固氮反應�,最終固氮反應的電流密度高達8.8 ± 1.4 mA cm-2��。最后作者進一步將鍍Pt的電極和鍍Li的電極耦合起來����,實現溫和條件下的固氮反應����。整個系統的體積足夠小,可以放置在實驗室的臺面上,可以通過將許多模塊連接在一起�,實現可持續的固氮反應����。但目前該反應的能源效率只有2%左右��,還有待進一步深入探究��。總而言之���,該體系不僅在合成氨領域有重要價值�����,而且在合成、儲能領域均有巨大潛力��。Nikifar Lazouski , et al. Non-aqueous gas diffusion electrodes for rapid ammonia synthesis from nitrogen and water-splitting-derived hydrogen. Nat. Catal., 2020.DOI:10.1038/s41929-020-0455-8https://www.nature.com/articles/s41929-020-0455-8