
納米顆粒通常通過全身注射來給藥,這使得它們暴露于血流的動態環境中。注射的納米顆粒在血液中以各種流速傳播,這些流速會引起不同的血管剪切速率。內皮細胞在這些血管中排列,在循環過程中攝取納米顆粒,但是這種相互作用在體內的流量依賴性卻很難表征。
有鑒于此,加拿大多倫多大學陳志和(Warren C. W. Chan)教授課題組開發了一種微流控系統來控制納米顆粒與內皮細胞相互作用時的流速,探索流速對“納米粒子-細胞”相互作用的影響。
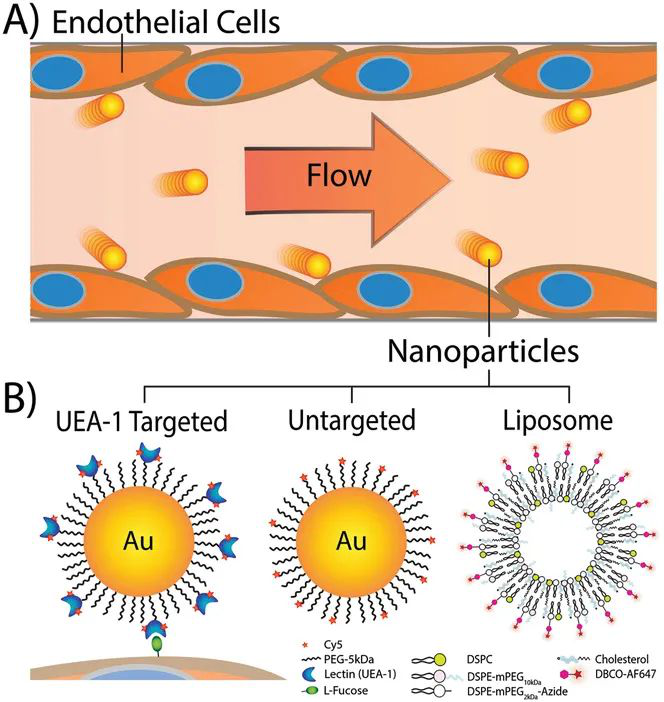
圖 | 流動下的納米顆粒-內皮細胞相互作用。
實驗裝置
首先我們來看看,作者是怎么控制流速的,如下圖所示,整個實驗裝置由蠕動泵(peristaltic pump)、微流芯片(Microfluidic chip)和培養液儲存器組成。使用微流體技術能夠控制流體流速和內皮細胞暴露于納米顆粒時所經歷的剪切應力。

裝置圖
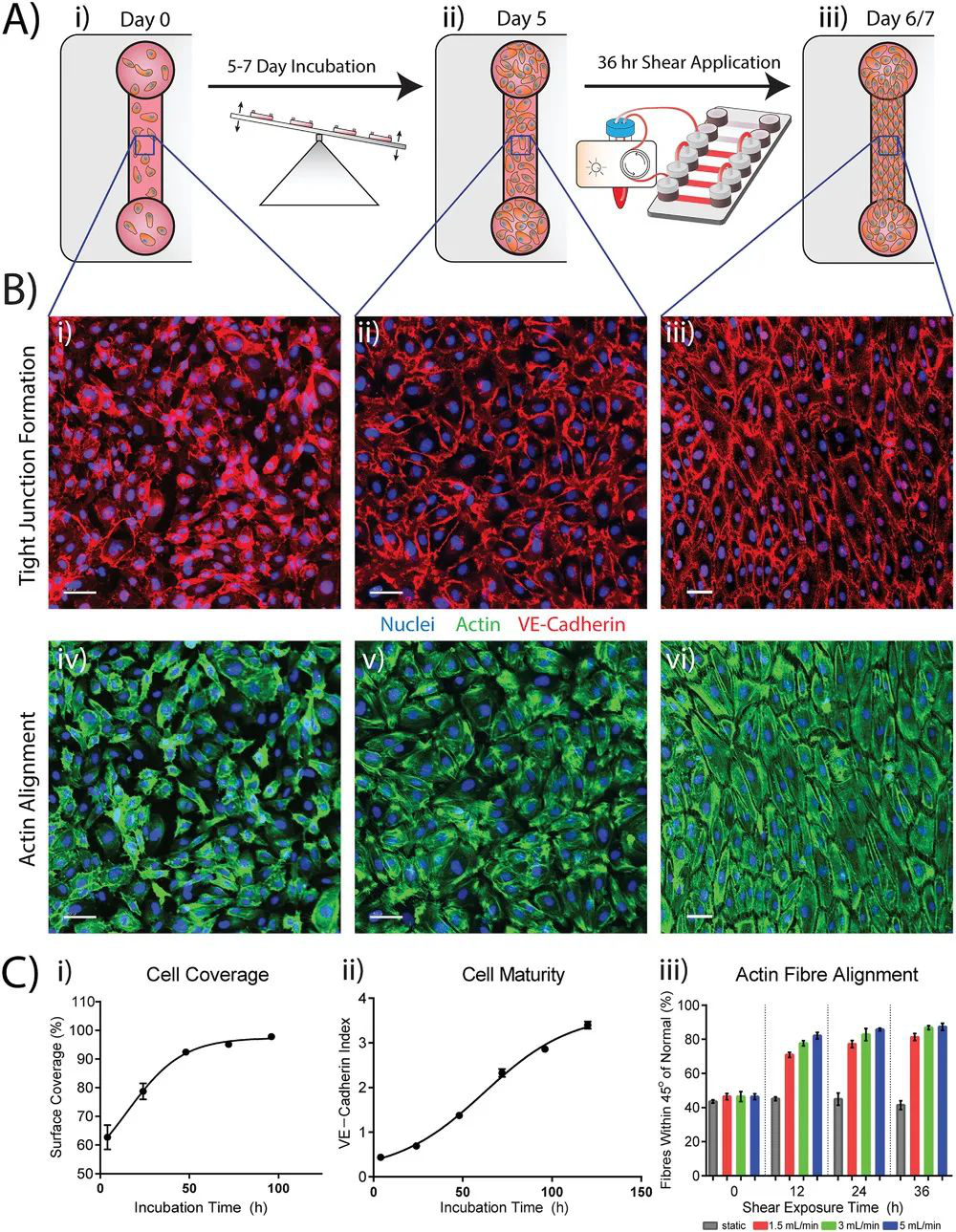
圖 | 內皮細胞裝置的制備
流速與細胞攝取成反比
研究人員將納米金顆粒在內皮細胞中的攝取以不同的流速進行定量,發現流速的增加會導致納米顆粒的攝取減少。內皮細胞對增加的流量剪切速率響應,使得吸收納米顆粒的能力降低。該平臺能夠顯示流速對細胞與納米顆粒之間相互作用的影響:流速與細胞攝取之間存在反比關系。
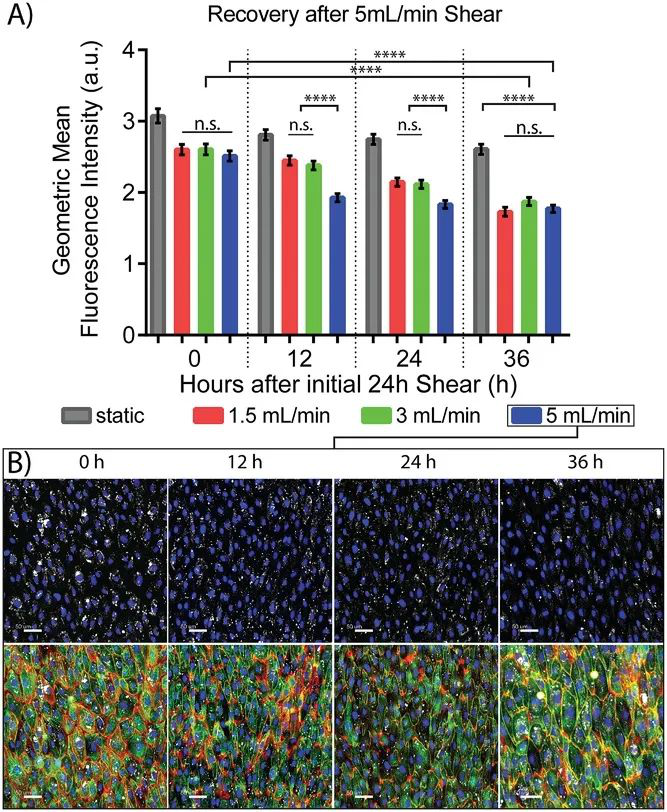
剪切力改變與細胞攝取
靶向化是否有影響?
研究人員還發現,使用靶向劑結合內皮細胞可以減輕血流速度的某些影響。用內皮細胞結合配體修飾納米顆粒表面可以將吸收部分地恢復到非流動水平,這表明功能化納米顆粒結合內皮細胞可以使納米顆粒抵抗流動效應。
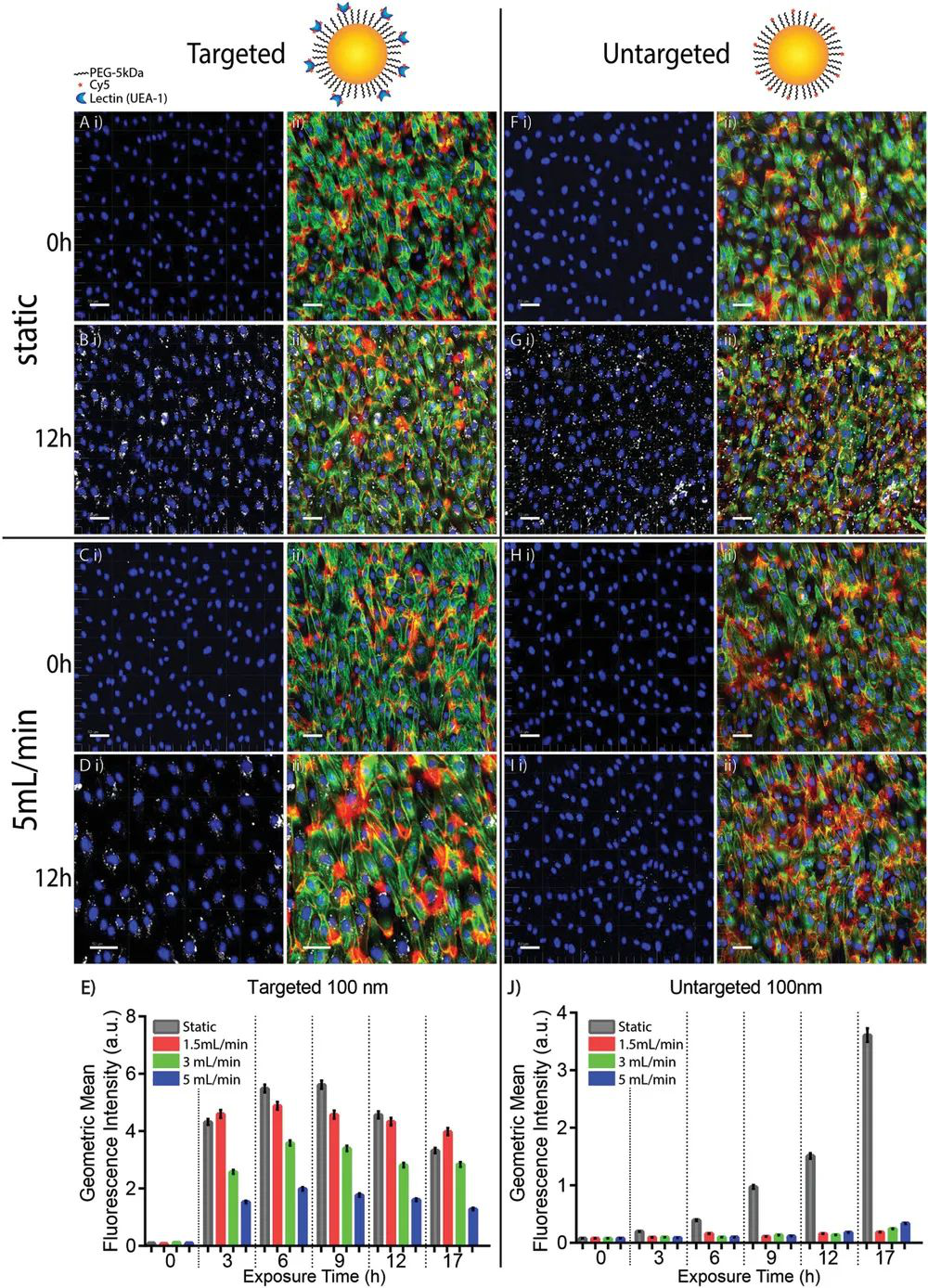
圖 | 納米顆粒流速的增加會減少攝取。
小結:
綜上,該項工作是第一代旨在探索流速對“納米粒子-細胞”相互作用影響的微流控系統,設計簡單。但體內的血管情況更為復雜,未來的微流體系統將需要包括更復雜的微流控結構來模仿這種曲折的脈管系統,需要開發這樣的裝置來對納米顆粒與生物系統之間的相互作用進行基礎研究。這些研究對于設計用于醫療應用的納米材料至關重要。
參考文獻:
Yih Yang Chen et al. Flow Rate Affects Nanoparticle Uptake into Endothelial Cells. Adv. Mater. 2020.
https://doi.org/10.1002/adma.201906274
關于陳志和教授的近期相關文章可參考:
1. Nature Materials:挑戰傳統! 臨床30年后,腫瘤納米給藥機制新發現!











