
曲曉剛,中科院長春應(yīng)化所研究員,博士生導(dǎo)師。國家杰青基金獲得者(2002),英國皇家化學(xué)會(huì)會(huì)士(FRSC),J. Mater. Chem. B副主編,J. Inorg. Biochem. 編委。
學(xué)習(xí)和工作經(jīng)歷:
1989-1995:中科院長春應(yīng)化所研究生、獲生物電化學(xué)專業(yè)博士學(xué)位,中科院院長獎(jiǎng)。師從董紹俊研究員(TWAS院士)和陸天虹研究員
1996-1999:美國Universily of Mississippi Medical Center, School of Medicine, J.B.Chaires教授
2000-2002:師從美國加州理工學(xué)院, NSF Laboratory for Molecular Sciences實(shí)驗(yàn)室主任諾貝爾獎(jiǎng)獲得者A H.Zewail教授
2006.12-2007.5:訪問美國UCSB諾貝爾獎(jiǎng)獲得者Alan J. Heeger教授實(shí)驗(yàn)室開展生物分子識(shí)別合作研究,部分結(jié)果已聯(lián)合發(fā)表
2002-至今:長春應(yīng)化所稀土資源利用國家重點(diǎn)實(shí)驗(yàn)室,化學(xué)生物學(xué)實(shí)驗(yàn)室研究員,英國皇家化學(xué)會(huì)會(huì)士(FRSC),J. Mater. Chem. B副主編,J Inorg. Biochem.編委,吉林大學(xué)生科院兼職博士生導(dǎo)師,中國化學(xué)會(huì)生物物理化學(xué)專業(yè)委員會(huì)副主任,化學(xué)生物學(xué)專業(yè)委員會(huì)委員,中國稀土學(xué)會(huì)理事,中國生物物理學(xué)會(huì)理事。
研究方向:
曲曉剛研究員主要研究領(lǐng)域?yàn)榛瘜W(xué)與生物學(xué)交叉,研究方向主要包括:(1)生物分子構(gòu)象與功能(研究具有重要功能核酸及蛋白的構(gòu)型轉(zhuǎn)化、多股核酸功能調(diào)控);(2)藥物與靶分子間作用機(jī)制(發(fā)現(xiàn)新的生物活性物質(zhì), 尋找它們?cè)谏矬w中的靶點(diǎn), 研究金屬配合物、有機(jī)化合物、中藥有效成分及納米材料與生物大分子之間的相互作用、構(gòu)效關(guān)系和作用機(jī)制, 進(jìn)一步在分子和化學(xué)鍵水平上研究它們?cè)谡{(diào)控生理過程中的分子識(shí)別、信息及能量傳遞);(3)生物體系電子傳遞、生物電化學(xué);(4)生物動(dòng)力學(xué)及熱力學(xué);(5)生物功能材料在抗癌、抗病毒及治療老年癡呆癥等重大疾病等。
主要研究成果:
共發(fā)表學(xué)術(shù)論文370余篇(IF>10論文120余篇),論文總引用超過2萬次以上,Physics News,ChemistryViews,Wliey Materials Views,ChemEuro,Nature China等對(duì)取得的多項(xiàng)成果給與40余次亮點(diǎn)報(bào)道和評(píng)論。2013年“中國百篇最具影響國際學(xué)術(shù)論文”,論文被Nature INDEX 2014評(píng)為WFC=16.3。科睿唯安2018及2017年全球高被引科學(xué)家;H-index 75。
以下,奇物論編輯部對(duì)曲曉剛研究員近期的部分研究成果進(jìn)行整理,供大家學(xué)習(xí)和交流!
1. ACS NANO:近紅外雙促進(jìn)非均相銅納米催化劑用于體內(nèi)高效生物正交化學(xué)

由于具有較好的穩(wěn)定性和生物安全性,非均相銅納米顆粒(CuNPs)作為Cu(I)催化的疊氮二烷基環(huán)加成(CuAAC)反應(yīng)的有力候選材料。但由于Cu(0)本身活性差,限制了其廣泛的生物應(yīng)用。中國科學(xué)院長春應(yīng)用化學(xué)研究所曲曉剛研究員團(tuán)隊(duì)利用生物相容性非均相銅納米催化劑在近紅外(NIR)照射下的的光動(dòng)力和光熱效應(yīng)對(duì)CuAAC反應(yīng)進(jìn)行了雙重促進(jìn)。
本文要點(diǎn):
(1)非均相銅納米催化劑在NIR照射下的光動(dòng)力學(xué)活性可以促進(jìn)Cu(0)向Cu(I)的轉(zhuǎn)化,加速CuAAC的催化過程。
(2)非均相銅納米催化劑在NIR照射下的較高的光熱轉(zhuǎn)換效率(η=50.6%)可以提高反應(yīng)的局部溫度,進(jìn)一步促進(jìn)整個(gè)反應(yīng)的進(jìn)行。
(3)從細(xì)胞實(shí)驗(yàn)到到線蟲的活體系統(tǒng)及小鼠體內(nèi)腫瘤治療實(shí)驗(yàn)發(fā)現(xiàn),在NIR照射下,熒光激活和藥物合成明顯加快。該研究為高催化性能和效率完成CuAAC反應(yīng)有很好的指導(dǎo)意義。
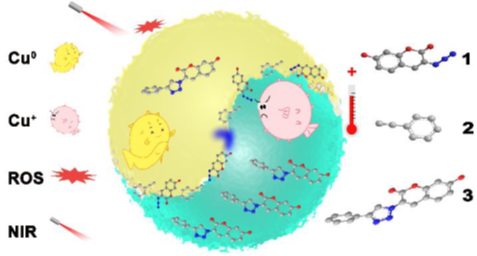
You, Y., et al., Near-InfraredLight Dual-Promoted Heterogeneous Copper Nanocatalyst for Highly EfficientBioorthogonal Chemistry In Vivo. ACS Nano. 2020;14(4):4178‐4187.
doi:10.1021/acsnano.9b08949.
https://dx.doi.org/10.1021/acsnano.9b08949
2. ACS central science:一種便攜式的可視化創(chuàng)可貼用于定點(diǎn)檢測和治療細(xì)菌感染

對(duì)于細(xì)菌感染和細(xì)菌耐藥性的前期監(jiān)測對(duì)于選擇治療方案非常重要。然而,常用的電阻傳感方法受時(shí)間、專業(yè)人員要求和昂貴儀器的限制。尤其是現(xiàn)在抗生素的濫用加速了細(xì)菌耐藥性的過程。中國科學(xué)院長春應(yīng)用化學(xué)研究所曲曉剛研究員團(tuán)隊(duì)構(gòu)建了一種便攜式紙基創(chuàng)可貼(PBA),該創(chuàng)可貼在檢測到耐藥性后,即可實(shí)施選擇性抗菌策略。
本文要點(diǎn):
(1)合成了一種卟啉基金屬有機(jī)骨架,在其內(nèi)部負(fù)載氨芐西林(抗生素,治療多種細(xì)菌感染),在其外部包裹殼聚糖,以吸引帶負(fù)電荷的細(xì)菌,實(shí)現(xiàn)酸敏感藥物釋放。
(2)溴麝香草酚藍(lán)(BTB)對(duì)感染部位的酸性環(huán)境有反應(yīng),顏色由綠色變?yōu)辄S色。因此將上述納米材料及BTB整合到纖維素紙中,制備出PBA。
(3)對(duì)于敏感性細(xì)菌(DS)引起的感染,PBA由綠色變?yōu)辄S色,并釋放抗生素以根除DS-E.coli(基于抗生素的化療)。
(4)對(duì)于耐藥性細(xì)菌(DR)引起的感染,PBA由黃色變?yōu)榧t色,并補(bǔ)充光照以消除耐藥性。與傳統(tǒng)的基于光動(dòng)力學(xué)療法(PDT)的抗菌策略相比,可以用肉眼實(shí)時(shí)跟蹤耐藥情況,減輕了靶外副作用(基于卟啉基金屬有機(jī)骨架的PDT療法)。
(5)PBA性能優(yōu)良、成本低、操作方便優(yōu)點(diǎn),可以開發(fā)出適合實(shí)際應(yīng)用的PBA。
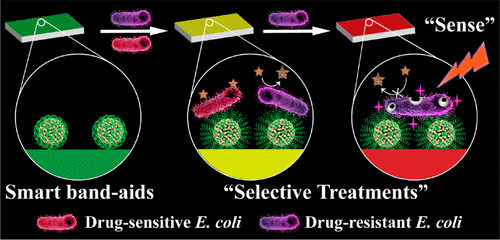
Sun, Y., et al., ColorimetricBand-aids for Point-of-Care Sensing and Treating Bacterial Infection. ACSCentral Science 2020, 6 (2), 207-212.
doi:10.1021/acscentsci.9b01104
https://doi.org/10.1021/acscentsci.9b01104
3. Chemical Science:斑塊處的銅催化點(diǎn)擊反應(yīng)合成雙功能藥物用于阿爾茨海默癥(AD)治療
銅是生命的基本元素之一。銅穩(wěn)態(tài)失衡與阿爾茨海默癥(AD)等神經(jīng)退行性疾病密切相關(guān)。對(duì)于銅聚積相關(guān)的疾病,最常見的治療方法是直接使用銅螯合劑。然而如何利用神經(jīng)毒性的銅對(duì)抗疾病,使其發(fā)揮作用,是一個(gè)巨大的挑戰(zhàn)。Cu(I)催化的疊氮二烷基環(huán)加成(CuAAC)反應(yīng)由于反應(yīng)效率高,動(dòng)力學(xué)快和條件溫和等特點(diǎn)近來在生物領(lǐng)域得到廣泛的應(yīng)用。但是生物體系中的CuAAC反應(yīng),一方面銅離子會(huì)通過芬頓反應(yīng)產(chǎn)生大量活性氧(ROS)。另一方面加入外源的銅催化劑會(huì)干擾生理環(huán)境中的銅穩(wěn)態(tài)。因此以內(nèi)源的銅離子為催化劑的點(diǎn)擊反應(yīng)具有特殊的吸引力。
阿爾茨海默癥(AD)與 β-淀粉樣蛋白(Aβ)的聚集和金屬穩(wěn)態(tài)失衡密切相關(guān)。Aβ 斑塊中銅的濃度可以達(dá)到 0.4 mM ,而正常大腦中的銅濃度僅為 0.2 -1.7 μM。最近的研究表明,天冬氨酸螯合的銅催化劑在低濃度下即可快速催化點(diǎn)擊反應(yīng)。中國科學(xué)院長春應(yīng)用化學(xué)研究所曲曉剛研究員團(tuán)隊(duì)發(fā)現(xiàn),Aβ斑塊中累積的銅能有效地催化疊氮化合物-炔烴生物正交環(huán)加成反應(yīng)。研究發(fā)現(xiàn)Aβ-Cu聚集體能在細(xì)胞、秀麗隱桿線蟲和三轉(zhuǎn)基因AD模型小鼠腦切片中,有效催化CuAAC反應(yīng)。
本文要點(diǎn):
(1)Aβ-Cu聚集體能在細(xì)胞、線蟲和腦切片中催化CuAAC反應(yīng)。
(2)通過Aβ-Cu聚集體催化的CuAAC反應(yīng),還可以原位合成雙功能藥物6。憑借光氧化Aβ和螯合銅的協(xié)同作用,雙功能藥物6能解離Aβ-Cu聚集體。
(3)雙功能藥物6能減少Aβ 斑塊、抑制Aβ誘導(dǎo)的線蟲癱瘓,并提高 CL2006線蟲的運(yùn)動(dòng)能力 。
(4)首次利用生理環(huán)境中局部的銅離子催化點(diǎn)擊反應(yīng),揭示了生物體系中內(nèi)源的金屬離子用于生物正交化學(xué)的潛力。為利用內(nèi)源性神經(jīng)毒性金屬離子原位合成多功能藥物治療神經(jīng)退行性疾病開辟了新的途徑。
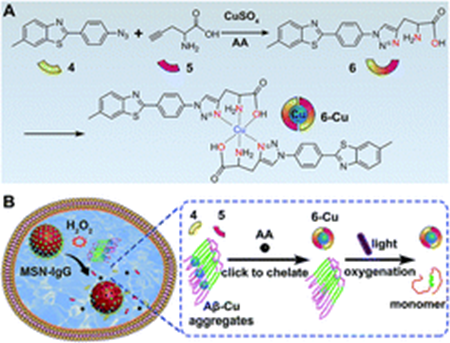
Du, Z., et al., Self-triggeredclick reaction in an Alzheimer's disease model: in situ bifunctional drugsynthesis catalyzed by neurotoxic copper accumulated in amyloid-β plaques. Chemical science 2019, 10 (44), 10343-10350.
doi:10.1039/c9sc04387j
4. JACS:基于H2O2穩(wěn)態(tài)干擾劑的仿生納米酶用于增強(qiáng)化學(xué)動(dòng)力學(xué)治療

瘤細(xì)胞內(nèi)過氧化氫(H2O2)水平不足與化學(xué)動(dòng)力療法(CDT)的有限療效密切相關(guān)。盡管付出了巨大的努力,但具有直接和安全的過氧化氫供應(yīng)能力的CDT試劑仍然是一個(gè)挑戰(zhàn)。研究發(fā)現(xiàn),腫瘤細(xì)胞內(nèi)H2O2的生成和清除具有一個(gè)平衡。中國科學(xué)院長春應(yīng)用化學(xué)研究所曲曉剛研究員團(tuán)隊(duì)構(gòu)建了基于H2O2穩(wěn)態(tài)干擾劑的仿生納米酶,通過促進(jìn)H2O2的產(chǎn)生和抑制H2O2的消除來提高細(xì)胞內(nèi)H2O2的水平用于增強(qiáng)化學(xué)動(dòng)力學(xué)治療效果。
本文要點(diǎn):
(1)在咪唑骨架-67(ZIF-67)上修飾小分子抑制劑3-氨基-1,2,4-三唑(3-AT)和聚乙二醇(PEG)得到H2O2穩(wěn)態(tài)干擾劑(PZIF67-AT)。
(2)PZIF67-AT具有超氧化物歧化酶(SOD)活性,可以將O2·-轉(zhuǎn)化為H2O2,促進(jìn)H2O2的生成。
(3)PZIF67-AT在弱酸性條件下可以釋放小分子,抑制其本身的過氧化氫酶(CAT)活性,從而減少了H2O2向H2O的轉(zhuǎn)化。還可以防止干擾物對(duì)過氧化氫的清除,無論是否加谷胱甘肽過氧化物酶(GPx)。
(4)促進(jìn)H2O2的產(chǎn)生和抑制H2O2的消除的精準(zhǔn)設(shè)計(jì)最終擾亂了過氧化氫的平衡,實(shí)現(xiàn)了癌細(xì)胞中過氧化氫的積累。
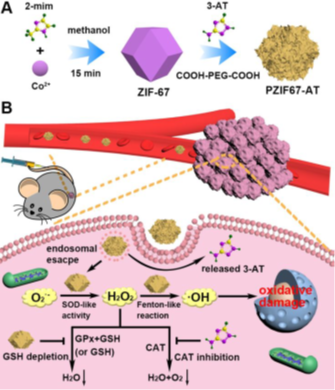
Sang, Y. , et al., BioinspiredConstruction of a Nanozyme-Based H2O2 Homeostasis Disruptor for IntensiveChemodynamic Therapy. Journal of the American Chemical Society,2020, 142 (11), 5177-5183.
DOI: 10.1021/jacs.9b12873
https://doi.org/10.1021/jacs.9b12873
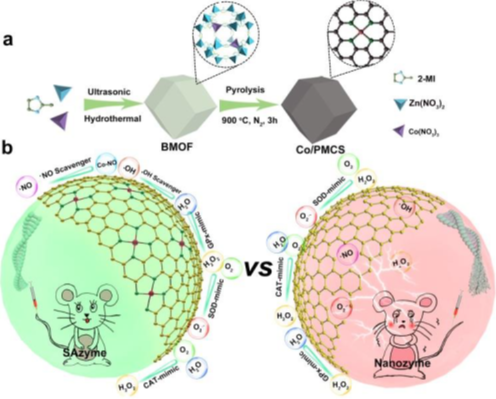
5. Angew: 單原子酶作為高效的多活性氧和氮清除劑在敗血癥治療中的應(yīng)用

敗血癥由于過度產(chǎn)生多種活性氧和活性氮,在世界范圍內(nèi)具有高發(fā)病率和高死亡率。盡管納米酶在敗血癥的治療方面取得了部分進(jìn)展,但由于開發(fā)的納米酶的特異性和活性比較低,因此能夠快速消除所有這些活性氧和活性氮的有效抗氧化療法仍然具有挑戰(zhàn)性。中國科學(xué)院長春應(yīng)用化學(xué)研究所曲曉剛研究員團(tuán)隊(duì)報(bào)道了一種新的單原子酶Co/PMCS,它具有原子分散的協(xié)同不飽和活性Co卟啉中心,能快速清除多種活性氧和活性氮,從而減輕敗血癥。
本文要點(diǎn):
(1)近來研究發(fā)現(xiàn)具有不飽和活性金屬中心的單原子催化劑具有更高的納米酶活性,因此制備了氮摻雜碳支撐原子分散的Co卟啉中心(Co/PMCS)作為多重抗氧化納米酶。
(2)Co/PMCS可以通過模擬超氧化物歧化酶(SOD)、過氧化氫酶(CAT)和谷胱甘肽過氧化物酶(GPx)等多種酶,有效地消除H2O2和O2-,同時(shí)通過氧化還原循環(huán)有效地降低?OH,表現(xiàn)出納米酶無法比擬的活性。
(3)研究發(fā)現(xiàn)?NO傾向于與金屬蛋白的未被占據(jù)的配位快速反應(yīng),形成金屬-硝基絡(luò)合物。受此啟發(fā),首次提出具有不飽和活性金屬中心的單原子催化劑通過形成亞硝基金屬絡(luò)合物可以有效清除?NO,目前的納米酶很難實(shí)現(xiàn)這一功能。
(4)在細(xì)胞水平和動(dòng)物水平可以降低促炎細(xì)胞因子水平,保護(hù)器官免受損傷,并賦予感染敗血癥小鼠明顯的生存優(yōu)勢,顯示了一種有前途的抗氧化治療劑。
Cao, F. , et al., AnEnzyme‐Mimicking Single‐Atom Catalyst as an Efficient Multiple Reactive Oxygenand Nitrogen Species Scavenger for Sepsis Management. Angewandte ChemieInternational Edition,2020, 132 (13), 5146-5153.
DOI: 10.1002/anie.201912182
https://doi.org/10.1002/ange.201912182











