
第一作者:魏妥,程強
通訊作者:Prof. Daniel J. Siegwart
通訊單位:美國德克薩斯大學西南醫學中心
CRISPR-Cas9作為一種強大的基因編輯工具,已被廣泛應用于生物醫學領域的各個方面。目前,遞送CRISPR-Cas9 核酸酶系統主要有三種方式:質粒遞送、Cas9mRNA/sgRNA共遞送和Cas9/sgRNA核糖核蛋白 (RNPs)遞送。由于低脫靶效應和低免疫原性的優勢, RNPs遞送越來越受到科學家們的青睞。然而RNPs具有分子量大、負電性強以及易失活等缺點,體內遞送極具挑戰。
奇物論曾報道過美國德克薩斯大學西南醫學中心Daniel J. Siegwart教授課題組發表于Nature Nanotechnology的“器官選擇性靶向(SORT)納米顆粒”,在mRNA遞送和CRISPR/Cas基因編輯的應用方面發揮巨大潛力。(深度解讀,附專訪)

近日,該課題組又乘勝追擊,通過對傳統脂質納米顆粒(LNPs)的簡單改造,成功解決了RNPs的體內遞送難題,并高效介導了體內器官選擇性的基因編輯(圖1)。相關研究成果發表于Nature Communications上,題為“Systemic nanoparticle delivery of CRISPR-Cas9 ribonucleoproteinsfor effective tissue specific genome editing”。

圖1 |脂質納米顆粒5A2-DOT-X LNPs體內靶器官遞送Cas9/sgRNA RNPs的策略。
研究亮點:
1.本文開發的脂質納米顆粒5A2-DOT LNPs可實現Cas9/sgRNA RNPs的體內靶器官遞送和高效基因編輯;
2.5A2-DOT LNPs可同時敲除多個基因位點,成功、快速地構建了器官特異性小鼠腫瘤模型;
3. 5A2-DOTLNPs可成功實現對小鼠疾病模型的基因編輯治療,對遺傳類疾病的治療具有廣泛的應用前景。
要點1: 5A2-DOT LNPs的開發過程
通常,LNPs包裹RNA的過程是在酸性緩沖液中完成。在酸性條件下,LNPs中的可電離陽離子脂質(ionizable cationic lipid)會帶上正電荷,從而完成對負電荷RNA的包裹。與RNA不同,Cas9/sgRNA RNPs在酸性條件下極易失去活性,而在中性條件下更穩定。因此,研究人員必須嘗試在中性緩沖液中包裹Cas9/sgRNA RNPs。可惜的是,可電離陽離子脂質在中性環境中并不會發生質子化,因此無法吸引帶負電荷的Cas9/sgRNA RNPs。基于前期積累的經驗,Daniel J. Siegwart教授課題組在LNPs原有的四種核心脂質的基礎上引入了第五種陽離子脂質(DOTAP),這樣不僅能增強其在中性條件下對Cas9/sgRNA RNPs的包載,而且保留了傳統LNPs的高效遞送能力。通過該策略,他們成功地將Cas9/sgRNA RNPs遞送到細胞內,基因編輯效率高達80%以上。
要點2:5A2-DOT LNPs可實現對 RNPs的體內靶器官遞送和高效基因編輯
研究人員發現,將包裹Cas9/sgTOMRNPs的5A2-DOT-10 LNPs局部注射到tdTOM模型小鼠的肌肉和腦部,可成功實現對小鼠肌肉細胞和腦細胞的基因編輯,激活tdTomato基因并使之表達紅色熒光。(圖2a-e)
基于該課題組前期開發的Selective ORgan Targeting (SORT)技術,研究人員在原有四種脂質組分比例(5A2-SC8 :DOPE: Chol : PEG = 15:15:30:3)的基礎上,通過調節DOTAP的摩爾比(5%-60%)制成了一系列包裹Cas9/sgTOM RNPs的5A2-DOT-X LNPs,并將其靜脈注射到tdTOM模型小鼠和C57BL/6小鼠中。研究發現,隨著DOTAP摩爾百分比的增加,基因編輯逐漸從小鼠肝臟轉移到肺部,且肺部基因編輯效果更高。此外,研究人員還發現在低劑量下(0.33 mg kg?1 sgRNA),5A2-DOT-50LNPs可高效遞送多達6種sgRNA到小鼠肺部,并成功對針對的6個基因位點進行基因敲除。(圖2f-j)

圖2 | Cas9/sgRNA RNPs的體內靶器官遞送和高效基因編輯。
要點3:5A2-DOT LNPs可快速構建器官特異性小鼠腫瘤模型
鑒于5A2-DOT LNPs可同時敲除多個基因位點,這對快速構建復雜的小鼠腫瘤模型具有極大的優勢。因此,研究人員通過肝靶向納米載體(5A2-DOT-5 LNPs)和肺靶向納米載體(5A2-DOT-50 LNPs)分別遞送多種不同的sgRNAs, 成功構建了小鼠肝癌模型和肺癌模型。該方法簡單、快捷,為新型小鼠腫瘤模型的建立提供了新的思路。
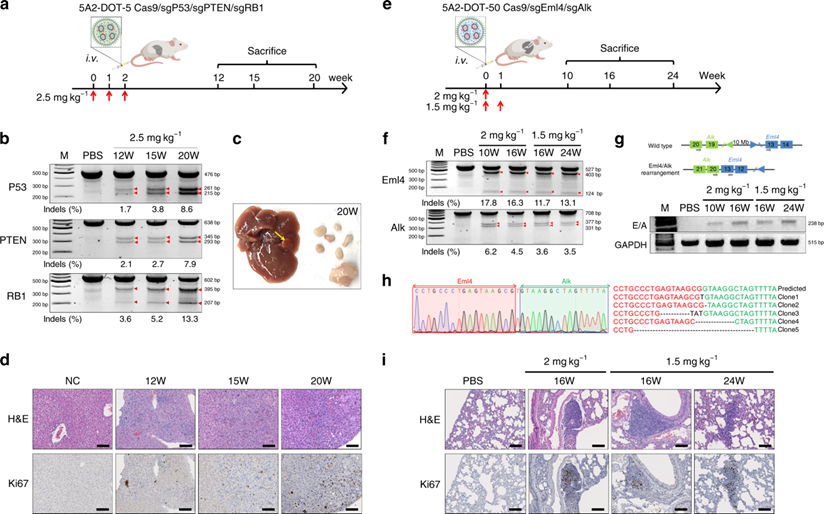
圖3 | 5A2-DOT LNPs可簡化小鼠肝癌模型和肺癌模型的構建。
要點4:5A2-DOTLNPs可成功實現對小鼠遺傳類疾病模型的基因編輯治療
研究人員進一步探索了5A2-DOT LNPs對小鼠遺傳類疾病模型的治療潛力。通過與德克薩斯大學西南醫學中心Eric N. Olson教授課題組合作,將包裹Cas9/sgDMD RNPs 的5A2-DOT-10 LNPs局部肌肉注射到杜氏肌營養不良癥模型小鼠(ΔEx44 DMDmice)中,可成功對模型鼠肌肉細胞中的突變基因進行基因編輯和修復,并成功恢復了dystrophin蛋白在肌肉中的表達。(圖4a-c)
接著,研究人員探索了肝靶向基因編輯的治療潛力,以PCSK9為研究靶點。靜脈注射5A2-DOT-5 Cas9/sgPCSK9 RNPs到小鼠體內后,成功在小鼠肝臟中檢測到PCSK9位點的基因編輯,且使小鼠血清中PCSK9蛋白的表達水平顯著降低。(圖4d-f)
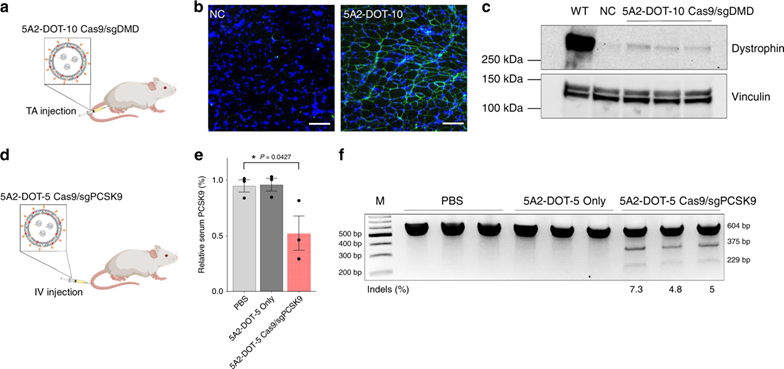
圖4 | 5A2-DOT LNPs可成功實現對小鼠遺傳類疾病模型的基因編輯治療。
小結:
本文提供了一種器官選擇性遞送RNPs的有效策略。在傳統脂質納米顆粒組分的基礎上引入一個永久性陽離子脂質,改進了包載RNPs的方法,使之能在中性緩沖液中進行,從而達到保護Cas9蛋白生物活性的目的。通過調節永久性陽離子脂質的加入比例,該文成功實現了RNPs的系統遞送和器官選擇性基因編輯。開發的RNPs遞送體系不僅可以簡化小鼠原位腫瘤模型的構建,還表現出了在遺傳類疾病中基因治療的應用價值。
參考文獻及原文鏈接:
Wei,T., Cheng, Q., Min, Y. et al. Systemic nanoparticle delivery of CRISPR-Cas9ribonucleoproteins for effective tissue specific genome editing. Nat Commun 11,3232 (2020).
https://doi.org/10.1038/s41467-020-17029-3
通訊作者:

DanielJ. Siegwart是德克薩斯大學西南醫學中心的副教授。他的研究計劃專注于開發先進的基于聚合物和脂質的系統,該系統可精確控制大分子的結構、順序和響應性,以用于藥物輸送、成像、遺傳疾病和癌癥。他是ReCode Therapeutics公司的共同創始人,致力于修飾tRNA負載的納米顆粒,用于糾正引起囊性纖維化和其他疾病的無義突變。











