目前,癌癥疫苗已被廣泛研究,如Hpv疫苗。然而,在大多數(shù)情況下,癌癥疫苗僅在預(yù)防癌癥方面有效,并且通常向健康個體給藥,但在已經(jīng)患癌癥的患者中啟動強(qiáng)大的抗腫瘤細(xì)胞毒性T細(xì)胞免疫反應(yīng)仍然是一項重大挑戰(zhàn),這主要是由于腫瘤內(nèi)部和腫瘤之間的異質(zhì)性以及免疫抑制性腫瘤微環(huán)境(TME)。
自體腫瘤細(xì)胞是接種疫苗的最佳來源,因為它們呈現(xiàn)了與腫瘤相關(guān)的抗原表位(TAE)的整個頻譜,可以觸發(fā)全面的免疫反應(yīng)。體外制備自體腫瘤細(xì)胞疫苗過程繁瑣并且需要足夠的腫瘤標(biāo)本,而體內(nèi)原位制備自體腫瘤細(xì)胞疫苗是一種很有吸引力的策略,它可以使用量身定制的疫苗有效地靶向個體患者的腫瘤。
通常,常規(guī)的癌癥治療策略,例如放射療法、化學(xué)療法和光動力療法(PDT),會觸發(fā)大量癌細(xì)胞的凋亡。細(xì)胞凋亡會釋放出“吞噬”信號,即膜磷脂酰絲氨酸(PS)由脂膜內(nèi)側(cè)翻向外側(cè),從而觸發(fā)巨噬細(xì)胞釋放免疫抑制性細(xì)胞因子。因此,巨噬細(xì)胞清除凋亡性腫瘤細(xì)胞可以增強(qiáng)TME的免疫抑制并防止刺激宿主免疫系統(tǒng)。值得注意的是,如果凋亡細(xì)胞不能被巨噬細(xì)胞迅速識別和清除,它們將失去細(xì)胞膜完整性并繼發(fā)性壞死。與細(xì)胞凋亡形成鮮明對比的是,繼發(fā)性壞死會產(chǎn)生多種TAE和損傷相關(guān)的分子模式(DAMPs),從而使垂死的腫瘤細(xì)胞具有免疫原性。在繼發(fā)性壞死條件下,DC有更多機(jī)會吸收TAE并接受DAMP的進(jìn)一步刺激,從而刺激免疫系統(tǒng)并觸發(fā)抗腫瘤免疫反應(yīng)。

圖| 細(xì)胞凋亡過程(自網(wǎng)絡(luò))
因此,推測在體內(nèi)將正在死亡的腫瘤細(xì)胞上的PS暴露作為將“凋亡” 轉(zhuǎn)化為“繼發(fā)性壞死”可能是創(chuàng)建原位自體腫瘤細(xì)胞疫苗的有前途的策略。
膜聯(lián)蛋白A5(ANX5)是一種用作檢測細(xì)胞凋亡的分子成像劑。先前報告表明,ANX5或可以阻斷PS。然而,在生理條件下,PS也暴露于某些特定的正常細(xì)胞的膜上,如成肌細(xì)胞,巨核細(xì)胞等。在這些正常細(xì)胞上阻斷PS暴露可能會導(dǎo)致嚴(yán)重的副作用。同時,由于PS暴露主要是細(xì)胞凋亡的早期過程,因此ANX5阻斷PS的最佳時間點(diǎn)被限制在一個狹窄的時間窗內(nèi)。
所以,一旦凋亡過程開始,則需要迅速釋放ANX5來阻止PS暴露并抑制巨噬細(xì)胞的吞噬作用對于實(shí)現(xiàn)特定的抗腫瘤免疫。
那如何能實(shí)現(xiàn)該迅速釋放策略呢?
于此,美國NIH陳小元、Zhen Yang、范文培等人利用一種直接的、多功能的納米技術(shù)用于原位治療性疫苗接種(ISTV),其中原發(fā)腫瘤作為特異性抗原庫來啟動個性化的抗腫瘤免疫。相關(guān)成果發(fā)表于Nature Biomedical Engineering上。

整體過程(劃重點(diǎn))
為了實(shí)現(xiàn)PS阻斷,研究人員首先設(shè)計了二硒化物橋接中空介孔有機(jī)硅納米膠囊(HMSeN)來固定ANX5,與此同時,膠囊還雜交上光敏試劑HPPH,而且將透明質(zhì)酸修飾的細(xì)菌外膜囊泡(HOMVs)裹在HMSeN(HMSeN–ANX5@HOMV)上,以進(jìn)一步促進(jìn)其穩(wěn)定性并增強(qiáng)其免疫刺激能力。HMSeN可以在生物氧化或生物還原條件下容易降解(二硒鍵斷裂),在氧化性TME或還原性細(xì)胞內(nèi)環(huán)境中實(shí)現(xiàn)ANX5蛋白的按需突發(fā)釋放。釋放的ANX5與PS結(jié)合后,巨噬細(xì)胞對凋亡細(xì)胞的識別被抑制,吞噬清除被延遲或阻斷。凋亡細(xì)胞會發(fā)生繼發(fā)性壞死,釋放TAEs和DAMPs,刺激TME,進(jìn)而刺激免疫系統(tǒng)恢復(fù)抗腫瘤免疫反應(yīng)。
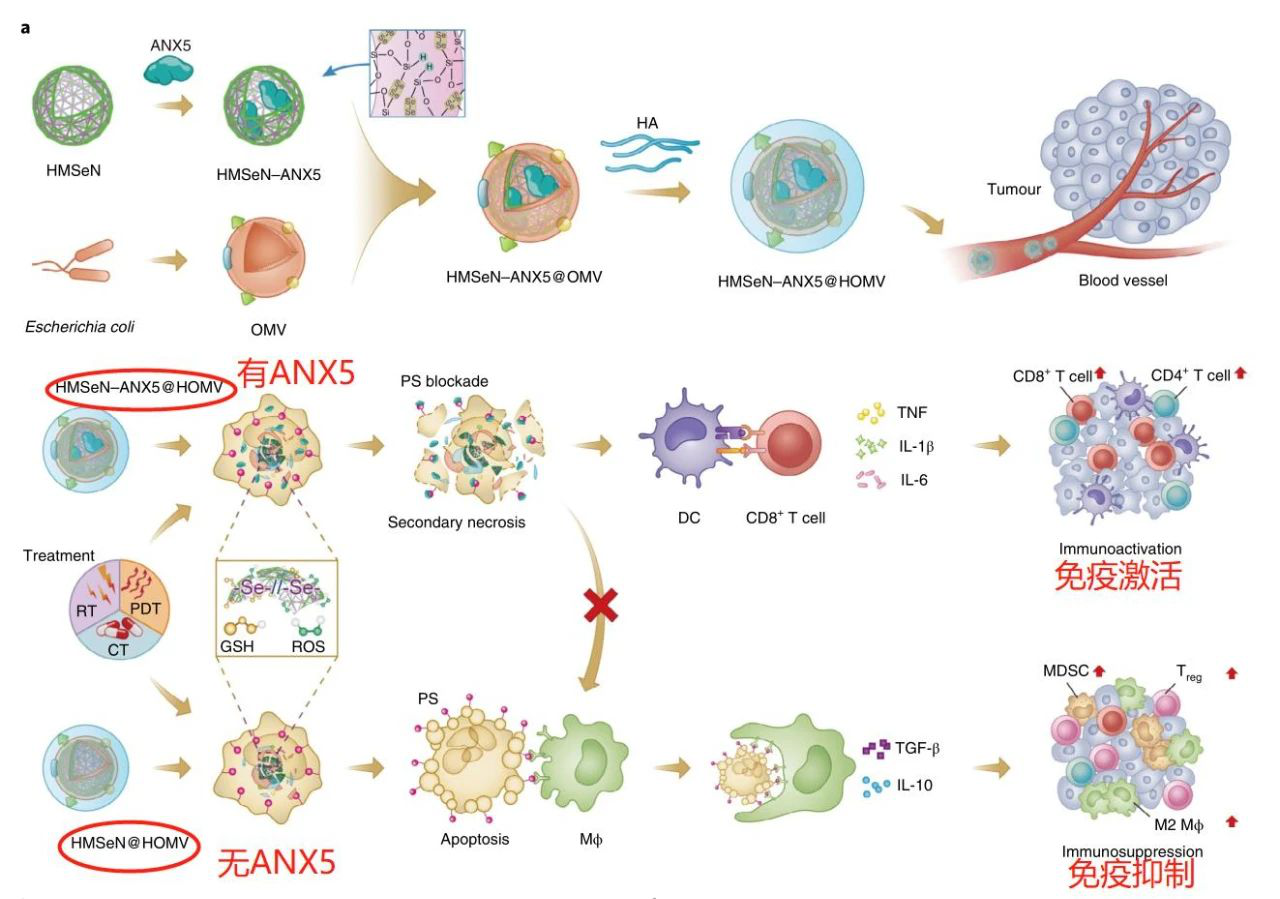
整體示意圖
快速釋放60%蛋白
在體外模擬體內(nèi)釋放試驗種,表明納米粒子在12小時內(nèi)顯示出大約60%的ANX5蛋白快速釋放,且ANX5蛋白在激光照射后還保留其生物活性。
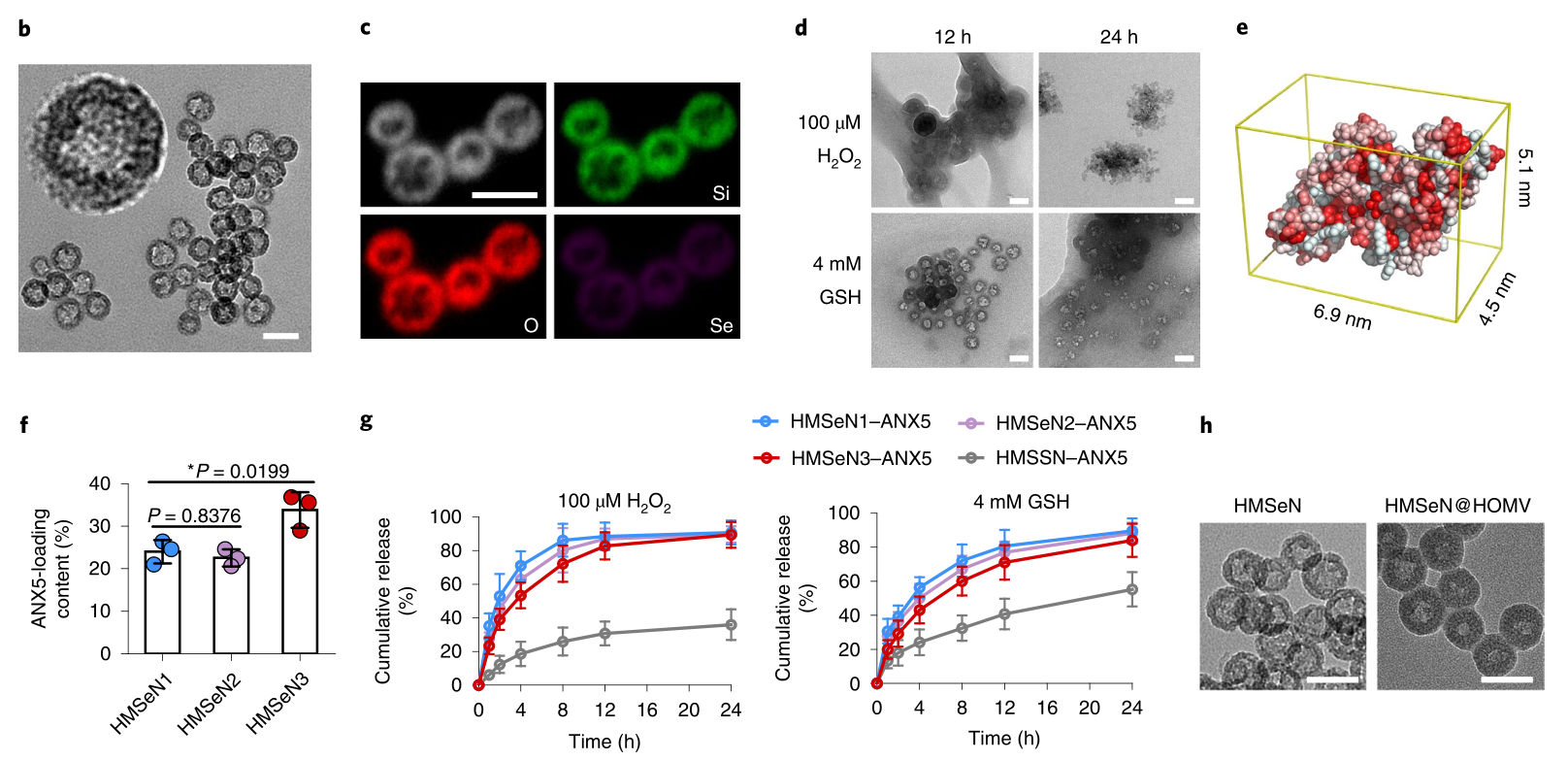
圖|材料表征與釋放曲線
體外細(xì)胞和體內(nèi)試驗表明,巨噬細(xì)胞對凋亡細(xì)胞的吞噬清除是一種抗炎過程,阻斷PS在凋亡細(xì)胞上的暴露以抑制巨噬細(xì)胞的吞噬作用可以將抗炎過程轉(zhuǎn)化為促炎過程。
還證實(shí)了通過HMSeN–ANX5 @ HOMV阻斷PS暴露以將細(xì)胞凋亡轉(zhuǎn)化為繼發(fā)性壞死可以刺激TME并刺激免疫系統(tǒng)。而且該誘導(dǎo)具有全身免疫刺激作用,并且全身炎癥是短暫的(7天可恢復(fù)正常),這對于確保其安全性至關(guān)重要。

圖|對PS的阻斷導(dǎo)致體內(nèi)腫瘤的轉(zhuǎn)錄組和細(xì)胞因子譜改變
根除一半小鼠的腫瘤
在后期的多種腫瘤模型治療實(shí)驗中,ISTV可以導(dǎo)致有效的腫瘤消退和腫瘤生長抑制。事實(shí)上,ISTV在大約50%的小鼠體內(nèi)徹底根除了4T1(小鼠乳腺癌細(xì)胞)腫瘤,并產(chǎn)生了持久的免疫記憶。
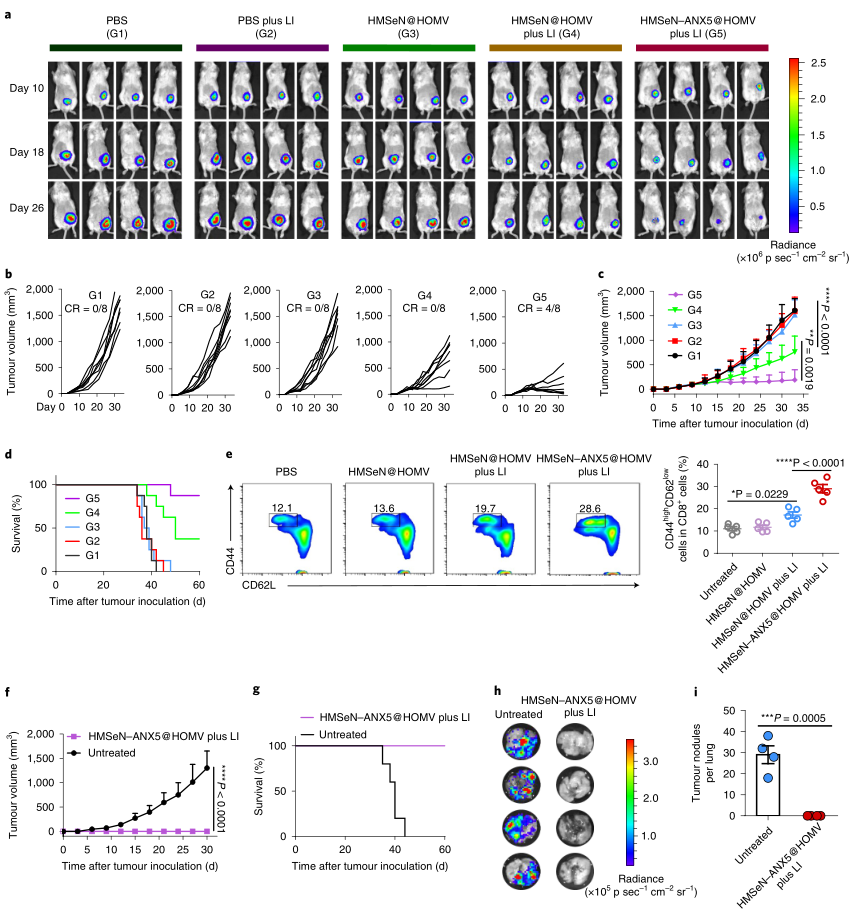
圖|HmSeN–ANX5@HomV引發(fā)針對原位4T1乳腺腫瘤的強(qiáng)大抗腫瘤功效和持久的免疫記憶
小結(jié):
綜上所述,本文使用原發(fā)腫瘤本身充當(dāng)原位貯存庫,其中包含啟動強(qiáng)大的抗腫瘤免疫反應(yīng)所需的所有TAE和DAMP,這種針對ISTV的方法避免了繁瑣的體外腫瘤抗原生產(chǎn)。合成無定形二氧化硅通常被美國FDA視為安全材料,硒是人體中抗氧化酶的重要成分,有助于潛在的臨床轉(zhuǎn)化。鑒于當(dāng)前大多數(shù)癌癥治療方法均可誘導(dǎo)細(xì)胞凋亡,因此ISTV方法可為個性化原位癌疫苗的開發(fā)提供強(qiáng)大而直接的通用方法。
參考文獻(xiàn):
Li,L., et al. Burst release of encapsulated annexin A5 in tumours boosts cytotoxicT-cell responses by blocking the phagocytosis of apoptotic cells. Nat BiomedEng (2020).
https://doi.org/10.1038/s41551-020-0599-5











