先天性免疫激動(dòng)劑被認(rèn)為可能會(huì)促進(jìn)腫瘤特異性CD8+ T細(xì)胞的啟動(dòng)和募集,并作為一種癌癥免疫療法而受到關(guān)注。近日,Science期刊上背靠背發(fā)表了兩篇關(guān)于先天性免疫激動(dòng)劑用于抗腫瘤的論文,兩篇論文分別是來自美國(guó)斯克利普斯研究所(論文1)和美國(guó)默克公司(論文2)的研究人員報(bào)道了兩種新型全身給藥(一種為口服,一種靜脈給藥)的先天性免疫激動(dòng)劑。
論文1講述的是關(guān)于確定了一種非核苷酸的小分子STING激動(dòng)劑,稱為SR-717。
論文2報(bào)道的是確定了一種可口服的非核苷酸人類STING激動(dòng)劑,MSA-2。皮下和口服MSA-2方案具有良好的耐受性,可刺激腫瘤中的干擾素-β分泌,誘導(dǎo)腫瘤消退并具有持久的抗腫瘤免疫力,并與抗PD-1治療協(xié)同作用。

論文1

論文2
靶向免疫檢查點(diǎn)受體、程序性細(xì)胞死亡蛋白1(PD-1)或其主要配體PD-L1的抗體已被美國(guó)FDA批準(zhǔn)用于15種不同癌癥的臨床應(yīng)用。臨床療效與治療前激活的T細(xì)胞基因標(biāo)志物相關(guān),抗PD-1給藥后,腫瘤浸潤(rùn)性CD8+ T細(xì)胞顯著擴(kuò)張。盡管臨床上取得了成功,但大部分癌癥患者缺乏足夠的T細(xì)胞炎癥,這些患者通常對(duì)檢查點(diǎn)阻斷免疫治療沒有反應(yīng)。據(jù)認(rèn)為,在腫瘤微環(huán)境中觸發(fā)基于T細(xì)胞的炎癥反應(yīng)可能有助于擴(kuò)大從抗PD-1治療和其他免疫療法中獲益的患者的比例。
實(shí)現(xiàn)這一目標(biāo)的一個(gè)策略是了解T細(xì)胞自發(fā)激活和腫瘤浸潤(rùn)發(fā)生時(shí)所涉及的基本機(jī)制步驟,目的是在未發(fā)生時(shí)模仿或復(fù)制這些步驟。通常,適應(yīng)性免疫應(yīng)答(即誘導(dǎo)T細(xì)胞或抗體反應(yīng))首先需要先天免疫系統(tǒng)的激活,其非特異性地暗示“危險(xiǎn)”或外部威脅的存在。臨床前腫瘤模型顯示,先天性抗原呈遞細(xì)胞(APC)對(duì)內(nèi)源性CD8+ T細(xì)胞的啟動(dòng)作用(激活)在STING(干擾素基因刺激物)缺陷小鼠中顯著減少。缺乏STING的小鼠還顯示出對(duì)腫瘤植入的反應(yīng),包括干擾素-β(IFN-β)在內(nèi)的細(xì)胞因子產(chǎn)生減少,并且未能排斥高度免疫原性的腫瘤。在缺乏其他先天免疫途徑(例如特定的Toll樣受體(TLR))的小鼠中未觀察到這些缺陷。
STING途徑
STING途徑是一種胞質(zhì)DNA傳感途徑,在腫瘤浸潤(rùn)性APCs的細(xì)胞質(zhì)中可以發(fā)現(xiàn)腫瘤來源的DNA。當(dāng)與cGAS [cGAMP合酶)結(jié)合時(shí),在細(xì)胞內(nèi)檢測(cè)到胞質(zhì)DNA,生成cGAMP,cGAMP繼而參與并激活STING。STING下游的信號(hào)傳導(dǎo)導(dǎo)致APC激活和炎性細(xì)胞因子的產(chǎn)生,繼而促進(jìn)T細(xì)胞的啟動(dòng)和募集。綜上所述,這些發(fā)現(xiàn)形成了一個(gè)假設(shè):即STING途徑的外源性激動(dòng)劑可能具有觸發(fā)新的先天性免疫激活的潛力,從而導(dǎo)致可以單獨(dú)或結(jié)合檢查點(diǎn)阻斷免疫療法來控制腫瘤生長(zhǎng)。
研究用于免疫療法的第一個(gè)STING激動(dòng)劑是DMXAA分子,它在臨床前模型中具有抗腫瘤活性,隨后被確定與小鼠STING分子相互作用但不與人類STING相互作用。第一代人類STING激動(dòng)劑,包括MIW815(ADU-S100)和MK-1454,已在早期臨床試驗(yàn)中單獨(dú)進(jìn)行了研究,并與抗PD-1組合進(jìn)行了研究。迄今為止,已經(jīng)觀察到了對(duì)這些激動(dòng)劑的一些臨床反應(yīng),但是僅在少數(shù)患者中。人們正在探索幾種生物學(xué)上的考慮,以了解反應(yīng)與抵抗的機(jī)制。這些包括破譯腫瘤微環(huán)境中的哪些免疫細(xì)胞才能使STING激動(dòng)劑誘導(dǎo)下游T細(xì)胞啟動(dòng),了解STING激動(dòng)劑的最佳劑量和時(shí)間表以避免過度刺激和負(fù)調(diào)節(jié),并確定臨床活動(dòng)的預(yù)測(cè)生物標(biāo)志物。
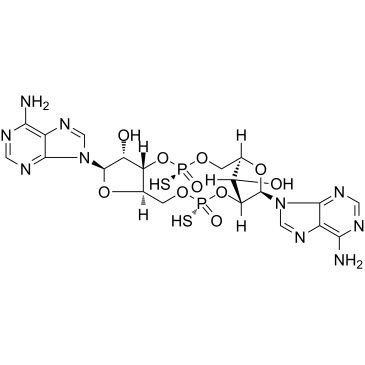
ADU-S100化學(xué)結(jié)構(gòu)式(自MCE官網(wǎng))
基于環(huán)二核苷酸的STING激動(dòng)劑的代謝不穩(wěn)定,需要在腫瘤內(nèi)施用,但腫瘤內(nèi)給藥的具有局限性。少數(shù)靜脈注射的STING激動(dòng)劑已開始在臨床試驗(yàn)中進(jìn)行評(píng)估(NCT03843359,NCT04420884和NCT04096638),STING激動(dòng)劑的下一個(gè)發(fā)展重點(diǎn)可能是針對(duì)全身給藥的激動(dòng)劑,正如本次發(fā)表的兩篇論文一樣。
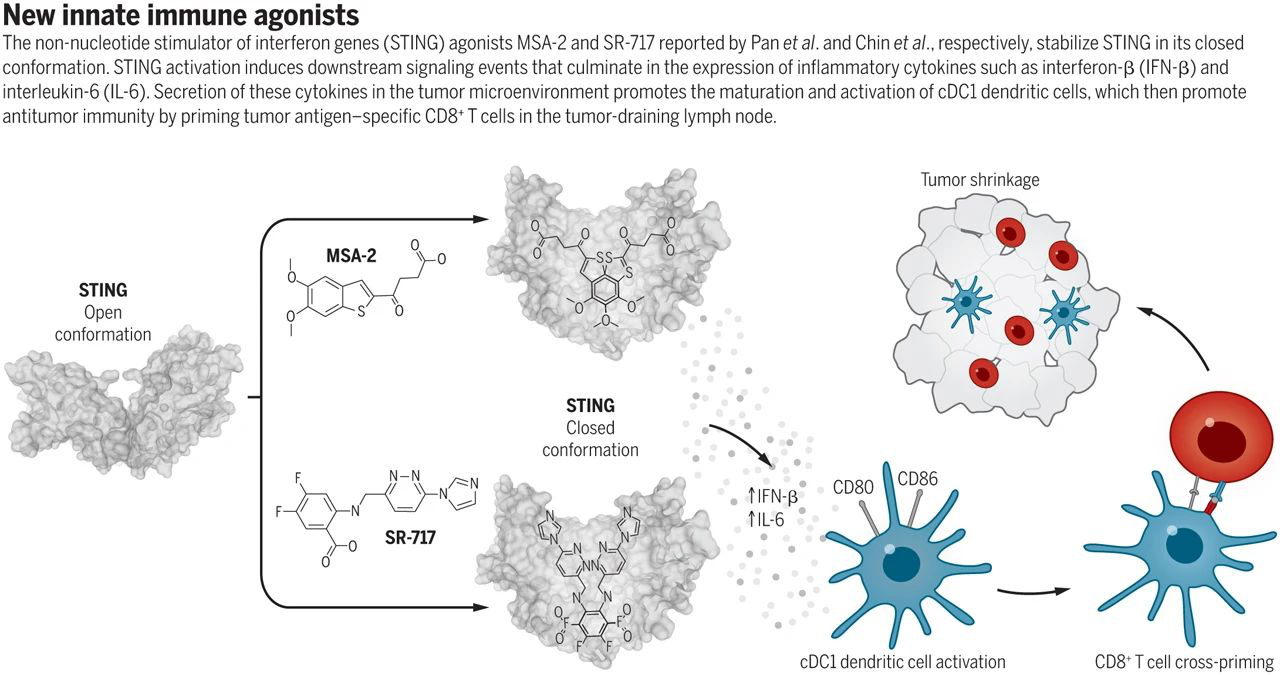
新的先天免疫激動(dòng)劑(源自Science)
全身給藥的STING激動(dòng)劑的臨床開發(fā)需要考慮幾個(gè)重要因素。
1)一種是全身性給藥可能導(dǎo)致更大的毒性,因?yàn)樵谀[瘤微環(huán)境之外使用APC可能會(huì)釋放大量的IFN-β和其他炎性細(xì)胞因子。來自斯克利普斯研究所的論文報(bào)告稱,有效劑量的SR-717導(dǎo)致血清IFN-β的濃度明顯低于另一種最近開發(fā)的全身性STING激動(dòng)劑diABZI-2。全身給藥diABZI-2也可促進(jìn)腫瘤控制。但是,diABZI-2以其開放構(gòu)象穩(wěn)定STING,類似于細(xì)菌產(chǎn)物環(huán)狀di-GMP,但不同于內(nèi)源性cGAMP。
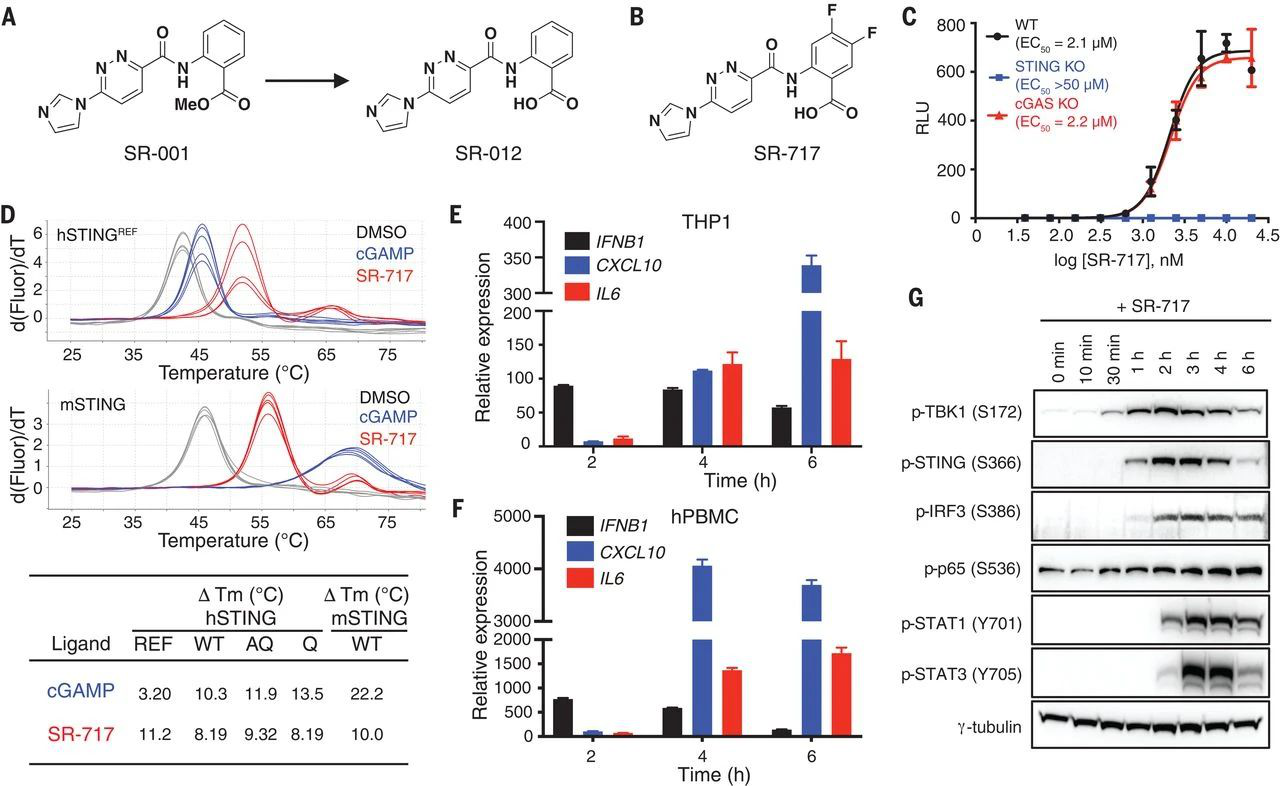
論文1|小分子STING激動(dòng)劑SR-717的發(fā)現(xiàn)和概況
兩篇論文所使用的激動(dòng)劑都穩(wěn)定了STING的閉合構(gòu)象。有必要進(jìn)行進(jìn)一步的研究,以弄清穩(wěn)定STING處于開放和封閉狀態(tài)的生物學(xué)后果。來自默克公司的論文描述的MSA-2化合物盡管在全身給藥,但在小鼠中顯示出有限的毒性,這是由于其在腫瘤微環(huán)境的酸性環(huán)境中具有優(yōu)先的生物活性。
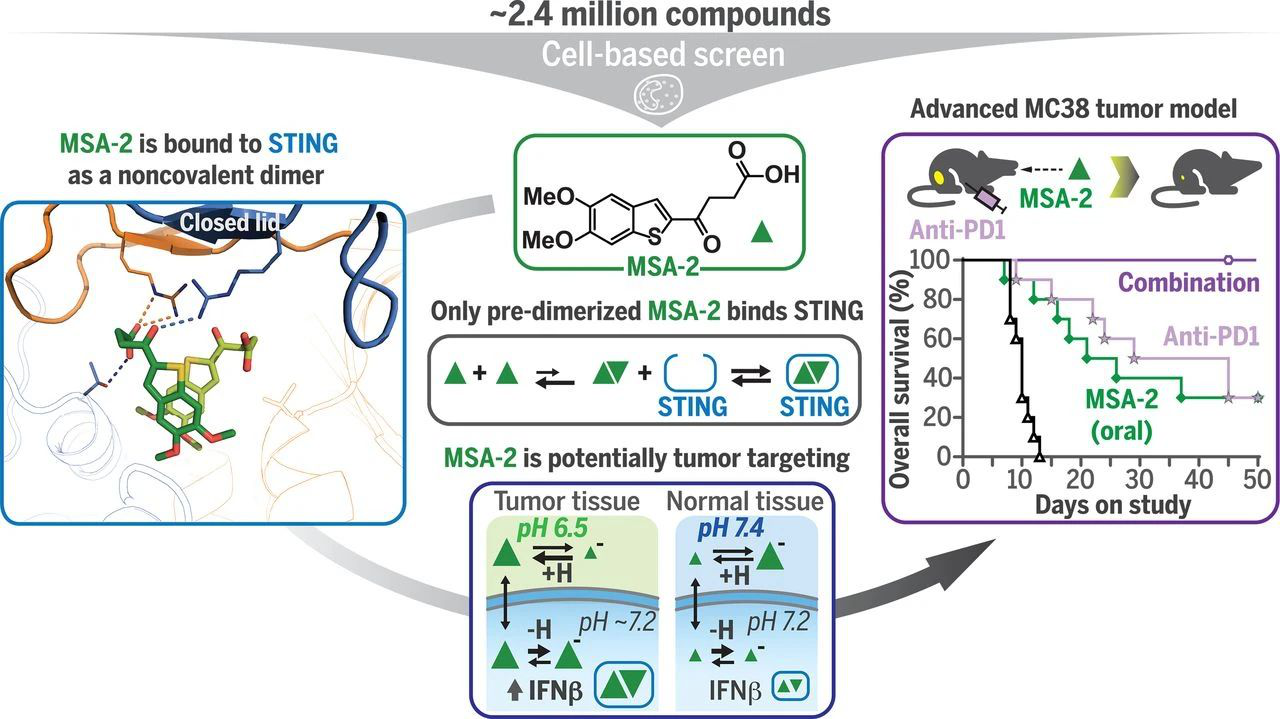
論文2|STING激動(dòng)劑MSA-2
2)第二個(gè)重要考慮因素是全身性STING激動(dòng)劑對(duì)特定免疫細(xì)胞亞群的影響。第1篇論文指出,SR-717可以在體外原代人外周血單核細(xì)胞中誘導(dǎo)免疫抑制分子PD-L1和吲哚胺2,3-雙加氧酶1(IDO1)的表達(dá)。此外,在黑素瘤小鼠模型中腹膜內(nèi)注射SR-717導(dǎo)致CD11c+ CD8-樹突細(xì)胞上PD-L1表達(dá)增加,但從引流腫瘤的淋巴結(jié)中分離出的CD8+樹突細(xì)胞上PD-L1表達(dá)增加。盡管CD8+樹突狀細(xì)胞被認(rèn)為是誘導(dǎo)腫瘤特異性CD8+ T細(xì)胞啟動(dòng)的關(guān)鍵APC亞型,但值得注意的是SR-717對(duì)這些樹突狀細(xì)胞亞型的影響不同。STING激動(dòng)劑在腫瘤微環(huán)境內(nèi)相關(guān)細(xì)胞亞群中誘導(dǎo)刺激和抑制事件的方式的進(jìn)一步表征至關(guān)重要。在黑色素瘤小鼠模型中,抗PD-1或抗PD-L1治療均未改善SR-717的抗腫瘤功效,這與論文2種的MSA-2相反,MSA-2與抗PD-1療法組合可明顯縮小腫瘤。這些差異可能是由于這些STING激動(dòng)劑的分子特性不同,與免疫檢查點(diǎn)阻斷劑相結(jié)合的劑量和給藥方案差異或所使用的實(shí)驗(yàn)?zāi)P椭g的差異。
3)臨床發(fā)展的第三個(gè)考慮因素是給藥藥物的劑量和時(shí)間安排。這些需要仔細(xì)優(yōu)化,因?yàn)槿斫o藥也可能產(chǎn)生鐘形的功效曲線。在與活動(dòng)相關(guān)的腫瘤微環(huán)境中探索藥效學(xué)終點(diǎn)應(yīng)指導(dǎo)治療劑量的選擇。
4)還需要考慮哪些腫瘤類型和哪些患者可能對(duì)這些藥物產(chǎn)生反應(yīng),因此還需要針對(duì)適當(dāng)?shù)幕颊哌x擇進(jìn)行預(yù)測(cè)性生物標(biāo)記。
5)最后要考慮的是,其他先天性免疫激動(dòng)劑也在臨床開發(fā)中不斷發(fā)展,包括靶向TLR途徑的藥物,例如TLR9。了解哪種先天性免疫途徑在不同的患者群體中在功能上相關(guān),對(duì)于利用現(xiàn)有免疫療法優(yōu)化先天性免疫激動(dòng)劑組合至關(guān)重要。
這兩篇Science報(bào)道的化合物說明了STING激動(dòng)劑的獨(dú)特分子特性如何決定腫瘤活性與全身活性之間的平衡。可以全身給藥的非核苷酸小分子STING激動(dòng)劑可能是靶向該途徑的一種有吸引力的方法,一旦優(yōu)化就具有轉(zhuǎn)化治療前景的潛力。
參考文獻(xiàn):
1.Emily N. Chin, et al., Antitumor activity of a systemic STING-activatingnon-nucleotide cGAMP mimetic. Science 2020.
DOI:10.1126/science.abb4255
2.Bo-Sheng Pan,et al., An orally available non-nucleotide STING agonist withantitumor activity. Science 2020.
DOI:10.1126/science.aba6098
3.Emily F. Higgs, et al., Immunotherapy with a sting. Science 2020.
DOI:10.1126/science.abc6622











