作為21世紀生物科學領域最具發展前景的技術,干細胞治療技術是攻克各種傳統醫學力所不及的重大疾病的一種嶄新的醫療技術。由于干細胞尚未分化或分化程度低,通過誘導干細胞可以“變形”成其他組織細胞,在生命科學的細胞修復、發育生物學、藥物學等領域有著極為廣闊的應用前景。
在20世紀60年代,干細胞移植治療開始發展。近年來,研究人員探索了通過誘導多功能干細胞培養的心臟細胞移植治療心臟病的可能性。但是,移植的心臟細胞通常不能植入體內,而且幾天后也會死亡。臨床醫生也擔心,確實植入的細胞可能會導致嚴重的健康問題,如心律失常,從長遠來看甚至會導致腫瘤的形成。而且,在2009年,我國衛生部將干細胞技術歸入“第三類醫療技術”( 涉及重大倫理問題,安全性、有效性尚需經規范的臨床試驗研究進一步驗證的醫療技術)。
那么,有沒有辦法擺脫細胞植入也能實現心臟的治療呢?
本文簡介:
近日,阿拉巴馬大學伯明翰分校Jianyi Zhang、Ling Gao等人開發出一種策略,該策略是直接使用外泌體來模擬心臟細胞移植產生的心臟再生作用,而且重要的一點是,它同時有可能避免與全細胞移植相關的風險。該課題組的方法加速了豬心臟病發作后的恢復,可以解決限制全細胞心臟療法的臨床應用安全性和有效性的問題。成果以題為“Exosomes secreted by hiPSC-derived cardiac cells improve recoveryfrom myocardial infarction in swine”發表于ScienceTranslational Medicine上,并選為封面文章。
封面|減輕心肌梗塞
整體思路:
本文提出的研究是通過使用來自不同hiPSC衍生細胞類型(hiPSC-CM(來自心肌細胞),hiPSC-EC(內皮細胞)和hiPSC-SMC(平滑肌細胞))的外泌體進行大量體外測定,并與由人誘導的多能干細胞(hiPSC)衍生的心肌細胞(CMs; 1000萬),內皮細胞(ECs; 500萬)和平滑肌細胞(SMCs; 500萬)的混合物的治療效果進行比較,并評估心肌梗塞后豬的心肌恢復能力。
實驗主要分組有:接受假手術;未經治療的梗死(MI組);使用hiPSC-CM,hiPSC-EC和hiPSC-SMC進行梗塞和治療(MI +細胞組);與來自同劑量細胞的均質化片段一起給藥組(MI + Fra組);從hiPSC-CMs:hiPSC-ECs:hiPSC-SMC=2:1:1混合物中提取的外泌體組(7.5mg)(MI + Exo組)
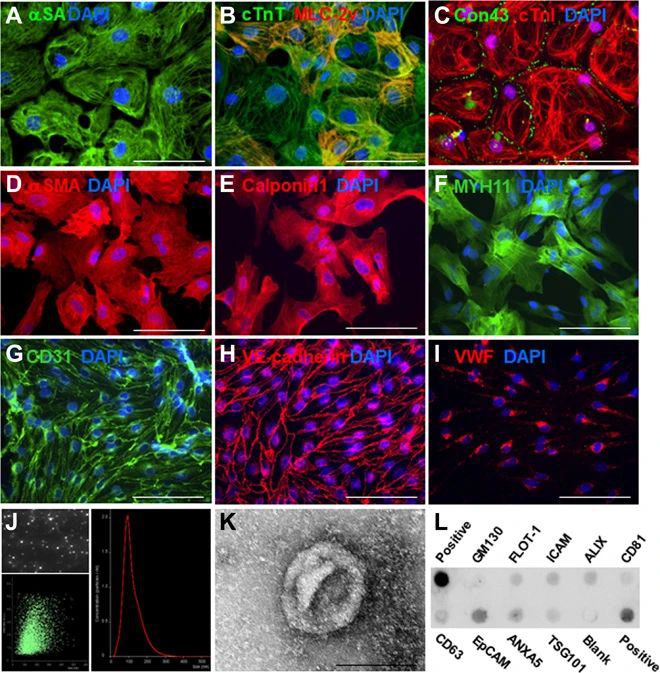
圖|hiPSC-CM,hiPSC-SMC和hiPSC-EC以及所有三種細胞類型分泌的外泌體的表征
體內實驗的主要發現有兩點:
(i)在心肌梗塞4周后,用hiPSC-CC,hiPSC-CC片段或hiPSC-CC外泌體治療的動物的左室功能,梗塞面積,壁應力,心臟肥大,細胞凋亡和血管生成的測量值相似,且與無需三項實驗處理即可恢復的動物相比有明顯改善。
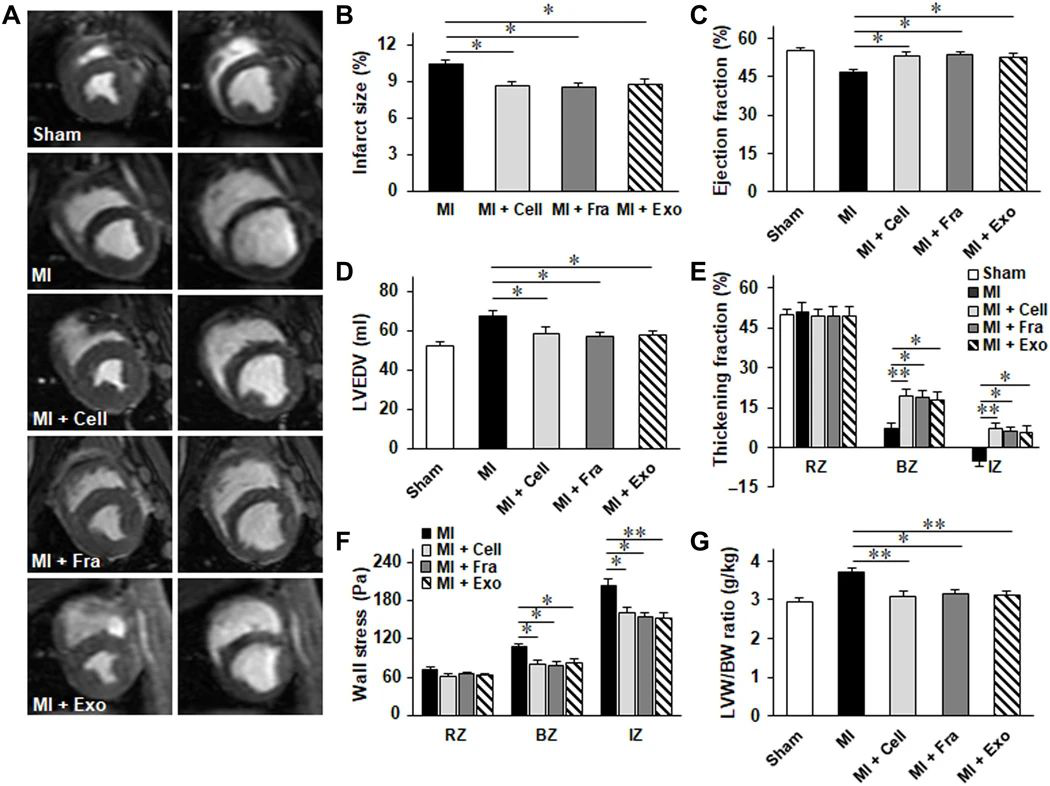
圖|hiPSC-CC外泌體可促進心肌功能的恢復并限制心臟肥大
(ii)外泌體治療并沒有增加心律失常的頻率。研究人員還表明, hiPSC-CC產生的外泌體可促進培養的EC和分離的主動脈環中的血管生成活性,并且通過減少細胞凋亡、維持細胞內鈣穩態和增加細胞ATP含量來保護培養的hiPSC-CM免受無血清低氧培養基的細胞毒作用。
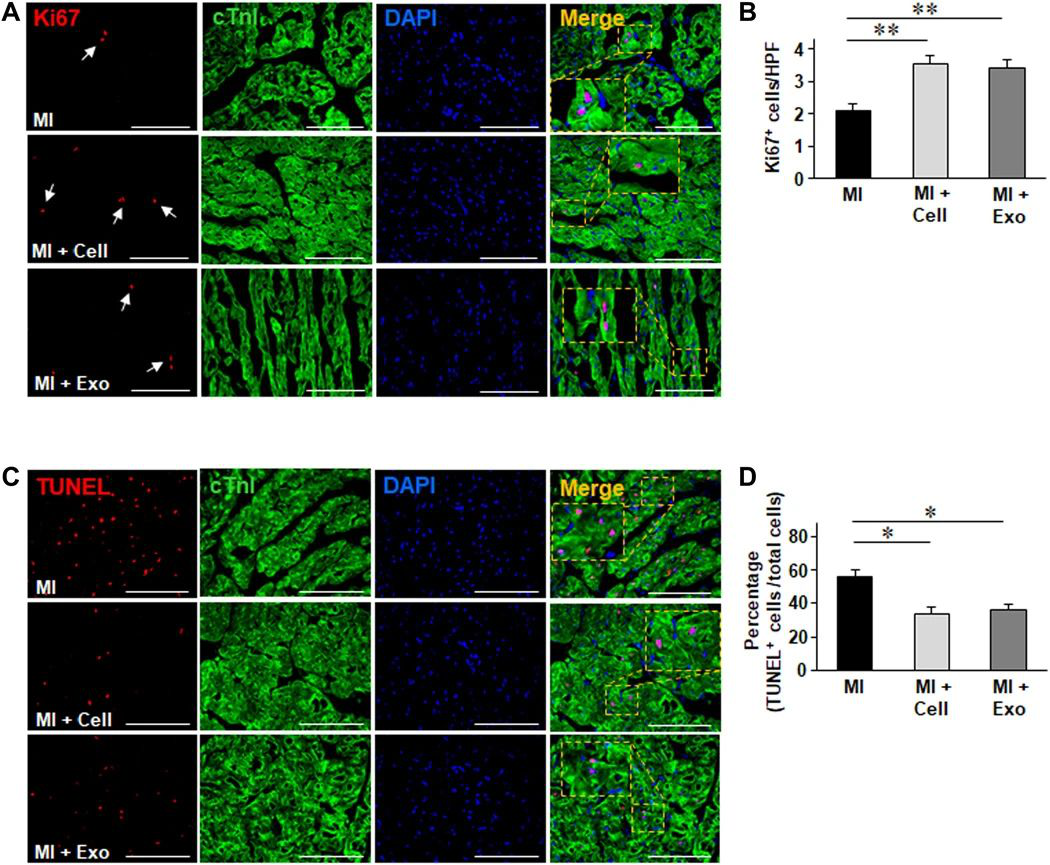
圖|hiPSC-CC外泌體改善增殖并減少細胞凋亡

圖|hiPSC-CC外泌體可改善梗死豬心臟的細胞能量代謝
小結
綜上所述,在豬MI模型中,hiPSC-CC產生的外泌體可重現與注射的hiPSC-CC相關的許多益處。hiPSC-CC外泌體是無細胞的,因此,可使醫生利用hiPSC衍生細胞的心臟保護和修復特性,同時避免與致瘤風險、細胞存儲、運輸和免疫排斥相關的復雜性。因此,有必要進行其他研究以全面評估hiPSC-CC外泌體的治療潛力。
參考文獻:
LingGao, et al., Exosomes secreted by hiPSC-derived cardiac cells improve recoveryfrom myocardial infarction in swine. Science Translational Medicine 2020.
DOI:10.1126/scitranslmed.aay1318
https://stm.sciencemag.org/content/12/561/eaay1318











