中國科學院上海硅酸鹽研究所(簡稱上海硅酸鹽所)淵源于1928年成立的國立中央研究院工程研究所,上海硅酸鹽所現已成為集材料前沿探索、高技術創新、應用發展研究為一體的無機非金屬材料科研機構,形成了“基礎研究—應用研究—工程化、產業化研究”有機結合的較為完備的科研體系。
學科方向是先進無機材料科學與工程,主要研究領域覆蓋了高性能結構陶瓷、功能陶瓷、透明陶瓷、陶瓷基復合材料、人工晶體、無機涂層、能源材料、生物材料、古陶瓷以及先進無機材料性能檢測與表征等,是國內該領域科學研究單位中門類最為齊全的研究所。
緊密圍繞中科院“率先行動”計劃、上海科創中心建設,圍繞先進制造、能源、信息、環境與健康、國防工業等重點應用領域,聚焦“三重大產出”,在基礎與前瞻性研究、高技術研究、產業化關鍵技術與成果轉化等方面取得了一系列具有重要影響力的研究成果,為國家安全、國民經濟建設以及社會進步作出了重要貢獻
于此,奇物論編輯部整理了近年上海硅酸鹽所在Nature、Science系列發表的論文,供大家學習和交流。
1. Science Advances:一種高靈敏度、高選擇性的近紅外鉀離子成像納米傳感器
K+濃度是多種生物體過程中的重要指標,目前成功開發了多種光學K+離子探針用于監測生物體中的K+變化,但是目前的K+離子探針具有一定缺陷,比如靈敏度較低,難以對生物體中的信號變化清楚的表征。此外,對生物體中的深部組織的探測無法實現,這是因為目前大多數的K+探針使用波長較低的光激發。
于此,中科院硅酸鹽研究所施劍林、步文博,中國科學院腦科學與智能技術卓越中心杜久林、熊志奇等報道了紅外K+離子納米探針實現了對生物組織和活體動物深層結構的高選擇性高響應度的成像監測。這種納米探針通過上轉換材料進行測試(在多孔SiO2納米粒子中裝載上轉換納米材料和K+指示劑)并在SiO2上包覆K+離子過濾膜,通過離子過濾膜對K+的選擇性過濾,上轉換納米粒子通過吸收紅外光并轉變為紫外光,激發K+指示劑,因此能夠對環境中的K+濃度變化進行表征。

文章要點:
要點1:材料合成
YCl3,YbCl3,TmCl3溶解于油酸和1-十八碳烯混合溶液中,Ar氣氛中加熱到156 ℃保持1 h,降低到室溫后加入NH4F和NaOH的甲醇溶液,隨后加熱到290 ℃保持1.5 h,得到NaYF4:Yb納米粒子。隨后在NaYF4:Yb界面上包覆一層NaYF4:Yb/Nd。通過將合成的NaYF4:Yb/Nd/NaYF4:Yb分散到Igepal CO-520環己烷溶液中,加入NH3水,緩慢加入TEOS原硅酸四乙酯,得到包裹有SiO2的材料。隨后再負載一層介孔SiO2膜,通過加入CTAC十六烷基三甲基氯化銨、TEA三乙醇胺,在80 ℃中加入TEOS,得到包覆介孔SiO2層的材料。在材料表面負載保護層:保護膜前驅液配制,將N-芐基水楊酰胺、K2CO3溶解于DMF中,加熱到90 ℃,隨后加入1,1,1-三(對甲苯磺酰氧基甲基)乙烷、2-氨基對苯二甲酸攪拌24 h。通過柱層析方法(石油醚/乙酸乙酯:2:1)得到白色固體保護膜原料。在乙腈溶液中將保護膜負載到上轉換復合納米材料表面。
要點2:水溶液中的K+離子監測性能測試
對150 mM K+, 150 mM Na+, 2 mM Ca2+, 2 mM Mg2+, 50 μM Fe2+, 2 mM Zn2+, 50 μM Mn2+, 50 μM Cu2+監測性能顯示,K+離子指示劑對K+的選擇性較高。并且結果顯示界面上~2 nm厚度的過濾膜改善了監測性能。
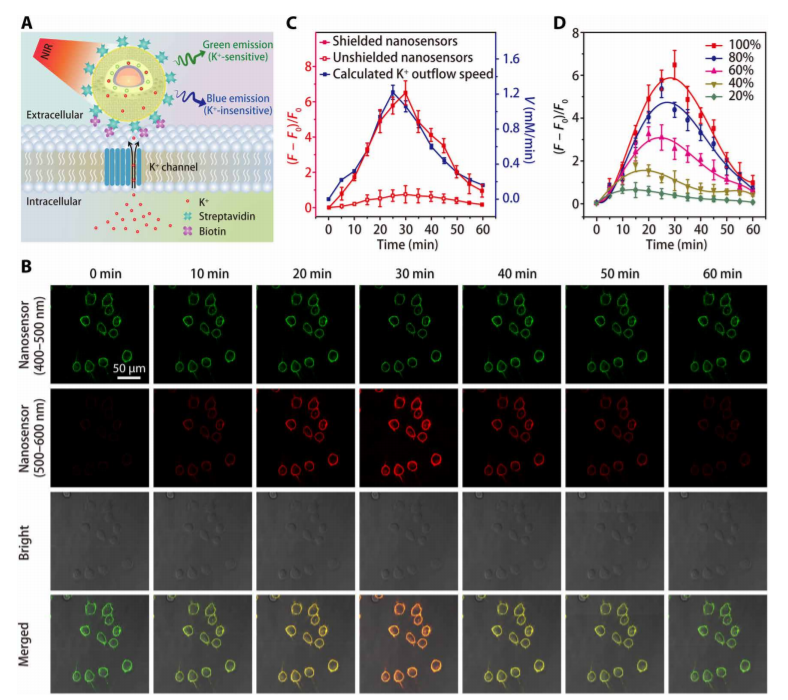
要點3:細胞中微量K+測試
在納米顆粒界面上負載一層PEG膜結構防止對蛋白質的無選擇吸附、并改善探針的穩定性,結果顯示這種探針具有監測生物體中的K+變化能力。對鼠大腦和斑馬魚大腦中的K+和Ca2+監測。
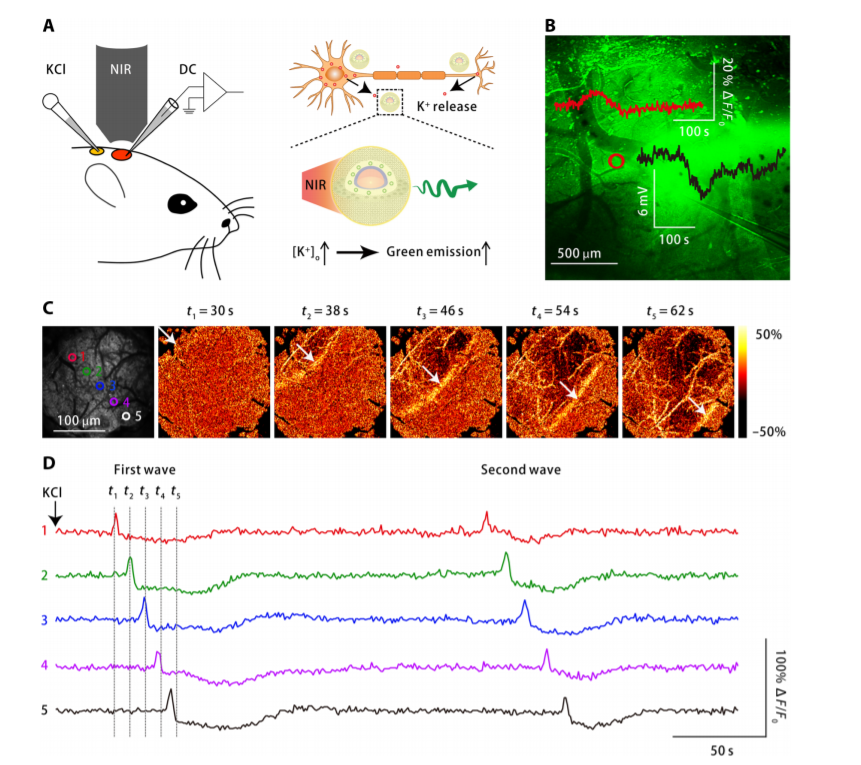
Jianan Liu, et al. A highly sensitive and selective nanosensor for near-infrared potassium imaging,Science Advance 2020, 6, 16, eaax9757
DOI: 10.1126/sciadv.aax9757
https://advances.sciencemag.org/content/6/16/eaax9757.full
常江Science子刊:邊燒邊修復,生物活性玻璃測出最佳腫瘤治療溫度!(深度解讀)
中科院上海硅酸鹽研究所常江研究員等人設計了一種具有光熱性能、熒光溫度監測性能和組織修復活性的Nd-Ca-Si生物玻璃系統和可注射的玻璃/藻酸鹽復合水凝膠,并在腫瘤部位進行了注射并達到了最佳效果。光熱性能可實現最佳的腫瘤治療,并具有生物活性,可在PTT期間修復受熱損傷最小的組織。
通過水凝膠的溫度測量功能,確定了小鼠模型的最佳PTT溫度在53°C,在該溫度下,腫瘤被完全消除,而周圍的正常組織僅受到了最小程度的燒傷。此外,由于復合水凝膠的再生生物活性,在PTT期間誘導了輕微受損組織的再生。研究結果表明,這種多功能生物材料不僅可以作為具有溫度監測和組織修復功能的植入式醫療器械在PTT腫瘤治療中具有潛在的應用價值,而且可以作為溫度監測材料用于其他類型的熱療法的原位溫度測量。
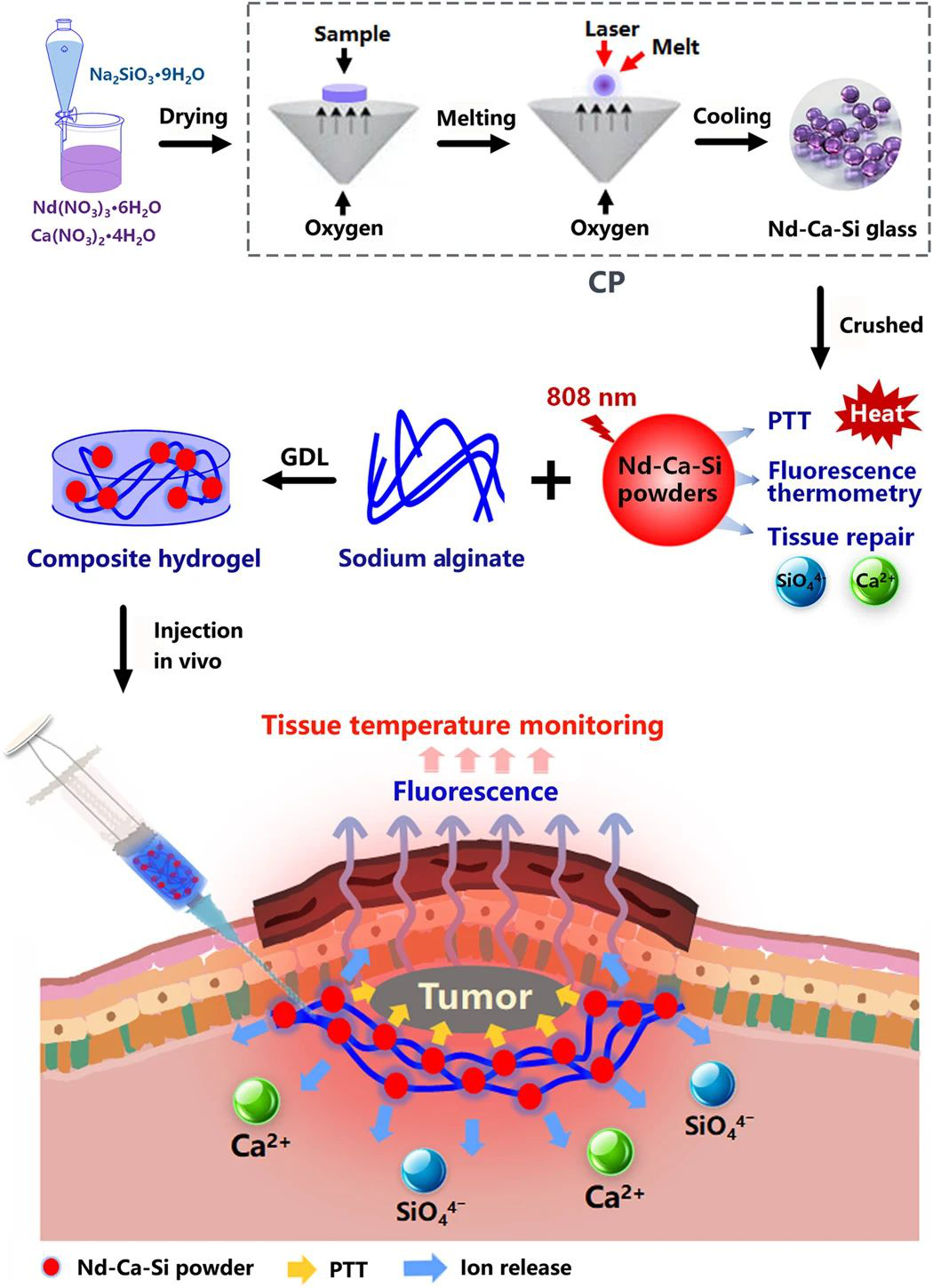
Lingling Ma, et al.,Multifunctionalbioactive Nd-Ca-Si glasses for fluorescence thermometry, photothermal therapy,and burn tissue repair. Science Advances 2020.
DOI: 10.1126/sciadv.abb1311
https://advances.sciencemag.org/content/6/32/eabb1311
3. Science Advances:3D打印仿骨支架用于骨骼再生中的多細胞遞送
組織工程支架的結構與功能的整合對于模擬天然骨組織具有重要意義。然而,層次結構的復雜性、對力學性能的要求以及骨常駐細胞的多樣性是構建仿生骨組織工程支架的主要挑戰。于此,中國科學院上海硅酸鹽研究所吳成鐵等人利用基于數字激光處理(DLP)的3D打印技術,成功制備了一種具有完整層次哈弗氏骨結構的哈弗氏仿骨支架。
本文要點:
1) 通過改變模擬哈弗骨骼結構的參數,可以很好地控制支架的抗壓強度和孔隙率。
2) 通過體外誘導成骨、血管生成和神經源性分化,模擬哈弗氏骨的支架顯示出巨大的多細胞傳遞潛力,并在體內加速血管的生長和新骨的形成。這項工作通過模擬天然復合骨組織進行組織再生,為設計結構化和功能化的生物材料提供了一種新的策略。
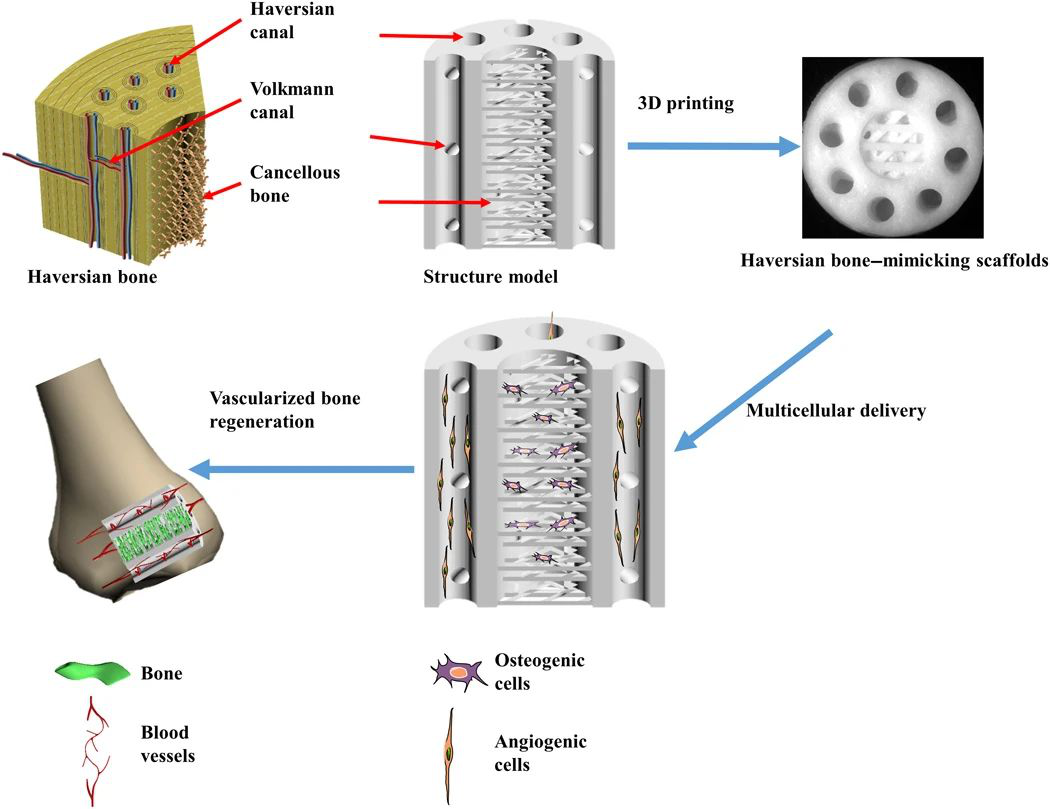
Zhang M, et al. 3D printing of Haversian bone–mimicking scaffolds for multicellular delivery in bone regeneration. Science Advances. 2020;6(12):eaaz6725.
https://doi.org/10.1126/sciadv.aaz6725
4. Nature. Commun:血管外凝膠收縮引起的內應力用于增強對腫瘤的饑餓治療
盡管目前的饑餓療法有效,但它們往往伴隨著一些固有的缺點,如持續性差、易發生腫瘤轉移和復發。在此,同濟大學徐輝雄、張坤等聯合中科院上海硅酸鹽研究所陳雨等建立了血管外凝膠收縮引起內應力策略,用于擠壓和收縮血管,阻斷血液和營養供應,降低血管密度,誘導缺氧和凋亡,最終實現惡性腫瘤的饑餓治療。
他們設計了一種由金納米棒(GNRs)和熱敏性水凝膠混合物組成的生物相容性復合水凝膠,其中GNRs可以增強水凝膠混合物的結構性能,并使凝膠收縮引起的內應力具有魯棒性。系統實驗表明,這種饑餓療法可以抑制PANC-1胰腺癌和4T1乳腺癌的生長。更重要的是,這種饑餓策略可以通過降低血管密度和血供,阻斷腫瘤的遷移通道,從而抑制腫瘤的轉移和復發,為腫瘤的綜合治療提供了一條頗具前景的途徑。

Kun Zhang, et al. Extravascular gelation shrinkage-derived internal stress enables tumor starvation therapy with suppressed metastasis and recurrence, Nat. Commun., 2019.
https://www.nature.com/articles/s41467-019-13115-3
5. Nature Commun:檢查點阻斷和納米增敏劑用于增強聲動力治療并降低腫瘤轉移
將檢查點阻斷(如PD1/PD-L1)與傳統臨床治療相結合往往產生副作用和較低的腫瘤治療效果。同濟大學張坤、徐輝雄和中國科學院上海硅酸鹽研究所陳雨團隊合作報告了一種利用納米增敏劑去增強聲動力治療(SDT)并將其和檢查點阻斷免疫治療相結合的腫瘤治療模式。
實驗使用的納米增敏劑(HMME/R837@lip)的所有成分均已獲得臨床批準。其中,作為載體的脂質體將聲敏劑(血卟啉單甲醚(HMME))和免疫佐劑(亞米喹莫特(R837))進行共同包裹。實驗利用多個腫瘤模型證明了這種增強的SDT與抗PD-L1結合后可以誘導抗腫瘤反應,不僅可以阻止原發性腫瘤的生長,還可以防止其向肺部轉移。該聯合治療策略還可提供長期的免疫記憶功能,以防止腫瘤的復發。
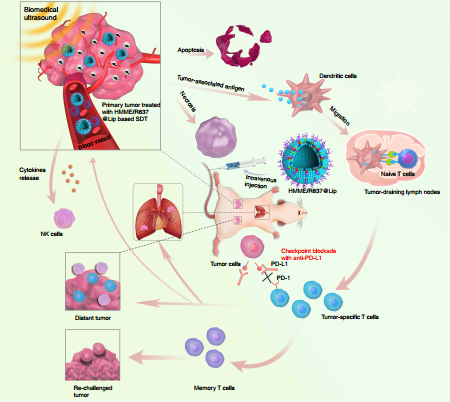
Wenwen Yue, Kun Zhang, Huixiong Xu, Yu Chen. et al. Checkpoint blockade and nanosonosensitizeraugmented noninvasive sonodynamic therapy combination reduces tumour growth and metastases in mice. Nature Communications. 2019
https://doi.org/10.1038/s41467-019-09760-3











