腫瘤微環(huán)境(TME)具有失調(diào)的生物合成中間體(過表達(dá)的過氧化氫、葡萄糖和乳酸等)以及特殊的理化性質(zhì)(低氧、低pH和高谷胱甘肽等)。因此,開發(fā)具有腫瘤微環(huán)境響應(yīng)性的智能診療試劑有望為腫瘤特異性治療提供優(yōu)勢(shì)。其中,納米金屬有機(jī)框架(nMOFs)具有優(yōu)異的結(jié)構(gòu)可設(shè)計(jì)性和功能多樣性,極具腫瘤特異性治療潛力。
中科院寧波材料所慈溪醫(yī)工所吳愛國團(tuán)隊(duì)近年在nMOFs催化醫(yī)學(xué)研究取得了系列成果,相關(guān)工作發(fā)表在Nano Lett. 2019, 19, 8, 5674-5682,Small2018, 14, 1801851(封面文章),Nano Res. 2020,13, 273-281等期刊。近日,該團(tuán)隊(duì)系統(tǒng)討論了nMOFs介導(dǎo)的酶促反應(yīng)用于腫瘤特異性催化治療,相關(guān)工作以“Navigating nMOFs-Mediated Enzymatic Reactions for CatalyticTumor-Specific Therapy”為題,以Minireview形式發(fā)表在Materials Horizons,并選為近期該期刊Outside BackCover。
本文系統(tǒng)論述了基于nMOFs的腫瘤特異性催化治療的設(shè)計(jì)策略,包括具有模擬酶活性的nMOFs、天然酶功能化的nMOFs和納米酶功能化的nMOFs。作者歸納了具有過氧化氫酶(CAT)、過氧化物酶(POD)和氧化酶(OXD)等固有模擬酶活性的nMOFs,主要包括鐵基、銅基、錳基、鈷基和鈰基nMOFs。總結(jié)了天然酶,如葡萄糖氧化酶(GOx)、過氧化氫酶(CAT)、乳酸氧化酶(LOD)和氯化物過氧化物酶(CPO)等功能化的nMOFs及其在腫瘤特異性催化診療領(lǐng)域的應(yīng)用。對(duì)納米酶(鉑納米酶、金納米酶和錳納米酶)功能化的nMOFs及其特異性催化治療應(yīng)用進(jìn)行了歸納。
該綜述有望推動(dòng)nMOFs在納米技術(shù)甚至其他領(lǐng)域的進(jìn)一步創(chuàng)新,為新一代催化納米藥物的開發(fā)策提供思路,并助于促進(jìn)納米催化醫(yī)學(xué)的發(fā)展。
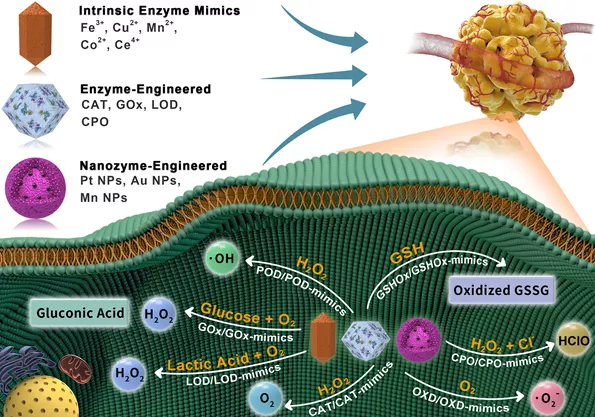
Scheme 1.nMOFs介導(dǎo)的酶促底物轉(zhuǎn)換用于腫瘤特異性催化治療

鐵基nMOF
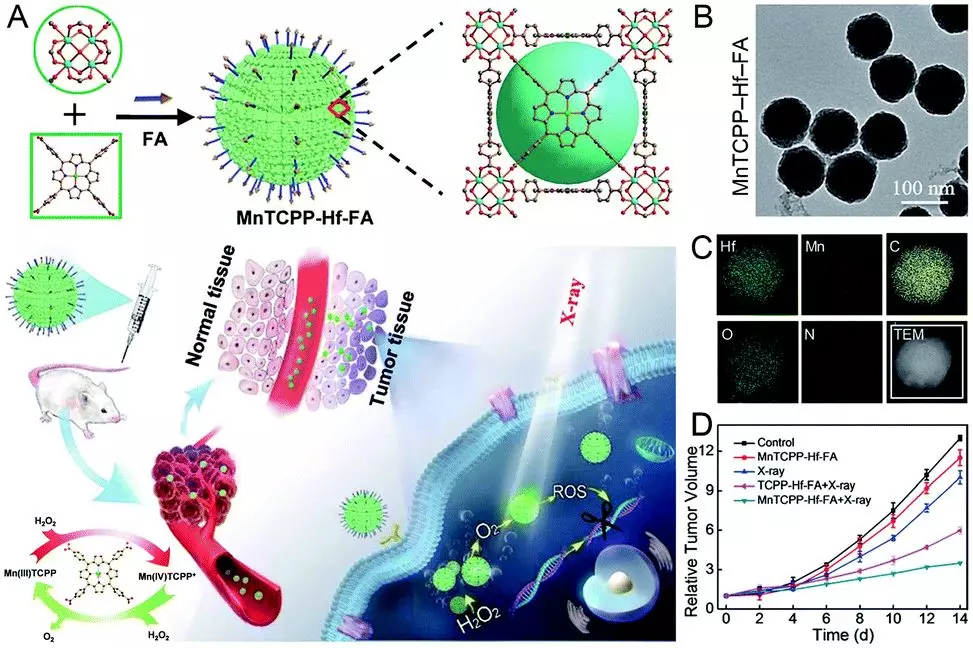
錳基nMOF
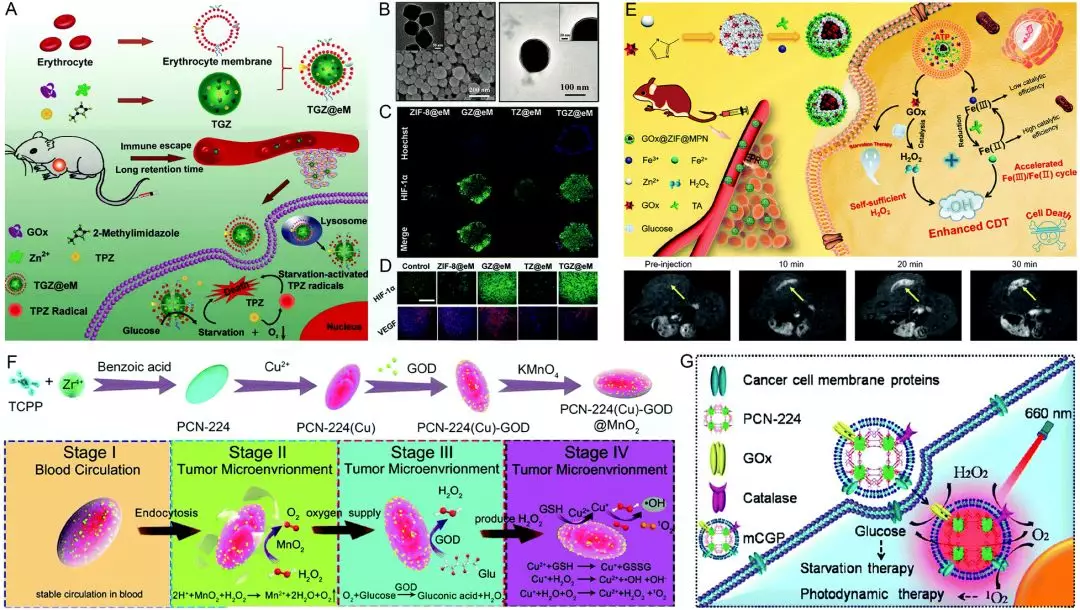
葡萄糖氧化酶工程化的nMOF
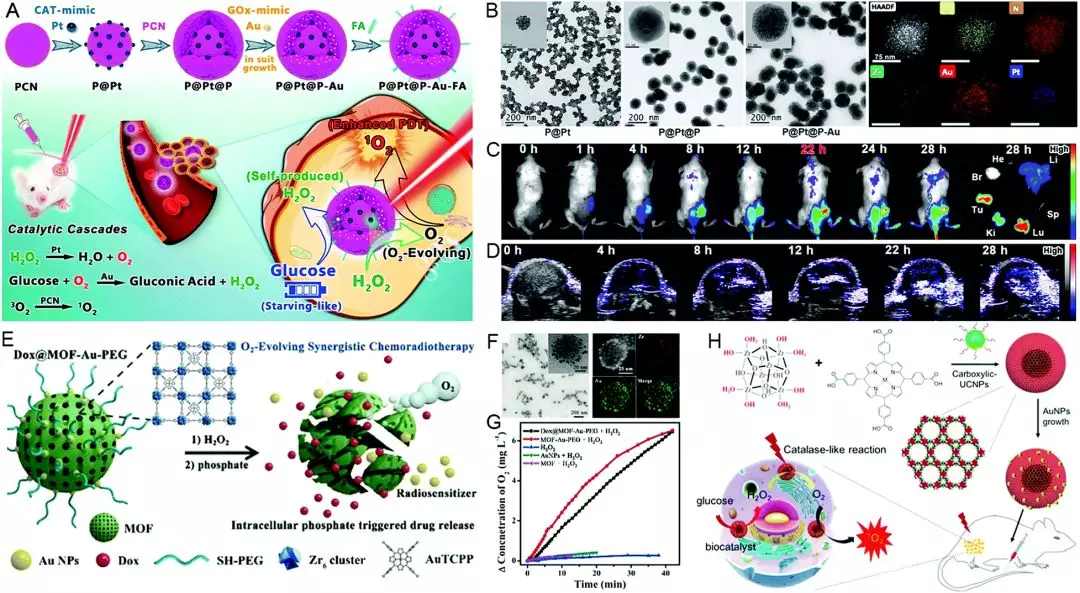
超小型金納米酶工程化的nMOF
參考文獻(xiàn):
Chuang Liu, et al. Navigating nMOF-mediated enzymaticreactions for catalytic tumor-specific therapy. Mater. Horiz., 2020,DOI:10.1039/D0MH01225D
https://pubs.rsc.org/en/content/articlelanding/2020/MH/D0MH01225D#!divAbstract











