葉酸受體(FR)是介導葉酸及其衍生物內吞的糖基磷脂酰肌醇連接膜糖蛋白。已在人體中鑒定出兩種膜結合的FR異構體(FR-α和FR-β),均顯示出與葉酸的極高結合親和力并有效促進葉酸的細胞內運輸。在許多人類癌癥中已經觀察到FR-α的表達上調,并且FR-α的高表達水平通常與晚期組織學侵襲性相關。FR-α高表達在人類癌癥中使其成為靶向遞送的理想候選靶點。在過去的幾十年中,為治療,診斷和手術導航目的而針對FR-α做出了許多努力。不幸的是,目前還沒有一種藥物被批準用于臨床。
究其原因,為何該靶向分子在臨床表現不行?
成果簡介
鑒于此,復旦大學占昌友教授等人重新研究了血漿蛋白對FA功能化納米藥物體內命運的調節作用,重新探索了葉酸在體內的靶向能力。成果發表于ACS Nano雜志上。

剝奪靶向,還被捕獲
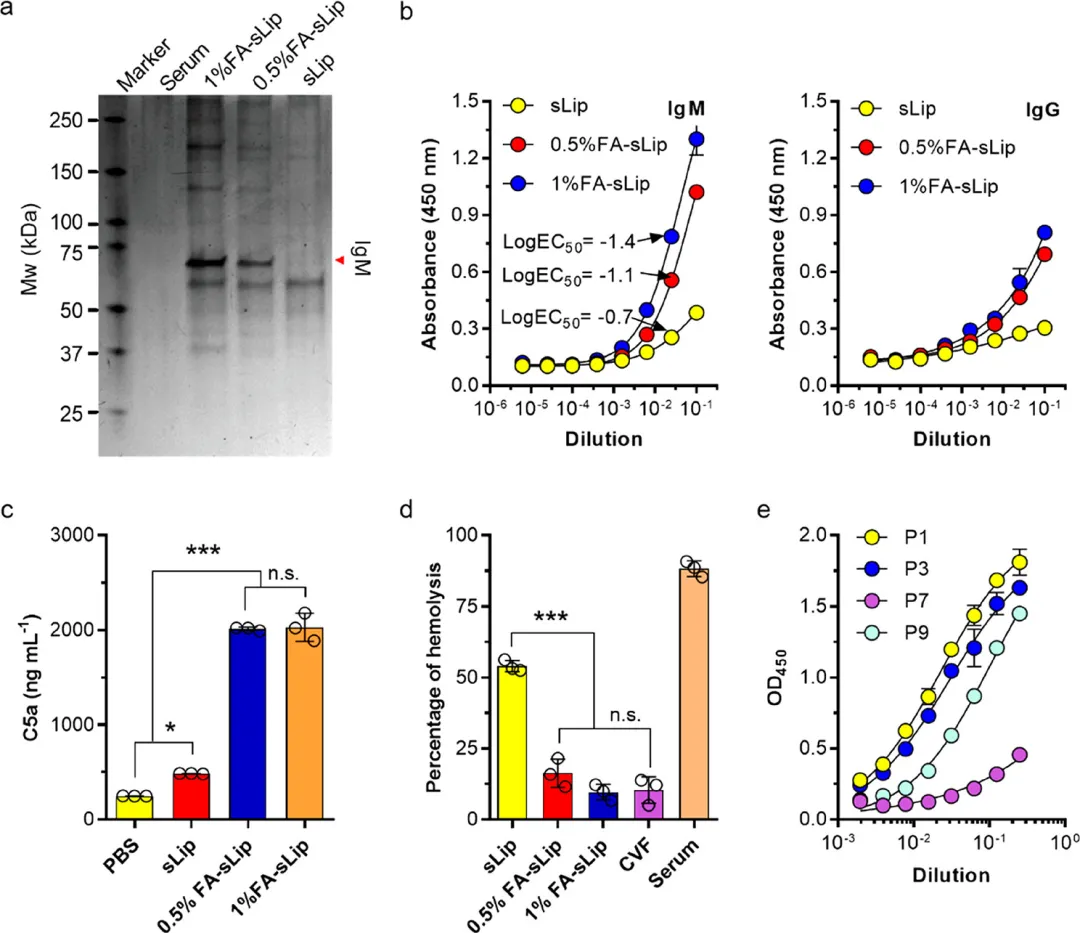
發現FA功能化會誘導脂質體表面被大量天然IgM吸附,這剝奪FA受體識別的能力,加速體內補體激活。與普通脂質體(不含FA)相比,FA功能化并不會增強脂質體在FR-α高表達腫瘤中的分布,反而會加劇巨噬細胞在腫瘤、肝臟和脾臟中對脂質體的捕獲。
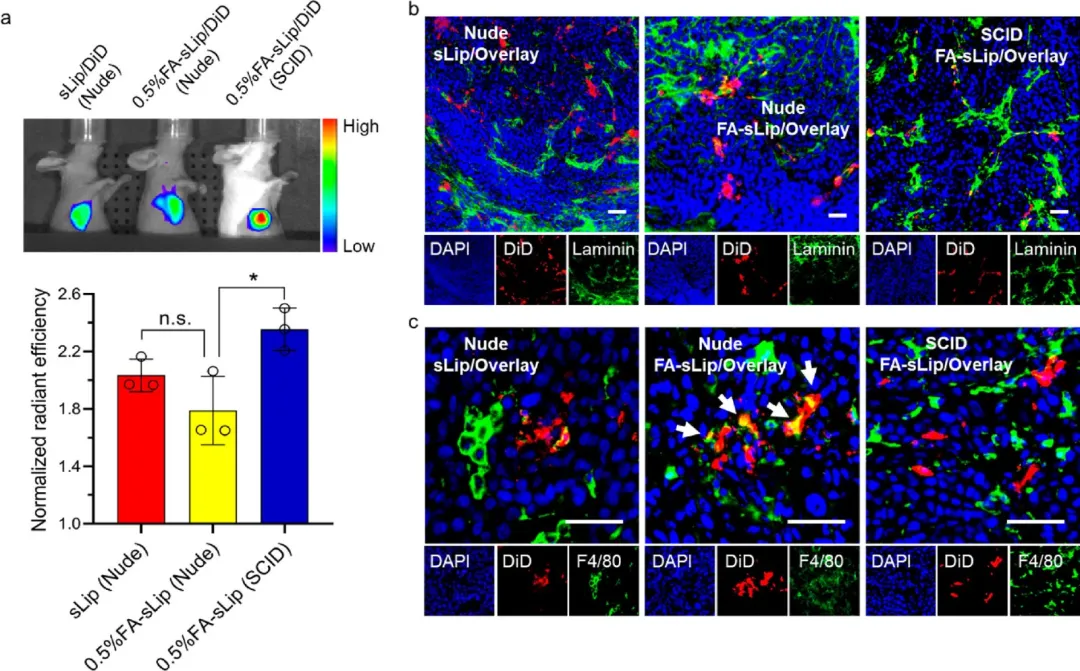
臨床應用需謹慎
此外,FA功能化聚合物納米粒子也容易受到天然IgM吸附的影響。這項工作強調了天然IgM在調節FA功能化納米藥物體內給藥中的關鍵作用。由于免疫紊亂和免疫球蛋白水平與癌癥患者的普遍聯系,FA靶向給藥系統的臨床應用需要格外謹慎。
參考文獻:
Huan Wang, et al., Interrogation of Folic Acid-Functionalized Nanomedicines: The Regulatory Roles of Plasma Proteins Reexamined. ACS Nano 2020.
DOI: 10.1021/acsnano.0c02821
https://pubs.acs.org/doi/10.1021/acsnano.0c02821











