基因編輯技術(shù)逐漸成熟,但是體內(nèi)遞送問題卻限制了其發(fā)展。治療性基因組編輯需要有效且有針對性的遞送方法。使用腺相關(guān)病毒遞送Cas9 mRNA可導(dǎo)致有效的體內(nèi)治療效果,但會引起持續(xù)的Cas9表達(dá)、抗Cas9免疫反應(yīng)和脫靶編輯。慢病毒載體已經(jīng)過工程設(shè)計(jì),可以傳遞瞬時(shí)表達(dá)的核酸酶,但缺乏其生物醫(yī)學(xué)功效的體內(nèi)證據(jù)。利用慢病毒載體打通體內(nèi)基因編輯治療最后一公里
于此,上海交通大學(xué)蔡宇伽教授等人于1月4日在Nature Biomedical Engineering上發(fā)表了關(guān)于利用慢病毒載體共遞送Cas9 mRNA和靶向血管內(nèi)皮生長因子A(Vegfa)的導(dǎo)向RNA,可預(yù)防小鼠中與年齡有關(guān)的濕性黃斑變性。

一次視網(wǎng)膜下注射工程化慢病毒可在視網(wǎng)膜色素上皮細(xì)胞中剔除44%的Vegfa,并使脈絡(luò)膜新生血管面積減少63%,而不會引起脫靶編輯或抗Cas9免疫反應(yīng)。用于瞬時(shí)表達(dá)核酸酶的工程化慢病毒可能構(gòu)成視網(wǎng)膜新血管疾病新療法的基礎(chǔ)。而在今日,該研究團(tuán)隊(duì)在Nature Biotechnoloy上發(fā)表了另一篇利用慢病毒載體來進(jìn)行基因遞送。

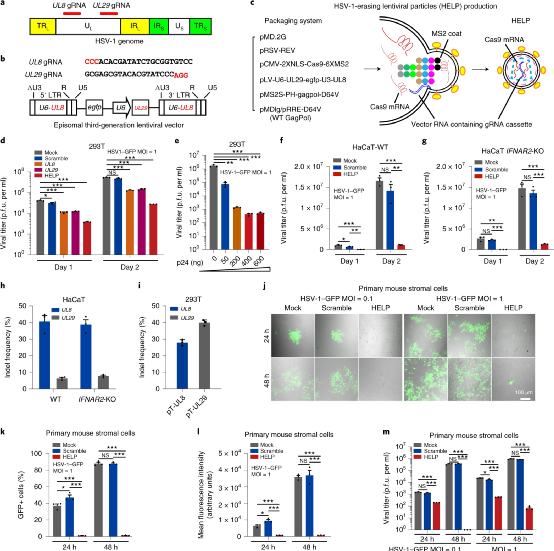
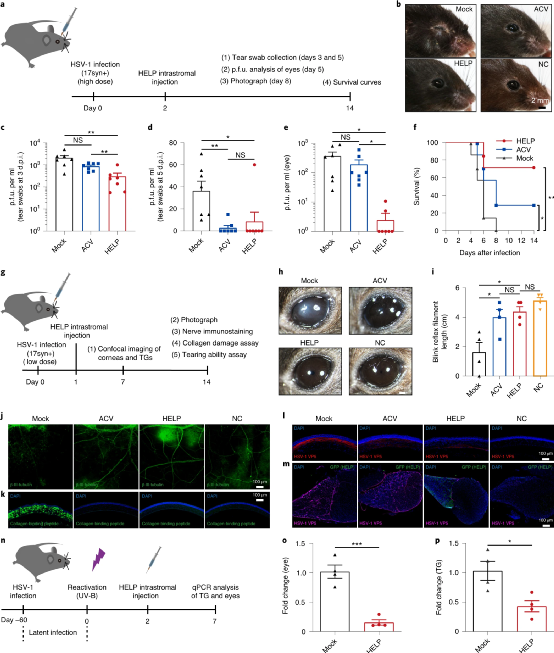
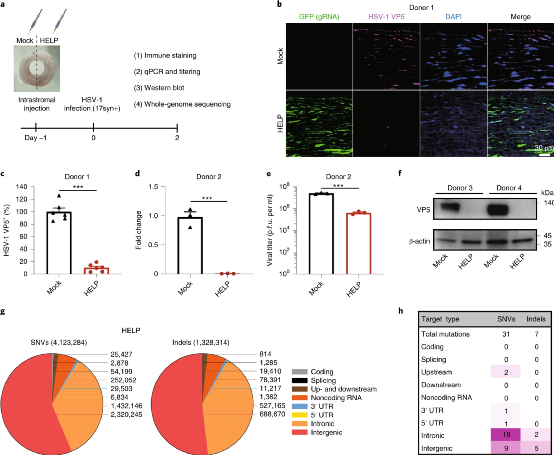
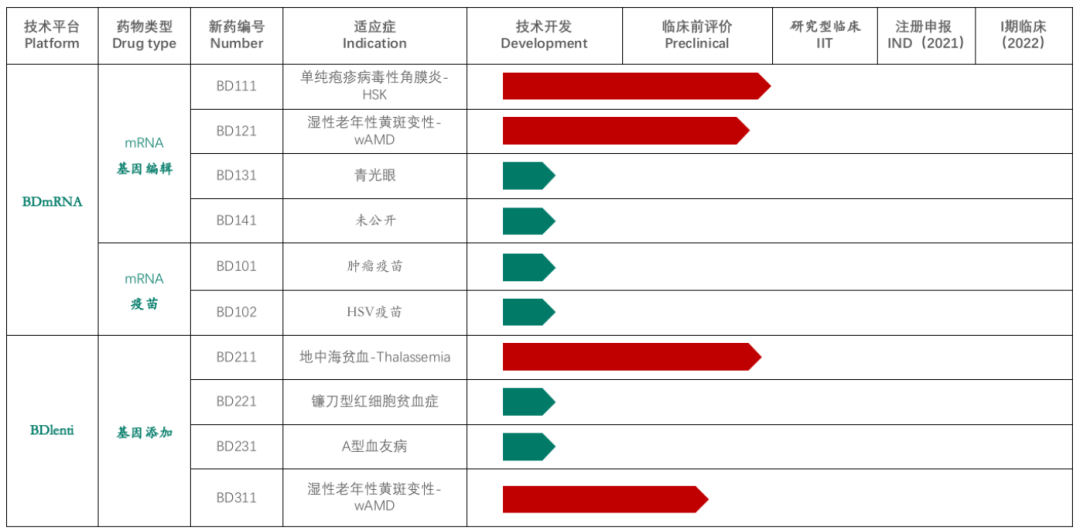
1型單純皰疹病毒(HSV-1)是導(dǎo)致傳染性失明的主要原因。目前對HSV-1的治療不能從三叉神經(jīng)節(jié)的感染部位或潛在的儲存庫中消除病毒。于此,上海交通大學(xué)蔡宇伽教授和復(fù)旦大學(xué)附屬眼耳鼻喉科醫(yī)院洪佳旭等人直接使用攜帶mRNA的慢病毒顆粒直接靶向HSV-1基因組,該顆粒同時(shí)傳遞SpCas9 mRNA和靶向病毒基因的導(dǎo)向RNA(稱為HSV-1消除慢病毒顆粒,稱為HELP)。研究人員表明,在三種不同的感染模型中,HELP有效地阻止了HSV-1復(fù)制和皰疹性基質(zhì)性角膜炎(HSK)的發(fā)生。角膜內(nèi)注射HELP后,角膜保持健康狀態(tài),HELP能夠通過從角膜到三叉神經(jīng)節(jié)的逆行運(yùn)輸消除病毒庫,而且來自HELP的Cas9表達(dá)僅在體內(nèi)持續(xù)3 d。此外,根據(jù)全基因組測序所示,HELP可抑制人源角膜中的病毒復(fù)制,而不會引起脫靶效應(yīng)。這些結(jié)果支持了HELP治療難治性HSK的潛在臨床效用。與腺病毒載體(AAV)相比,HELP能夠克服AAV的大小限制,并與SpCas9和gRNA共同包裝,從而在體內(nèi)有效消除HSV基因組,從而使病毒基因組的數(shù)量比大范圍核酸酶減少1-2 log。重要的是,HELP是基于mRNA的,對于Cas9沒有啟動子。相反,AAV構(gòu)建體可能會在不分裂的神經(jīng)元中持續(xù)很長時(shí)間,并且需要強(qiáng)大的啟動子才能有效表達(dá)核酸酶。因此,從臨床角度來看,它們伴隨著長期安全風(fēng)險(xiǎn)。圖|HELP可在治療和復(fù)發(fā)模型中治愈HSK從臨床角度來看,HELP可能首先應(yīng)用于因病毒復(fù)發(fā)和角膜移植術(shù)而導(dǎo)致的急性角膜穿孔或角膜移植失敗的患者。鑒于這種治療在最嚴(yán)重的HSK病例中顯示出的安全性和有效性,HELP還可以擴(kuò)展為早期HSK,作為通過消除角膜和TG中的病毒來治愈或預(yù)防HSK復(fù)發(fā)的一線選擇。圖|HELP消除人角膜組織培養(yǎng)中的HSV-1總之,該研究顯示了HELP的功效和安全性特征有力地支持了CRISPR對這些靶向HSV-1的慢病毒顆粒的進(jìn)一步臨床測試。另外,由于HELP的gRNA靶向病毒的基因組而不是人類基因組,因此可以加速臨床轉(zhuǎn)化。該研究還可能促進(jìn)針對其他病毒(例如人乳頭瘤病毒(HPV)或遺傳性疾病)的CRISPR治療藥物的開發(fā)。另外,蔡宇伽教授還為上海本導(dǎo)基因公司的聯(lián)合創(chuàng)始人,目前該公司的研發(fā)管線利用兩種技術(shù)平臺進(jìn)行開發(fā)基因編輯、基因疫苗等藥物。從圖中可見,BD111和BD121為最新兩篇研究論文所對應(yīng)的藥物。
1. Ling, S., Yang, S., Hu, X. et al. Lentiviral delivery of co-packaged Cas9 mRNA and a Vegfa-targeting guide RNA prevents wet age-related macular degeneration in mice. Nat Biomed Eng (2021). https://doi.org/10.1038/s41551-020-00656-y2. Yin, D., Ling, S., Wang, D. et al. Targeting herpes simplex virus with CRISPR–Cas9 cures herpetic stromal keratitis in mice. Nat Biotechnol (2021). https://doi.org/10.1038/s41587-020-00781-83. 本導(dǎo)基因:http://www.bdgenetherapeutics.com/index.html