
第一作者:Tuhin Patra
通訊作者:Frank Glorius
通訊作者單位:明斯特大學
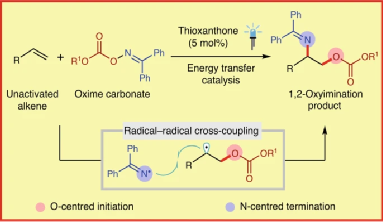
圖1. 碳酸肟、烯烴選擇性合成1-胺基-2-醇的示意圖
困難和挑戰
1,2-胺基醇結構是一種最重要的有機分子結構單元,在藥物、天然產物中非常重要。通常此類結構的合成需要對底物進行預先官能團化,而且為了保證所需的位點選擇性,每步反應中只能修飾一個官能團。
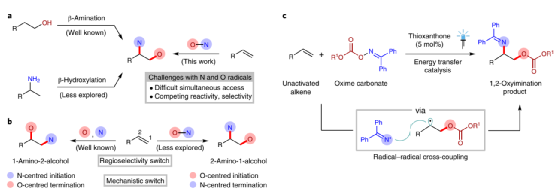
圖2. (a) 傳統的醇的β-胺基化(常見方法)、胺的β-羥基化(較為少見的方法)和烯烴直接雙官能團化方法的區別 (b) 烯烴合成1,2-胺基醇的不同種類 (c) 本文發展的選擇性1-胺基-2-醇合成。
有鑒于此,明斯特大學Frank Glorius等報道了一種無需金屬的光敏化方法學,能夠通過一步反應中將胺基、醇基修飾到烯烴雙鍵。該方法中通過碳酸肟同時作為氧中心、氮中心自由基,選擇性實現了對Sharpless胺羥基化選擇性的補充。該方法學以簡單易得的原料,在溫和的反應條件中進行。
反應體系優化
反應體系優化。以1-辛烯(1)、N-二苯甲基碳酸肟(2h)作為反應物,加入1 mol %光敏劑,在室溫乙酸乙酯中反應。考察了不同的光敏劑,常用的Mes-Acr純有機光敏劑、Ru基、Ir基光敏劑,其中[Mes-Acr](ClO4)、[Ru(bpy)3](PF6)2都未見目標產物生成,[Ir(ppy)2(dtbbpy)](PF6)、fac-[Ir(ppy)3]、fac-[Ir(dF(ppy))3]、[Ir(dF(CF3)ppy)2(dtbbpy)](PF6)分別實現了6 %、27 %、54 %、69 %的產率。同時,不含金屬的硫雜蒽酮(5)光敏劑同樣實現了71 %的產率,與Ir光敏劑的活性相比并沒有明顯降低。由于該有機光敏劑不含Ru、Ir等貴金屬,因此有一定的優勢。
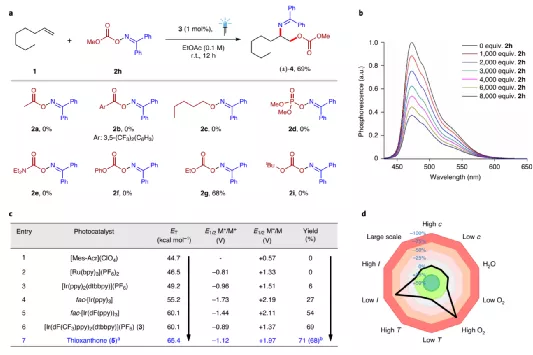
圖3. 反應體系優化
反應機理
機理驗證實驗。當反應中不加入光敏劑,在405 nm光激發過程中反應無法有效進行。該反應只有在365 nm光激發中才能夠進行;當反應中加入自由基引發劑(AIBN、DTBP、BPO),反應沒有目標產物生成;當在優化的光催化反應中加入TEMPO自由基捕獲劑,未見目標產物生成;當在碳酸肟底物中的碳酸基團上引入烯丙基,發現反應中生成含有環狀碳酸乙烯酯結構的亞胺產物。
基于此,作者提出了可信的反應機理。光敏劑通過和底物之間的三重態-三重態能量轉移過程,將底物分子激發,隨后底物中的O-N鍵均裂,生成基于碳酸酯的醇氧羰基自由基60、亞胺基自由基61,隨后醇氧羰基自由基和烯烴在端基位點反應,生成的碳自由基隨后和亞胺自由基進行自由基交叉偶聯生成目標產物。
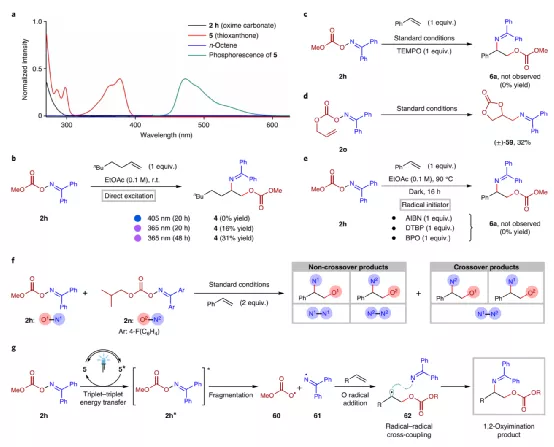
圖4. 反應機理
參考文獻及原文鏈接
Tuhin Patra, Mowpriya Das, Constantin G. Daniliuc & Frank Glorius*, Metal-free photosensitized oxyimination of unactivated alkenes with bifunctional oxime carbonates, Nat. Catal. 2021
DOI: 10.1038/s41929-020-00553-2
https://www.nature.com/articles/s41929-020-00553-2











