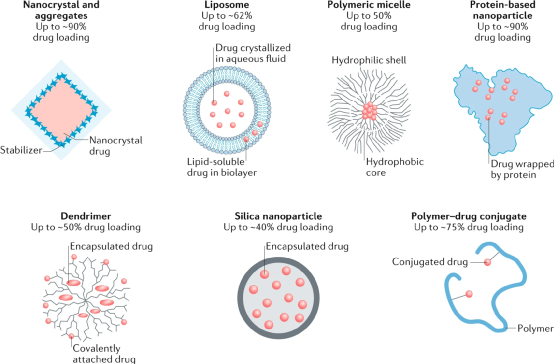
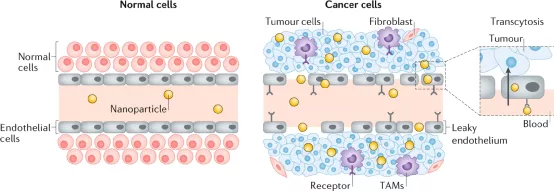
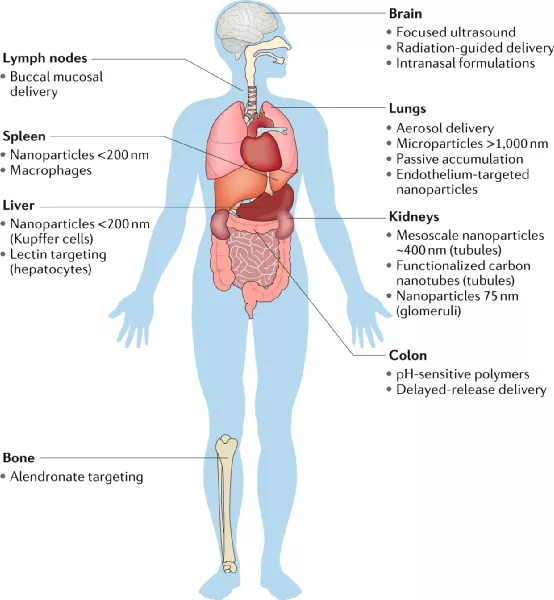
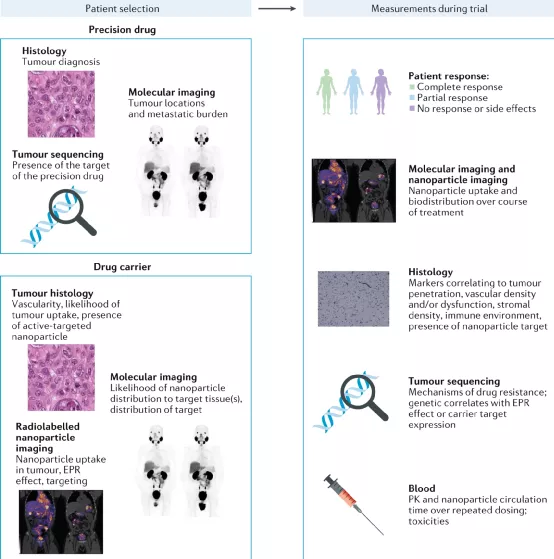
近年來���,隨著對癌癥的遺傳學理解、基因測序和生物信息學的發展�����,以及它們在藥理學和藥物開發中的應用����,精準醫學應運而生。精準醫學的核心原則是�����,可以利用基因�、環境和生活方式特征來確定每個患者的最佳治療策略。盡管這種方法在臨床腫瘤學中有著強大的應用前景�����,但轉化仍然受到一些問題的阻礙�����,包括藥物毒性和耐藥性。研究人員建議�,這些問題可以通過利用藥物遞送策略來緩解��,以擴展精準醫學的概念,并包括這些療法的位置(組織或器官)和時間(控制釋放)�����。美國紀念斯隆-凱特琳癌癥中心Daniel A. Heller等人在Nature Reviews Materials上綜述了近年來精準醫學領域的新進展����,闡明了現有策略的局限性,并提出了利用材料和藥物傳遞應用的潛在解決方案�。研究人員認為材料科學和癌癥生物學領域的結合可以改善患者的預后��。將藥物遞送策略納入藥物開發過程可能有助于改進療法的開發。具體而言����,抗癌藥可以成功地以治療劑量到達腫瘤����,使其靶標與之結合�,從而主動抑制促癌細胞機制,并避免在健康組織中產生可能導致劑量限制性毒性的作用�����。精準藥物中最大的一類是抑制位于信號通路關鍵節點中的酶(通常是激酶)。研究人員在本綜述主要針對此類精準藥物����,作為將靶向藥物與靶向藥物輸送系統整合的模型。研究人員對這些藥物的局限性進行了深入的討論���。像所有全身給藥的療法一樣,激酶抑制劑可引起多種副作用�。納米藥物可用于預防副作用��,例如神經毒性,血液學問題����,皮疹���,高血壓���,肝功能障礙�,肌肉骨骼問題����,胃腸道(GI)綜合征和心血管問題。納米醫學方法可用于將藥物遞送至腫瘤部位并避免正常組織的滲透�����。被動靶向允許適當大小的納米顆粒利用EPR效應�����,由于某些腫瘤類型的脈管系統滲漏���,從而增加了進入和保留的能力 使用納米載體表面上的受體結合部分進行主動靶向可通過跨內皮細胞的胞吞作用或通過直接結合在腫瘤細胞或腫瘤微環境中其他細胞類型(例如����,成纖維細胞或 腫瘤相關巨噬細胞)盡管主要關注激酶抑制劑�����,但本綜述也簡要介紹了其他種類的藥物,例如單克隆抗體,基于核酸的療法和免疫療法�。這些其他療法的分子特性可以受益于本文討論的獨特且重要的遞送方法���。這并不是對激酶抑制劑療法����,其他精準藥物或藥物遞送系統的全面綜述���;本文的目的是闡明精準藥物的主要改進領域�����、以及藥物輸送系統如何解決這些問題���。強調將藥物輸送與精準醫學聯系起來的整合研究的轉化價值�����。可以使用組織學、分子成像和腫瘤測序來選擇患者����,以進行診斷并確定患者是否適合使用精準藥物���。具體而言���,需要進行測量以確定納米顆粒被吸收到腫瘤中的可能性,包括組織學��、分子成像和(如果可能)對納米顆粒的放射標記形式進行成像���。在試驗過程中,與常規臨床試驗一樣��,需要監測患者的毒性和功效�。Manzari, M.T., Shamay, Y., Kiguchi, H. et al. Targeted drug delivery strategies for precision medicines. Nat Rev Mater (2021). https://doi.org/10.1038/s41578-020-00269-6