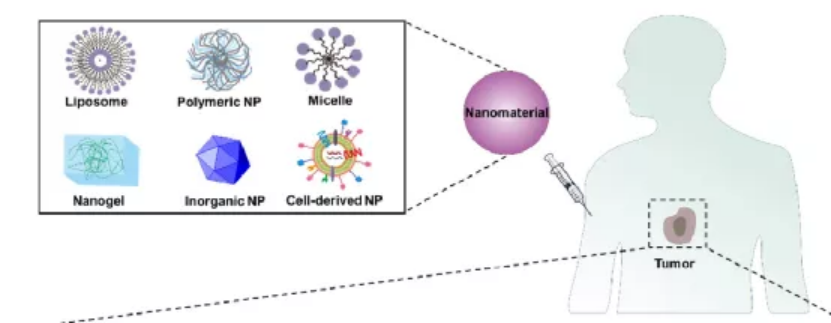
奇物論聯合納米人編輯部對2020內外重要科研團隊的代表性成果進行了梳理,今天,我們要介紹的是中國科學院院士,發展中國家科學院院士,國家納米科學中心趙宇亮研究員課題組。趙宇亮研究員主要從事納米生物效應分析與安全性研究,長期致力于推動納米科學與生物醫學交叉的科學前沿領域在我國的起步、形成和發展。創建了我國第一個納米生物效應與安全性實驗室;2006年領銜11個國家的科學家編著了納米毒理學領域的世界第一本教科書《Nanotoxicology》;2011年創建中國毒理學會“納米毒理學”專業委員會、2015年創建中國要學會“納米藥物”專業委員會等。趙宇亮研究員將放射化學原理發展到體外與體內超微量納米顆粒的定量方法學研究,揭示了多種無機納米材料、碳納米材料的體內分布圖譜,生物學效應規律,結構-效應關系,及其化學機制,在納米安全性和納米藥物領域做出了重要創新性貢獻。下面對趙宇亮院士課題組2020年的部分研究成果進行匯總,供大家學習交流。
1. Nature Biomed. Eng.:雙管齊下,有望突破腫瘤治療20多年研究瓶頸!
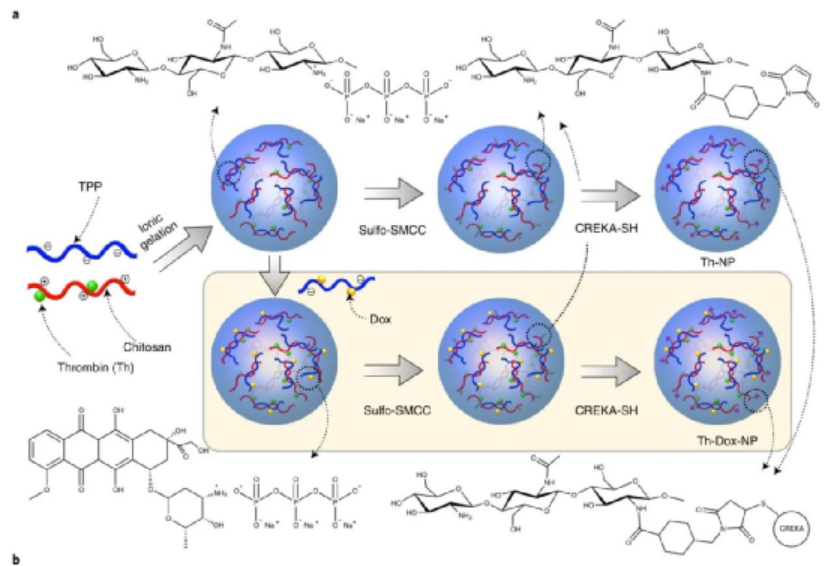
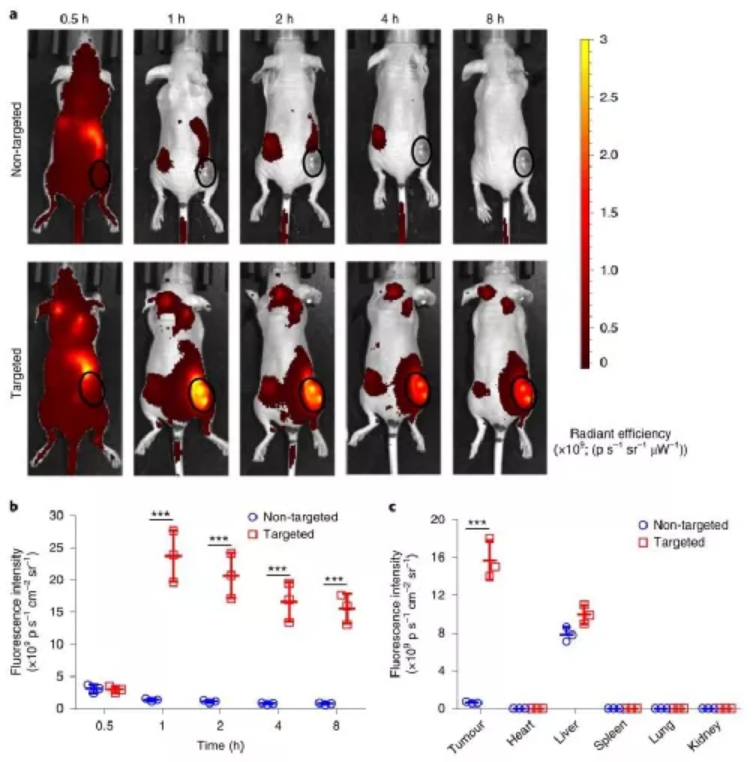
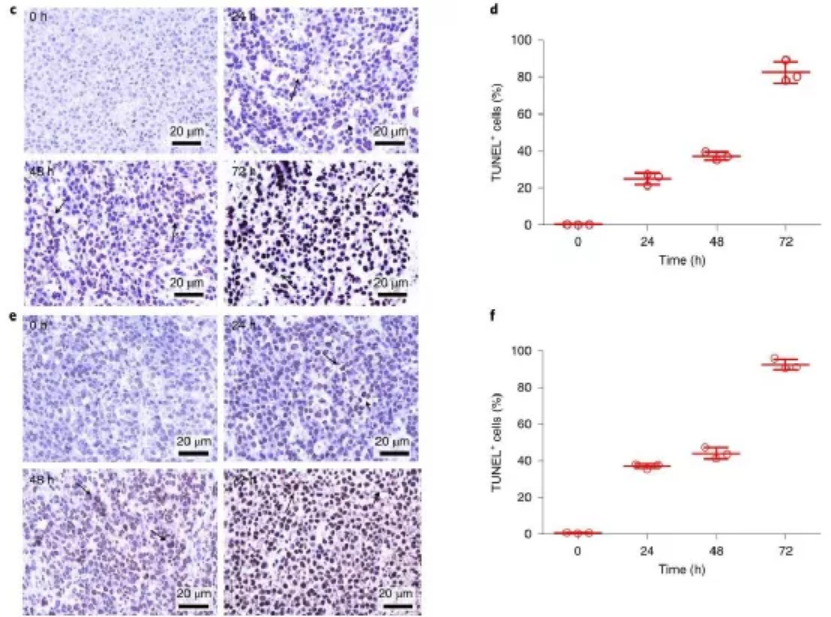
靶向促凝血劑誘導的腫瘤血管選擇性血栓閉塞是腫瘤治療的一個重要研究方向。對于急性血管事件,強烈的治療效果通常發生在幾個小時內,導致治療時間比大多數其他療法短得多。促凝血劑靶向腫瘤血管也可廣泛應用于治療多種癌癥,因為腫瘤供血血管通常具有相似的特征。此外,促凝血治療不太可能引起耐藥性(目前臨床癌癥治療面臨的最大挑戰之一)。腫瘤特異性靶向凝血誘導蛋白組織因子(tTF)的胞外結構域,是血液凝固的主要起始因子,已通過配體工程實現靶向多種腫瘤血管標志物。然而,雖然以腫瘤血管為靶點的功能性tTF在動物模型中已被報道能迅速誘導血栓形成,但臨床上仍缺乏成功的應用。腫瘤治療需要有效,安全地梗塞腫瘤血管的新策略。與tTF不同,凝血酶能夠通過直接激活血小板并在沒有其他輔助因子的情況下將循環的纖維蛋白原轉化為纖維蛋白而立即誘導血栓形成。因此,凝血酶應產生更有效和局部的閉塞作用,但腫瘤會復發。另外,腫瘤血管靶向/阻斷與細胞毒性藥物的結合可以更有效地抑制腫瘤的生長。但是,在先前的研究中,這兩種藥物是依序給藥的;這需要仔細選擇劑量和給藥計劃,因為次優的給藥和計劃可能導致兩種療法彼此相對。有鑒于此,國家納米科學中心聶廣軍研究員、趙宇亮院士、吳雁研究員等人開發了一種將凝血酶和化療藥物阿霉素(Dox)整合到單個納米載體中以同時殺死腫瘤的藥物共遞送納米系統。與兩種藥物的順序給藥相反,研究人員假設這樣的納米系統將通過同時影響腫瘤活力的兩個獨立方面(即腫瘤血液供應和癌細胞增殖)來引發協同效應,從而避免了與兩種單獨給藥的次優給藥和調度相關的問題。為了開發更經濟可行的納米載體,從而促進將血管阻斷療法轉化為臨床實踐,研究人員選擇了高分子大分子殼聚糖,由于其生物相容性和生物可降解性,被認為是一種可行的藥物材料,作為本研究中構建藥物共載納米系統的基石。采用離子凝膠法成功制備了殼聚糖基高分子納米粒(NPs),該納米粒對Dox(約17%)和人凝血酶(約78%)具有較高的包封率。將具有CREKA序列的腫瘤歸巢五肽移植到NPs表面,產生具有活性腫瘤組織靶向能力的NPs。CREKA肽能夠特異性地識別纖維蛋白-纖維連接蛋白復合物(腫瘤血管壁和腫瘤基質中獨特地過度表達)。由此產生的NPs在腫瘤部位表現出凝血酶的受控釋放,局部引發腫瘤內血栓形成,從而剝奪了腫瘤的營養,同時積累了Dox,通過腫瘤內擴散殺死腫瘤細胞,包括位于腫瘤邊緣的細胞。研究人員通過體內熒光成像評價納米載體的腫瘤靶向性和藥代動力學,結果表明,NPs在注射后主要被肝臟捕獲/清除,并通過腎臟迅速排泄,而靶向顆粒也顯示出相當大的腫瘤積累,而且相對于游離的Dox,Th-Dox-NP半衰期得以延長,其導致心臟組織中Dox濃度顯著降低(2.8倍)。這一發現是值得注意的,因為心肌病是游離Dox化療的劑量限制性副作用。Dox在腫瘤組織中積累的增加和心臟暴露的減少表明,Th-NP的封裝提高了Dox的治療功效。為了確定腫瘤中Th-Dox-NP的積累是否可以誘導血栓形成,研究人員用單尾靜脈注射Th-Dox-NPs(約2.30U凝血酶)對皮下接種MDA-MB-231乳腺腫瘤的小鼠進行了治療。注射后八小時,與對照組相比,腫瘤更明顯地被擦傷和變黑,表明由于血管破裂而積聚了血液。且其他器官均無明顯的可見的血塊,這表明Th-Dox-NP對腫瘤血管阻斷的高度選擇性。此外,Th-Dox-NP注射后72小時凋亡率達到92%。圖|th-Dox-NPs誘導血栓形成及腫瘤細胞凋亡在抗腫瘤實驗中,接受Th-Dox-NPs的小鼠的中位生存期提高了> 45.0d,超過接受Th-NPs的小鼠35.0d和接受Dox-NPs的28.0d。重要的是,腫瘤的完全消退僅限于Th-Dox-NP組,其中80%的消退腫瘤沒有再生長,表明聯合治療的效率大大提高。此外,在小鼠和兔子的肝癌模型中,表明了這種組合策略適用于廣泛的血管化腫瘤。在整個治療實驗中,未在小鼠中觀察到發病率或死亡率,這表明在目前的實驗條件下,Th-Dox-NPs不會引起嚴重的急性毒性。在動態高分辨率腦血流成像和各組織凝血情況等試驗中,均無造成明顯損傷。這些數據表明在目前的治療條件下Th-Dox-NP的長期安全性。這項研究為基于凝血的腫瘤治療的進一步發展打開了一扇門,盡管在該領域進行了超過二十年的研究,但在該學科中幾乎沒有令人鼓舞的進展。因此,研究人員著手將阻斷劑與其他細胞毒性藥物結合起來,以對腫瘤治療和動物生存產生更持久的影響。為了實現這一目標,本文探索了通過將兩種藥物整合到一種可生物降解的納米載體中來運送具有化學治療作用的血管閉塞劑的可行性,在這種載體中,殼聚糖NP可以有效制備并易于修飾以用于藥物遞送,并降解為水和二氧化碳。與現有的聯合治療策略(依次使用阻斷劑和細胞毒性藥物)相比,該策略由于同時攻擊腫瘤的兩個不同方面(血液供應和癌細胞增殖)而更有可能產生協同效益。通過選擇性地將凝血酶和化療性Dox共同遞送到具有主動腫瘤靶向機制的腫瘤中來實現這一目標。且這種方法還規避了優化連續給藥治療劑的劑量和時間安排的挑戰。Li,S., et al. Combination of tumour-infarction therapy and chemotherapy via theco-delivery of doxorubicin and thrombin encapsulated in tumour-targetednanoparticles. Nat Biomed Eng (2020).https://doi.org/10.1038/s41551-020-0573-2
2. Science子刊:正交上轉換納米粒,兩種NIR光控制逐級激活靶向和治療
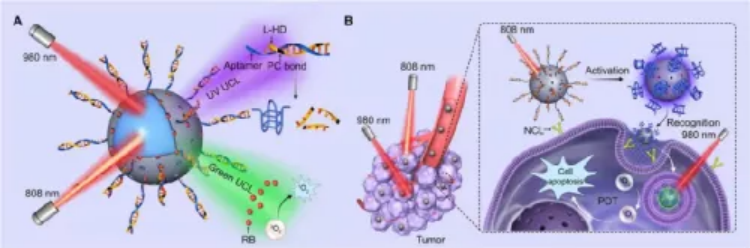
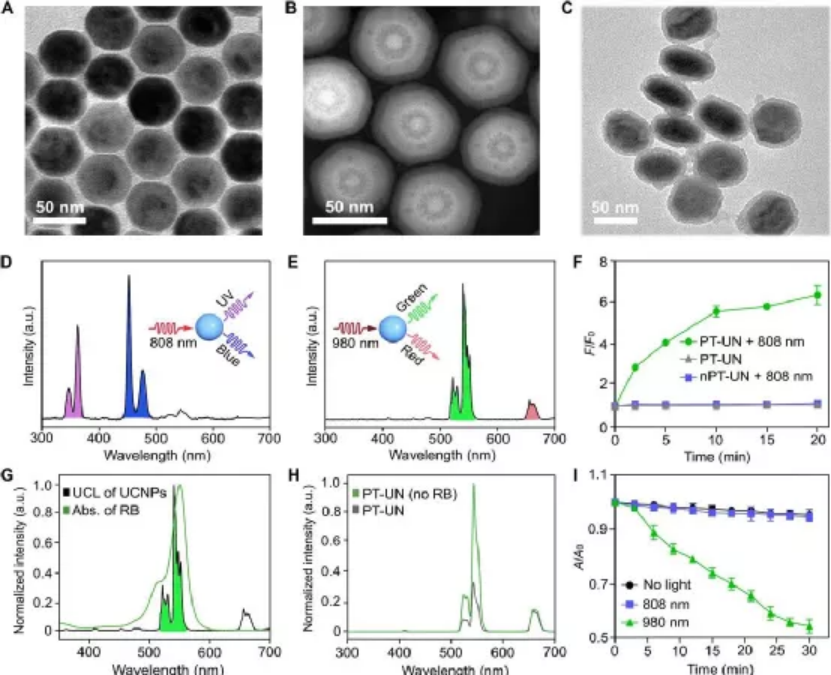
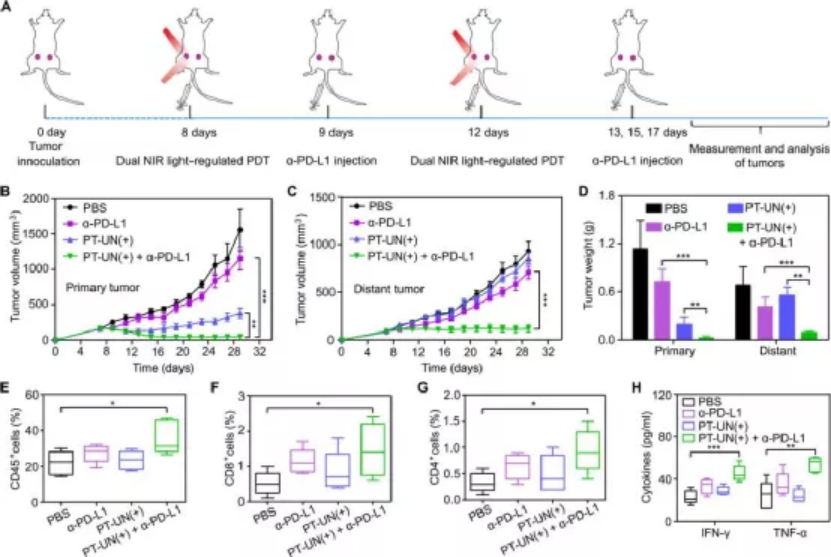
DNA正在成為一種高度可編程的構建模塊,用于設計具有特定功能的分子納米器件,包括傳感器、馬達和電路。這種DNA納米器件一旦與生物學接口,就可以完成多種任務,如生物傳感和成像、分子信息計算、可控的貨物運輸和釋放。特別是,最近的研究表明DNA納米器件可以作為智能藥物傳遞系統。這類設備的一個關鍵特點是,它們可以根據特定的生物信號執行細胞亞型定向傳遞。如趙宇亮院士等人在2018年發表在Nature Biotechnology上的關于DNA納米機器人作為癌癥治療劑的研究。盡管取得了一些進展,這些納米器件所識別的細胞表面受體并不是疾病細胞所獨有的,而在正常細胞中也有低水平的表達。因此,這種基于核酸適體的納米器件還可以與正常細胞上的同一靶點結合,從而產生on-target off-tumor效應。由于缺乏設計方法,基于適體的高時空選擇性納米器件的工程設計仍然是一個挑戰。事實證明,光是在空間和時間上精確調節化學和生物活動的誘人工具。例如,光遺傳學已對神經生物學和細胞生物學產生了變革性的影響。有鑒于此,國家納米科學中心李樂樂研究員、趙宇亮院士等人提出了一種利用近紅外光控DNA納米器件的設計概念方法,該方法可提高生物識別和腫瘤治療的時空選擇性。即采用正交上轉換納米技術,利用深部組織可穿透的近紅外(NIR)光實現對DNA納米器件的預期調節,從而實現高效的PDT,提高腫瘤特異性。此外,納米器件與免疫檢查點阻斷療法的結合通過促進細胞毒性T細胞的腫瘤浸潤,在荷瘤小鼠中引起協同效應和遠端效應。研究人員選擇一種適體,該適體可識別在各種癌細胞表面上過表達的核仁素(NCL),以證明該設計。如圖1A所示,納米器件(PT-UN)是通過在正交UCNPs表面上控制可紫外光激活的適體模塊(L-Apt)和PSs組成的。L-Apt是通過將適體與包含商業上可光裂解的2-硝基芐基接頭(PC接頭)的互補鏈(L-HD)雜交而設計的。在這種雙重狀態下,適體對NCL的識別能力受到抑制。UCNP充當光調節器,分別將兩種不同波長(808和980 nm)的NIR光分別轉換為正交UV和綠色上轉換發光(UCL)。在808 nm輻照下獲得的UV UCL可使PC鍵發生光解作用,并在所需的時間和位置釋放適體,而在980 nm輻照下獲得的綠色UCL則可以激發PS產生細胞毒性ROS。靜脈注射后,PT-UN可以在808 nm NIR光介導的局部觸發下特異性結合腫瘤細胞表面的NCL,然后在980 nm NIR光照射下產生ROS誘導腫瘤細胞凋亡。如何實現對兩個不同的近紅外光(808和980 nm)響應而發射正交UCL?研究人員設計了核-多殼的納米上轉換結構為:NaGdF4:Yb,Er@NaYF4@NaYF4:Yb,Tm@NaYbF4:Nd@NaYF4。核部分將Er3+/Yb3+共摻雜在其中,以在980nm激發下產生綠色發射。第一殼層為無任何摻雜劑的NaYF4,可防止能量在兩個發光區域之間遷移。第二和第三殼層的Tm3+/Yb3+和Yb3+/Nd3+共摻雜,實現808 nm激發時的紫外線發射。此外,在最外層生長NaYF4殼層,以最大程度地減少表面淬滅效果最后,還在UCNPs上涂上中孔二氧化硅殼,以在外表面修飾L-Apt,并在介孔中加載玫瑰紅(RB)光敏劑。體內外試驗表明,正交調節賦予納米器件時空控制的生物識別能力,增強了腫瘤特異性,并具有強大的抗腫瘤作用。此外,該納米器件還產生了免疫原性腫瘤微環境,顯著提高了免疫檢查點阻斷治療的效果。本研究設計允許將近紅外光敏劑賦予基于UCNP的納米光敏劑的生物認知能力,從而能夠以高時空精度遠程控制腫瘤靶向,因此能夠在正確的時間和地點觸發ROS的生成。本研究強調了UCNPs與DNA納米技術集成在精密PDT中的潛力。
3. Biomaterials:放射治療腹部腫瘤會引起胃腸道損傷?石墨二炔納米放射防護劑來解決!
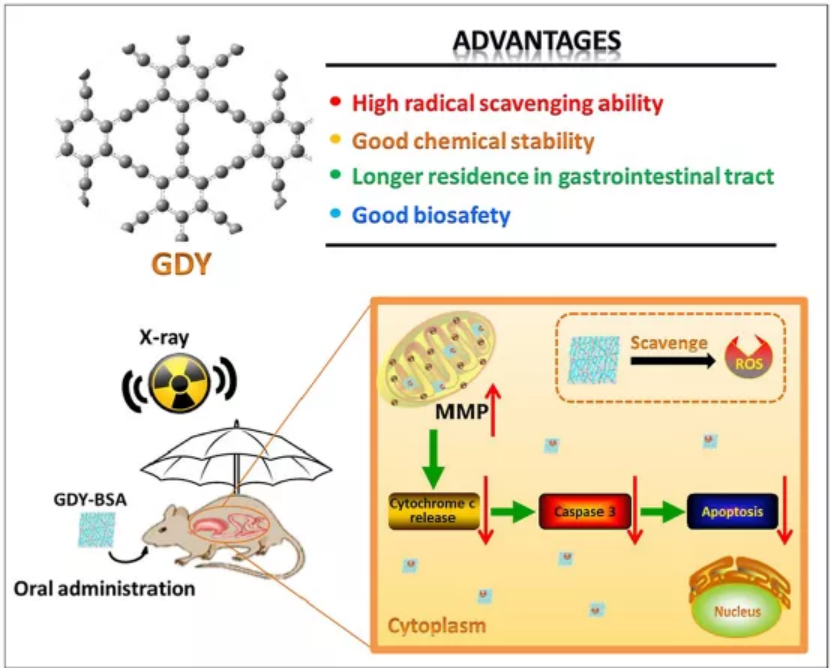
在用放射治療鄰近胃腸道組織的腹部腫瘤時,X射線照射對胃腸道的毒性是一個重要的臨床問題,它不僅使這些腫瘤得不到確定的治療劑量,而且還會引起厭食、腹痛、腹瀉和便血等一系列胃腸道疾病,從而嚴重降低了患者的治療效果和生活質量。因此,胃腸道放射防護劑的研制至關重要。然而,商品化的胃腸道放射防護劑在臨床上還很少見。有鑒于此,中國科學院大學趙宇亮、中國科學院高能物理研究所谷戰軍、中國科學院青島生物能源與過程研究所黃長水等人制備了牛血清白蛋白(BSA)修飾的石墨二炔(GDY)納米粒子(GDY-BSA NPs),并首次研究了其胃腸道放射防護性能。1)GDY納米材料具有清除自由基能力強、在胃酸條件下化學穩定性好、在胃腸道內滯留時間較長、口服生物安全性好等獨特優勢,為其作為胃腸道放射防護劑提供了有利的前提條件。2)體外實驗結果表明,GDY-BSA NPs能明顯減輕照射后胃腸道細胞的DNA損傷,提高細胞存活率。3)體內實驗結果表明,GDY-BSA NPs能顯著減輕小鼠放射性腹瀉、體重減輕和胃腸道組織病理損傷。4)此外,還深入研究了GDY-BSA NPs的胃腸道放射防護機制,表明GDY-BSA NPs能有效抑制活性氧(ROS)誘導的細胞凋亡信號通路,從而減少胃腸道細胞凋亡。本研究首次將GDY-BSA NPs應用于減輕放射性胃腸道損傷,不僅促進了新型胃腸道放射防護劑的開發,而且對利用納米藥物治療胃腸道疾病具有良好的指導意義。JianiXie, et al. Graphdiyne nanoradioprotector with efficient free radical scavenging ability for mitigating radiation-induced gastrointestinal tract damage, Biomaterials, 2020.https://doi.org/10.1016/j.biomaterials.2020.119940
4. ACS Nano:WO2.9-WSe2納米放射增敏劑用于局部腫瘤消融和檢查點阻斷免疫療法
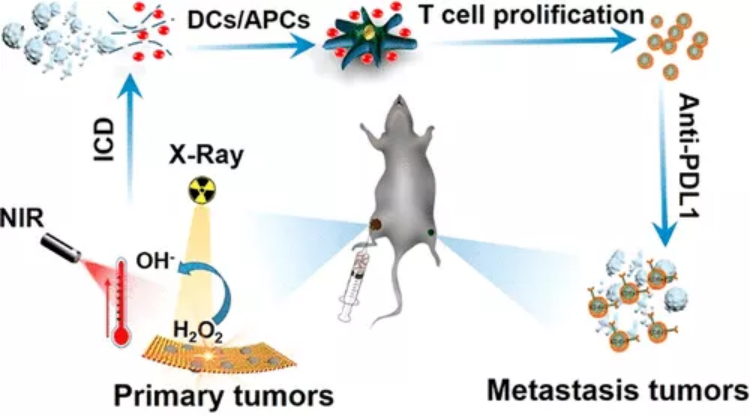
放射治療(RT)在實際應用中往往存在靶外副作用,對缺氧腫瘤微環境(TME)和遠處轉移無效。針對這些問題,中國科學院大學趙宇亮、谷戰軍和劉向峰等人提供了半導體異質結結構的WO2.9-WSe2-PEG納米顆粒,以實現協同RT/光熱療法(PTT)/檢查點阻斷免疫療法(CBT),以增強抗腫瘤和抗轉移效果。1)基于具有高Z元素的異質結納米顆粒,此納米系統可以在X射線照射下催化TME中高表達的H2O2生成非氧依賴性活性氧,從而進一步誘導免疫原性細胞死亡。2)同時,此納米系統還能在近紅外輻射下誘導熱療,從而提高RT效果。結果表明,加入抗PD-L1抗體的CBT后,在溫和的溫度和低輻射劑量下,局部RT/PTT能有效消融局部腫瘤,抑制腫瘤轉移,防止腫瘤復發。綜上所述,此研究不僅提供了一種基于半導體納米粒子的放射增敏劑,而且為同時治療局部和轉移腫瘤的三聯療法(RT/PTT/CBT)提供了一個多功能的納米平臺。Xinghua Dong, et al. A Heterojunction Structured WO2.9-WSe2 Nanoradiosensitizer Increases Local Tumor Ablation and Checkpoint Blockade Immunotherapy upon Low Radiation Dose. ACS Nano, 2020.DOI: 10.1021/acsnano.9b08962https://doi.org/10.1021/acsnano.9b08962
5. Biomaterials綜述:納米醫學在基于巨噬細胞的癌癥免疫治療領域中的應用
國家納米科學中心趙宇亮院士和王浩研究員對納米醫學在基于巨噬細胞的癌癥免疫治療領域中的應用進行了綜述介紹。(1)腫瘤免疫治療能夠利用宿主的協同免疫系統對抗腫瘤。然而,腫瘤免疫逃避的多種途徑也會導致的免疫治療效果不佳。腫瘤相關巨噬細胞(TAMs)是浸潤在所有腫瘤中的白細胞的主要成分,它可以通過介導慢性炎癥、促進血管生成、抑制保護性免疫反應、支持遷移和靜脈內灌注等多種機制在腫瘤的發生、發展和轉移中發揮重要作用。TAMs靶向治療在臨床實驗中也取得了顯著的成功效果,其中的主要策略是利用小分子試劑和抗體。然而,TAMs靶向治療的進一步應用也遇到了療效及安全性有限的難題。納米材料可以提供多種方法來實現對免疫調節的控制,以放大免疫反應,最終提高治療效益和降低治療毒性。(2)作者在文中綜述了在臨床中應用于以TAM為中心的癌癥治療的相關藥物;重點介紹了靶向TAMs的納米藥物的最新進展;并就納米醫學如何發揮其優勢以實現時空可控的免疫調節進行了討論。Yong-Dan Zhao. et al. Nanomedicine Enables Spatiotemporally Regulating Macrophage-based Cancer Immunotherapy. Biomaterials. 2020https://www.sciencedirect.com/science/article/pii/S0142961220307985
6. Small:15年納米安全研究趨勢!
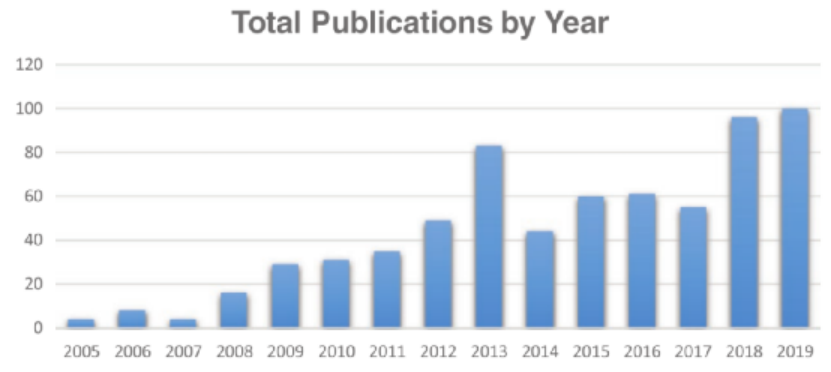
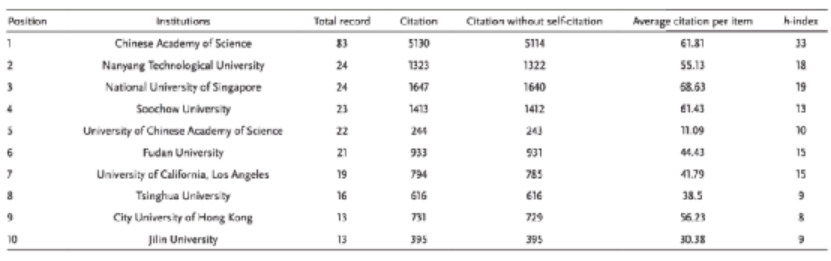
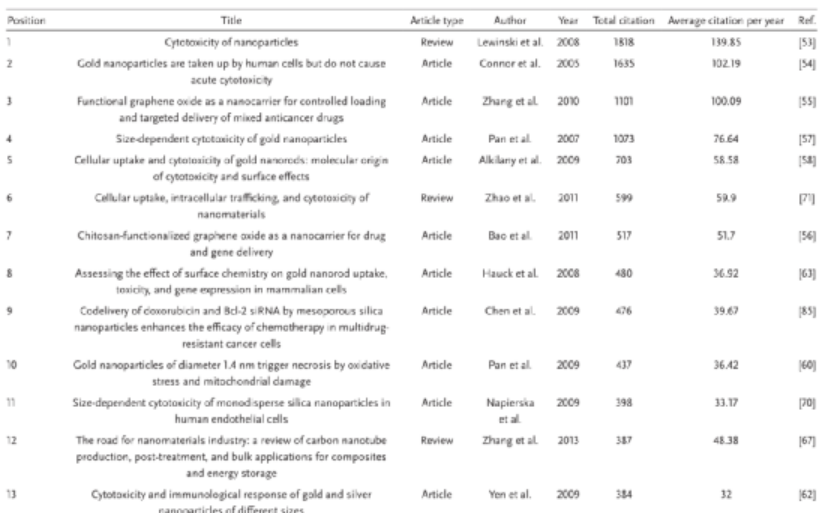
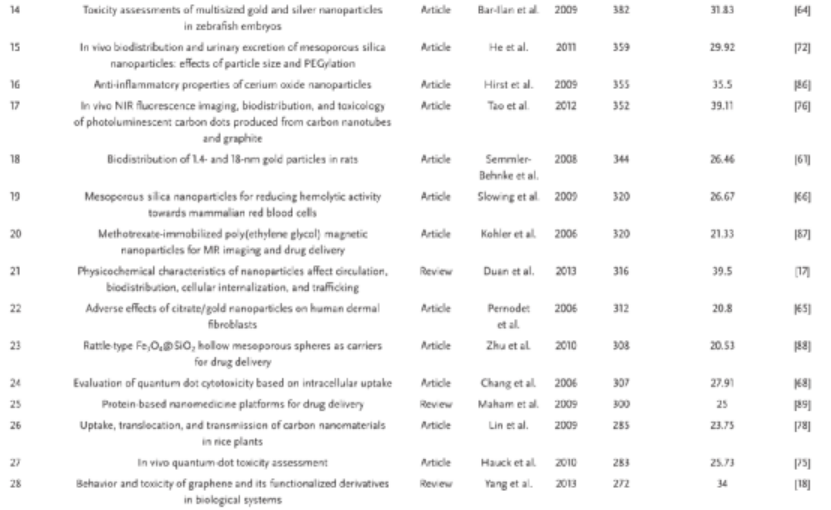
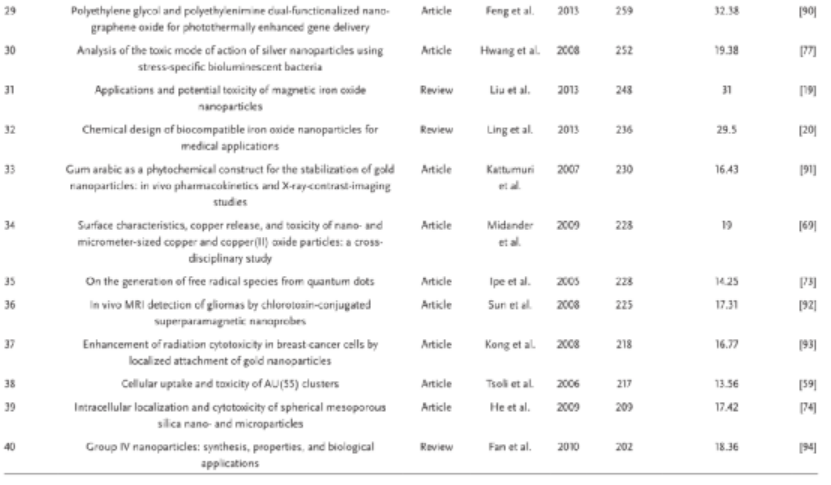
近年來,納米技術得到了飛速發展。根據全球行業分析公司最近的一份報告,到2024年,全球納米技術市場預計將達到1257億美元。顯然,各國都在致力于發展納米技術,這有助于改善甚至徹底改變許多科學和工業部門,如環境科學、信息技術、電子、能源和醫藥等。盡管納米技術帶來了諸多好處,但無所不在的納米材料在生物和生態方面的安全問題也引起了人們的廣泛關注。在2006年,趙宇亮院士領銜11個國家的科學家編著了納米毒理學領域的世界第一本教科書《Nanotoxicology》。納米材料的特性使其極易與人類接觸,然而,到目前為止,人們對納米材料的毒性效應還沒有完全了解。我們必須確保廣泛使用的納米材料不會對人類健康和環境造成不良影響。因此,納米安全研究成為納米科學研究的熱點之一。 鑒于此,中國科學院國家納米科學中心趙宇亮院士、陳春英研究員、谷戰軍研究員等人借助文獻計量分析了15年來發表在Small雜志上關于納米安全領域的相關論文,并為未來的研究的方向提供指引! 到2020年1月10日為止,這15年來,Small期刊在納米安全領域共發表了675篇論文,占所有出版期刊論文(8107篇)的1/12。由Small發文量的圖可以看出,2013年達到了一個小高潮,這主要是由于2013年Small的一個特刊:納米毒性學 的發布。除此之外,總體而言,多年來發表的論文數量呈增長趨勢,這表明納米安全性正受到學術研究人員的越來越多的關注。特別是在最近的兩年中,出版物的數量突然增加,幾乎占總數的1/4。圖|從2005年到2019年,每年關于“納米安全”出版論文數量自Small創立以來,來自世界各地的許多大學或機構都為該期刊做出了貢獻,包括與納米安全相關的研究領域。在此,作者根據總發表量、引用量(總引用量)和h指數,列出納米安全領域最具生產力和影響力的十大國家和機構。如表1所示,中國以309篇和13 456次引用文獻居于榜首。緊隨其后的是美國,發表了209篇。表1. 2005年至2019年間論文數量和影響力前十的國家在機構方面,中國科學院是“納米安全”領域中最多產的機構,貢獻了83篇論文和5130篇總引文。南洋理工大學和新加坡國立大學的出版數量分別排名第二和第三。除了總出版物數量外,此處還顯示了代表出版物的生產率和引文影響的h指數。在Small過去15年中,科學研究人員最關注的“納米安全”論文方面,表3列出了被引用最多的40篇論文。其中32篇是研究文章,其中8篇是綜述。特別是,引用最多的論文(被引用次數為1818)是Drezek及其同事于2008年發表的綜述(Cytotoxicity of Nanoparticles)。該綜述總結了基于碳、金屬和半導體的納米材料的細胞毒性數據。下一篇被高度引用的論文是研究金納米顆粒毒性的研究論文,有1635次引用。 表3. 2005年至2019年之間40篇被引用最多的論文從這個結果中,可以看到,對于納米顆粒的生物安全性研究,金納米顆粒特別受關注,多達10篇高被引用的論文與金納米粒子毒性相關。除了金納米顆粒之外,銀納米顆粒,二氧化硅納米顆粒,氧化鐵納米顆粒,碳納米顆粒和量子點也引起了相當大的關注。 除了選擇納米材料類型之外,納米尺寸是研究影響納米顆粒毒性的一般因素種最廣泛的一種。幾乎所有的納米安全性研究都會強調尺寸對納米顆粒毒性分布的影響。除了大小以外,其他因素(例如化學組成,形狀,表面化學和功能化,表面電荷,劑量/濃度以及蛋白質電暈的形成)也被視為影響納米顆粒毒理學的因素。還有,納米顆粒暴露引發的機制包括內吞作用、細胞膜滲漏、氧化應激的產生、線粒體功能受損、凋亡/自噬、DNA損傷、壞死、生物降解產物、免疫反應(如細胞因子釋放)等,也是納米安全研究的熱點。研究納米顆粒的細胞內效應有助于我們更好地設計安全的納米材料。 然而,盡管體外研究的重要性,它不能復制體內系統的復雜性。因此,研究納米顆粒在體內的分布具有重要意義,它可以為納米顆粒毒理學提供更全面的信息。納米顆粒的命運,如在體內的生物分布、代謝或排泄,也在一些文章中涉及。 此外,從表3中可以獲得的另一個有用信息是用于納米顆粒毒性檢測的生物模型。細胞系(如人內皮細胞或真皮成纖維細胞)、全動物(如大鼠)、微生物(如細菌)、水生生物(如胚胎斑馬魚)和植物(如水稻植物)用于揭示納米材料的生物和環境危害。不同的科學模型用于解釋或預測真實物體/系統中納米顆粒的行為。通過使用各種模型可以幫助我們更好地理解納米顆粒在生物和生態系統中的行為。 還值得一提的是,總引文量通常隨著時間累積。作者通過年度平均因此次數進行排名發現,Drezek及其同事被引用最多的論文仍然排名第一,但是近年來的一些論文也出現在了前面,這表明其他科學家近年來也在關注這方面的研究。 此外,作者還利用Citespace軟件識別了從前100篇被引用最多的與納米安全性相關的論文得出的主要術語,如圖所示,正如所指出的,這些研究中最重要的術語是“納米顆粒”和“細胞毒性”。諸如金納米顆粒,銀納米顆粒,碳納米管,中孔材料,石墨烯/氧化石墨烯和氧化鐵納米顆粒的納米顆粒類型是公認的。此外,納米毒性影響因素(例如尺寸)和機理(例如氧化應激)也被認為是熱門話題。該結果部分代表了前100名最受歡迎的論文的研究趨勢。圖|在Small中有關“納米安全性”研究的前100篇高被引論文中認可的主要術語。盡管在納米安全性研究中已經取得了成就,但在這一領域的一些新方面也應予以重視。例如,多年來,出版論文集中于尺寸、形狀或表面化學對納米毒性的影響。這就需要回答一個問題:我們是否真的需要這么多其他研究來一次又一次地證明納米粒子可能引發例如與大小或與氧化應激有關的毒性?納米毒性/安全性研究應強調哪些關鍵因素? 早在2013年,研究人員就已經指出,納米顆粒(低于100 nm的顆粒)的測定仍基于常規的顆粒毒理學數據,尚未發現新的“納米特異性危害”。使用常規粒子的可用危害數據而不強調“納米特異性效應”,會使有限的資源集中于徹底了解納米顆粒的毒性。 6年后,盡管進行了廣泛的研究,我們仍然徘徊在自己的禁區。 另外,對納米粒子對生物或生態系統的長期和長期安全性研究仍然很少。納米粒子在工作場所或一般環境中的暴露通常持續數年。幾周的安全研究肯定還遠遠不夠。 最后一點就是,與納米安全有關的出版論文正在增加,而對納米安全研究的類型充其量是零散的。例如,當涉及納米材料的尺寸依賴性毒性評估時,應測試哪些尺寸以及多少尺寸?采用什么樣的生物學模型?我們是否應該同時測量靶向納米顆粒的器官和蓄積器官的細胞內/遺傳毒性?如果沒有具體的系統來說明這些風險,很難定義納米材料的安全使用。盡管如此,經濟合作與發展組織先前還是提出了一種納米材料測試指南:《人造納米材料測試指南》,但沒有像預期的那樣廣泛使用。因此,為更好地了解納米顆粒安全性,目前迫切需要基于廣泛接受的指南系統地測量納米顆粒毒性。 Zhu,S., et al., 15 Years of Small: Research Trends in Nanosafety. Small 2020, 16,2000980.https://doi.org/10.1002/smll.202000980
7. Nano Research:納米二氧化鈦會誘導肥胖?嚇得我趕緊看了一眼油浴鍋
隨著經濟的發展和飲食結構的變化,肥胖癥的患病率在世界范圍內正在迅速增加。在美國,肥胖的發生率為42.4%,在歐洲為12.8%,在中國為12%。流行病學研究表明,肥胖與許多慢性疾病有關,如2型糖尿病心血管疾病、非酒精性脂肪肝和癌癥等。肥胖的原因很復雜,涉及遺傳和環境因素及其相互作用。其中,高脂飲食是過去幾十年來肥胖癥發展的一個重要原因,其對腸道微生物的重新塑造已被證明和機體健康密切相關,如能量吸收、肝臟脂肪生成、脂肪積累和免疫反應等。近期,一些食品添加劑,例如聚山梨酯80和羧甲基纖維素,也被證明可以改變腸道菌群進而促進肥胖的發展。二氧化鈦納米粒(TiO2-NPs)已廣泛用于商業、環境和工業領域。二氧化鈦(TiO2)由于其高亮度和高折射率而常被用作食品中的白色素。最近的研究表明,將近36%-44%的食品級TiO2顆粒處于納米級別(<100 nm)。據估計成年人的飲食中每天攝入TiO2的量約1-2 mg / kg體重,而兒童由于飲食偏好對TiO2-NPs攝入的更多,每天約為5.5-10.4 mg / kg。另外,由于TiO2-NPs具有出色的光催化性能,因此也廣泛用于清潔水中,導致其在水中的濃度高達0.7-16 μg L-1。飲食和水中的TiO2-NPs會在腸道中積聚,導致DNA損傷,結腸中的炎癥細胞浸潤以及健康個體中某些血清代謝產物發生改變。然而,已報道的TiO2-NP的毒性研究主要集中在其對健康群體中的效應上,而很少關注其對慢性病群體的作用。TiO2-NPs會被添加于一些誘導肥胖的高脂食品中,例如巧克力、油炸食品和一些液體飲料(含量高達1%),但是TiO2-NP在高脂飲食誘導肥胖中的毒性作用尚未被研究。楊祥良課題組發現長期口服暴露于TiO2-NPs會增加腸道通透性和改變腸道微生物結構,而這些變化會誘導慢性炎癥并最終加劇高脂飲食誘導的肥胖。他們發現經口攝入的TiO2-NPs會增加小鼠的體重,肝臟和脂肪組織的重量,尤其是在高脂飲食的小鼠中。
進一步機理研究表明,TiO2-NPs引起結腸粘液層的破壞和肥胖相關微生物群的失調。因此,粘液層破壞與微生物群失調共同引起了低度炎癥,最終加劇了高脂飲食誘導的肥胖相比之下,在抗生素清除腸道菌群的小鼠中,TiO2-NPs加劇高脂飲食誘導炎癥和肥胖的現象則消失,表明腸道菌群對于TiO2-NPs誘導的炎癥和肥胖是必需的。所有結果都表明TiO2-NP在飲食誘導肥胖群體中的重要作用,并強調了重新評估納米粒對易感群體毒性效應的必要性。Xiaoqiang Zhu, et al. Long-term exposure to titanium dioxide nanoparticles promotes diet-induced obesity through exacerbating intestinal mucus layer damage and microbiota dysbiosis.https://doi.org/10.1007/s12274-020-3210-1除此之外,趙宇亮院士課題組2020年還發表了一些其它成果,在此不一一列出,感興趣的讀者可以網上搜索學習。趙宇亮,研究員,中國科學院院士、發展中國家科學院院士,國家納米科學中心主任。目前擔任Nano Today主編等職位。已在Nature Biotech., Nature Nanotech., PNAS, JACS, Angew. Chem. In. Edit., Anal. Chem.等期刊發表SCI論文500余篇,被引>4萬次,H-因子約108。獲中國、美國、日本、歐盟的授權發明專利26項。研究成果獲“國家自然科學獎”二等獎2項,TWAS化學獎,中國毒理學杰出貢獻獎等。