





下面,我們重點介紹Science雜志,今天新鮮出爐的又一個分子篩研究進展。

第一作者:Niklas Pfriem
通訊作者:Johannes A. Lercher, Yue Liu
通訊作者單位:慕尼黑工業大學
對于催化劑而言,調控催化位點附近的分子環境能夠提高催化反應活性,在分子篩材料中,水分子通過形成水合陽離子,同時骨架中的Al呈負電荷,因此構建了離子型環境。當分子篩骨架上含有高濃度Al原子,能夠形成密度較高的陽離子-陰離子對,形成較高的局域離子強度,為參與反應的有機分子提供了更高的化學勢,同時提高了帶電荷的過渡態穩定性,降低反應的能壘,提高反應的速率。作者在水相中考察了環己醇脫水反應,展示了這種方法能夠通過調控離子強度實現定量的提高反應速率。
背景
含有Br?nsted、Lewis酸性位點的網狀硅酸鹽(tectosilicate)在工業分離、吸附、催化等領域中得到廣泛應用,通常情況中引入分子篩中的酸性位點為+3價態,這種位點在孔道中通過電荷、偶極作用導致較強的場效應,但是這種效應難以實現定量化調控。通過詳細大量的研究表征,發現當四面體取代位點的濃度不超過一定濃度時,Br?nsted酸位點(BAS)對吸附、催化反應的酸性強度是確定不變的,同時分子篩較高的本征催化活性通常被認為來自孔道結構對過渡態的穩定作用。
在近期的相關實驗中驗證了這種過渡態的穩定作用,該反應在水存在條件中進行催化反應,反應中生成[H3O+hydr.],這種水合氫離子的催化活性比溶液相中的穩定性高兩個數量級。在分子篩的環境中,水合氫離子在空間上更加靠近,這種非常靠近的酸位點導致有機分子的活度系數增加,相當于溶液相中溶解了濃度更高的酸、堿、鹽。同時這種更高的活度系數導致有機分子之間的相互作用強度降低,從而導致有機分子從溶液相環境轉變為約束狀態的納米孔,導致分子篩孔道中限域的有機分子物理化學性質產生改變。
分子篩孔道中的反應活度提高歸結于化學勢的提高,提高的化學勢導致分子的過渡態能量變化值降低,從而導致更高的反應速率。此外,分子篩孔道結構的極性環境有效的改善了極性過渡態的穩定性。而且,分子篩中分布密度較高的水合氫離子進一步導致過渡態的穩定,能夠降低反應的能壘。
主要內容
這種分子篩環境改善了反應物分子的熱力學反應活性,同時立體限域結構導致特定的酸-堿性產生顯著改變。作者在BAS [H3O+hydr.]濃度為0.05~0.86 mmol/gMFI的H-MFI分子篩考察環己醇脫氫反應,從而考察合適的[H3O+hydr.]濃度實現最大程度上改善反應化學勢。
在環己醇脫水生成環己烯的反應中,該反應通過H3O+hydr.催化。在溶液相中,當環己醇濃度大于0.1 mol/L,反應速率與環己醇的濃度無關。在分子篩中BAS [H3O+hydr.]作為催化位點,當BAS位點濃度在0.54提高至0.36 mmol/gMFI,反應TOF提高6倍,反應活化能從161 kJ/mol降低至140 kJ/mol;當BAS位點濃度進一步提高值0.86 mmol/gMFI,反應TOF降低了60 %,反應活化能增加至158 kJ/mol。
相比而言,對于氣相反應(沒有水參與),比如正戊烷裂解、丙醇脫水反應,反應速率TOF值不隨BAS位點濃度改變。這個結果能夠排除了Al原子位點表現為T型結構、成對分布結構影響催化反應活性的可能性,進一步證明了分子篩中影響反應活性的關鍵原因是離子強度。
水對BAS位點的影響
在氣相催化反應過程中,BAS位點主要表現為共價修飾的羥基,分布在Si-O、Al-O之間的橋氧位點;然而在溶液相中,BAS位點的結構變為H3O+hydr.同時以離子形式結合在分子篩上。
同時相對于溶液相中均勻分布的H3O+hydr.,H-MFI分子篩中的H3O+hydr.位點分布在分子篩的孔道中,這種情況導致局部H3O+hydr.濃度非常高,而且濃度不會隨著稀釋而降低。作者通過定量分析,發現H-MFI分子篩中單位結構的H3O+hydr.濃度數目為0.3~5個,對應于0.1~1.6 mol/L(按照晶胞大小~5.2 nm3);0.4~6.4 mol/L(按照H-MFI的微孔體積~1.3 nm3)。這種較高的H3O+hydr.濃度導致較高的離子強度、H3O+hydr./底物在微孔中的競爭。
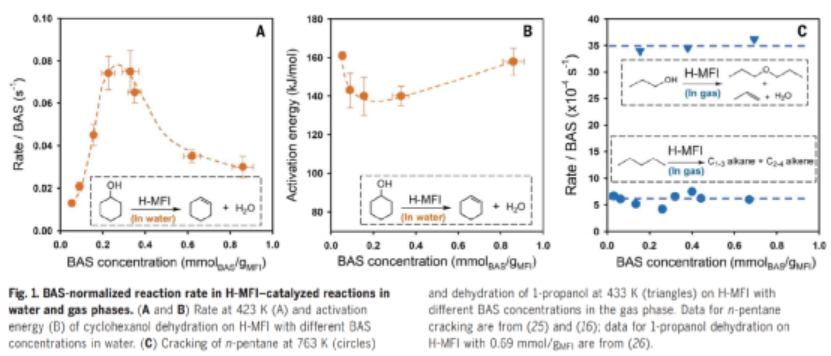
圖1. 水對H-MFI分子篩催化活性的影響
BAS位點濃度、離子強度、催化反應活性之間的關系
BAS位點對應于分子篩的離子強度變化,BAS位點濃度提高,分子篩的離子強度增加,同時離子強度提高導致催化反應速率提高,但是當BAS位點導致的離子濃度提高至> 2 mol/L,催化反應速率反而降低,這種效應與溶液相中的規律不同。
作者通過離子交換,發現當保持離子強度的同時將部分H3O+替換為Na+,反應速率并未降低,H-Na-MFI分子篩的催化反應TOF不變,因此驗證了催化反應速率的決定性因素是離子強度。
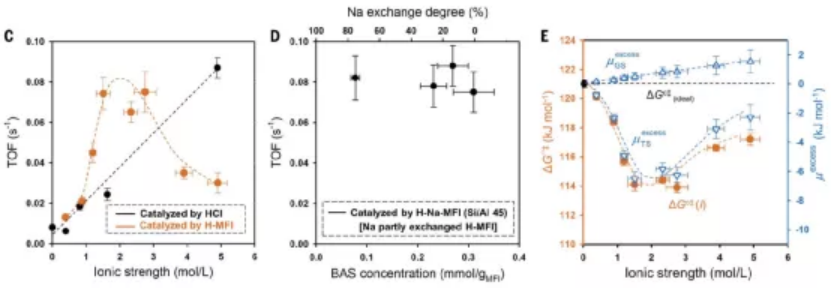
圖2. BAS位點濃度與分子篩的離子強度、催化反應TOF、反應活化能的關系
通過對H-Na-MFI (Si/Al 45) (Na+替換比例75 %)、H-MFI (Si/Al 200)兩種樣品對比,作者發現兩個樣品的BAS濃度分別為77、90 μmol/gMFI,但是離子強度分別為2.6、0.9 mol/L,TOF分別為0.082、0.021 s-1。因此,作者提出影響催化反應活性的原因主要來自于離子強度的區別。
作者進一步研究了分子篩在較高H3O+濃度條件中,催化反應速率反而降低的原因。當H3O+濃度較高,H3O+位點之間更加靠近,導致降低了環己醇的吸附。作者通過熱力學分析發現,更加靠近的H3O+位點導致焓變增加。當H3O+位點之間的距離達到0.8 nm(對應于液態環己醇的分子粒徑),導致環己醇分子在位點吸附過程中產生較強的vdW斥力,過渡態能量顯著增加,TOF降低。
總結
作者展示了限域在分子篩孔道中的H3O+hydr.通過體積效應、電荷兩個角度影響催化活性,H-MFI分子篩中H3O+hydr.表現為H+(H2O)8,結合在分子篩的位點上會與環己醇分子進行競爭性吸附,導致環己醇吸附位點處于相鄰H+(H2O)8之間,同時導致環己醇分子相互隔離;當H3O+hydr.濃度進一步提高,相鄰H+(H2O)8的距離縮減,導致反應速率反而降低。(但是,對于一些較小的分子,比如乙醇,并不適用這個規律,因為較小的分子能夠用于構建H3O+hydr.,比如形成(C2H5OH)(H3O+)(H2O)n)通過以上兩種作用,導致隨著H3O+hydr.濃度變化過程中,表現催化活性峰值。其中H-MFI分子篩的最高反應速率對應于相鄰H3O+hydr.的距離恰好容許一個底物分子。這種規律同樣適用于其他類型分子篩中,比如H-BEA分子篩。
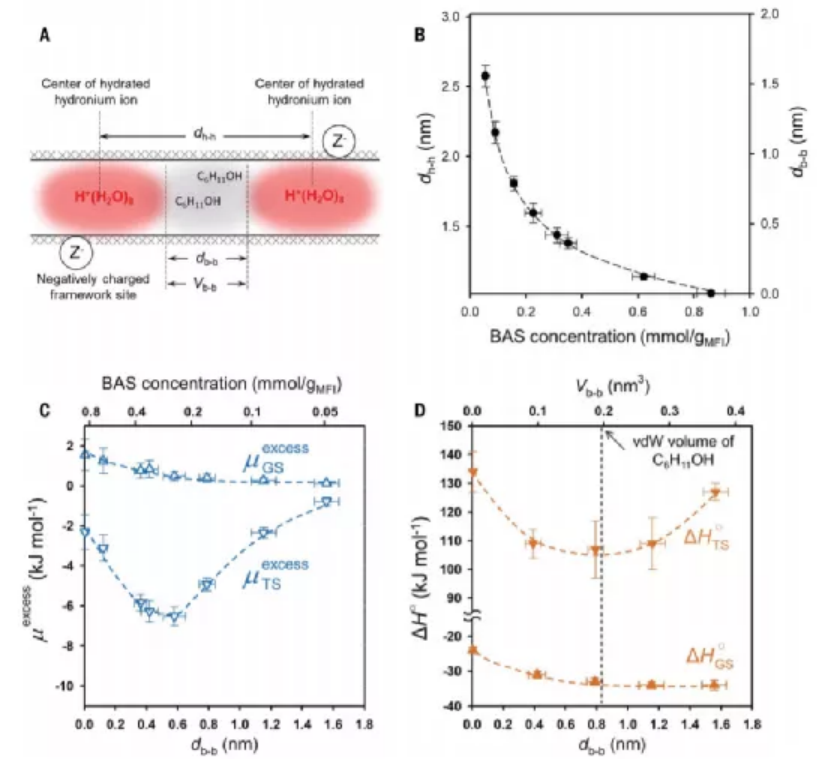
圖3. 分子篩中BAS間距對反應物反應性的影響
參考文獻:
Niklas Pfriem et al. Role of the ionic environment in enhancing the activity of reacting molecules in zeolite pores, Science 2021,
DOI: 10.1126/science.abh3418
https://science.sciencemag.org/content/early/2021/05/05/science.abh3418











