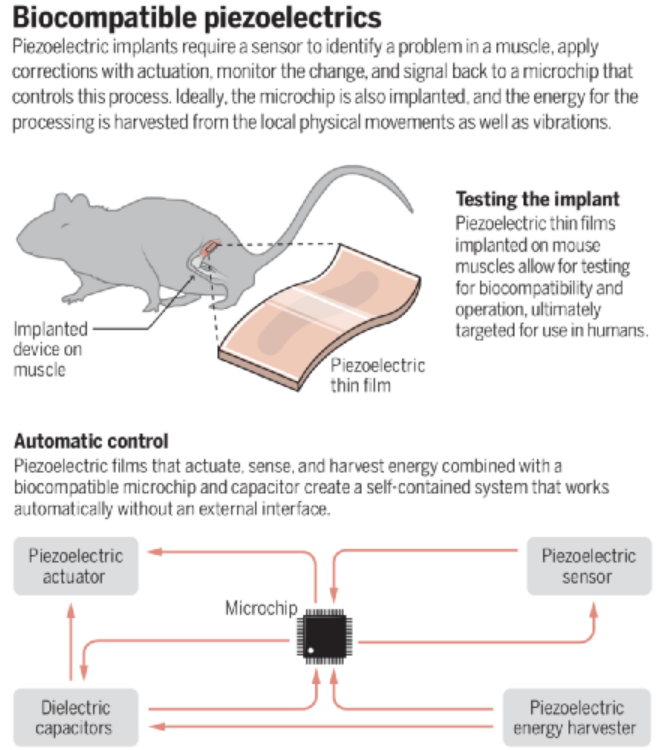
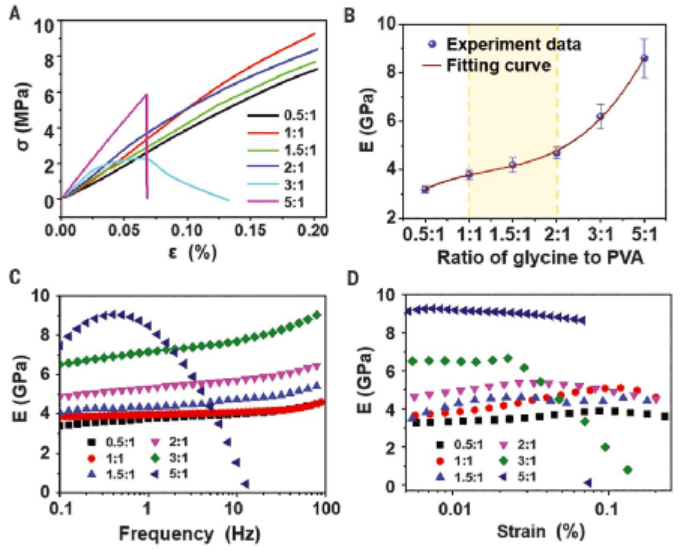
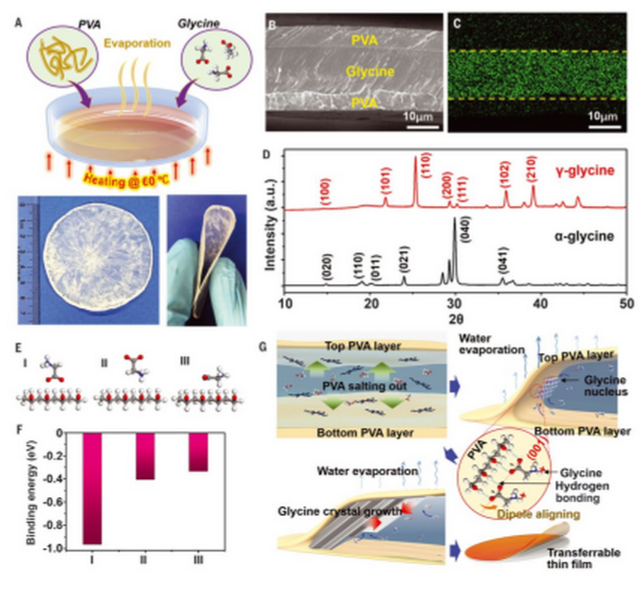
人體中的肌肉能夠提供人體運動所需要的機械力,人體不同器官的機械力能夠產生多種不同的運動形式(收縮和伸展、旋轉、彎曲)。當受傷或者遭受疾病,人體的肌肉可能無法正常工作,在嚴重的情況中甚至將致死。通過外科手術能夠解決此類問題,但是在一些比較嚴重的情況中無法完全克服。人工植入的生物相容器件能夠替代功能性喪失肌肉,但是需要檢測物理運動需求、從而在功能性喪失的肌肉位點施加合適的機械力。同時,這種器件能夠以自供電的方式驅動。生物相容性壓電材料能夠在體內將人體器官和組織的運轉情況進行傳感并且進行驅動管理器官和組織的運動,實現了通過壓電效應進行電能與機械能之間轉換。通過相鄰的離子鍵鍵長可逆變化產生隨著機械力或者電場變化的電化學偶極,這種變化過程導致形成壓電響應。而且人體中骨頭和肌肉中天然存在壓電材料,此類天然材料的蛋白成分為氨基酸,比如γ-甘氨酸、DL-丙氨酸等表現非常強的壓電響應信號。此外,聚二氟乙烯(PVDF)及其共聚物同樣能夠實現體內壓電響應效果。壓電材料是一類能夠在機械壓力與電荷之間進行可逆轉換,這種材料在傳感器、執行器、高精度電機等領域用處非常廣泛,有鑒于此,威斯康星大學麥迪遜分校王旭東等報道了發展一種簡單方法合成高晶化度的γ-甘氨酸晶體膜,將其修飾在兩層聚乙烯醇PVA之間。PVA能促進γ-甘氨酸的晶化取向,并且有助于沿著垂直于薄膜的方向形成極性軸(通過PVA-甘氨酸界面氫鍵作用)。因此,這種具有高度晶化度與取向性的薄膜實現了宏觀、穩定的壓電響應,同時這種薄膜材料是一種水溶性材料,能夠組裝為生物可降解壓電能量收集器件。由于該項研究的重要意義,以色列理工學院Shlomo Berger對該項研究的內容和意義進行總結與展望。壓電生物材料能夠實現在生物體中將“機械力學能”與“電能”耦合,在生物體內實現實時的傳感、執行、發電等多種功能集成,但是目前的研究中難以在大面積實現壓電材料相均勻排列,因此難以用在實際應用中。威斯康星大學麥迪遜分校王旭東等報道了一種新穎的生物相容壓電薄膜材料器件,能夠通過人體提供的能量驅動運動,具體的作者在實驗室進行老鼠體內實驗,驗證了通過電場驅動實現了準確的肌肉物理運動。作者發展了一種三明治結構自組裝多層結構,將晶化γ-甘氨酸組裝在兩層聚乙烯醇(PVA)之間,形成的異質結結構實現5.3皮庫/N、157.5×10-3 V/N的壓電效應,同時這種多層三明治結構的機械柔韌性比單純甘氨酸晶體提高了一個數量級。由于器件的材料由生物可降解材料組成,因此具有生物相容性、可降解性,能夠用于搭建生物可植入器件。作者發展了一種制備大面積生物相容性甘氨酸薄膜的方法,通過蒸發甘氨酸-聚乙烯醇混合溶液的方法,自組裝形成了大面積柔性甘氨酸壓電薄膜。在60 ℃中進行甘氨酸-PVA混合溶液加熱揮發溶劑固化的方法制備三明治結構甘氨酸薄膜,由于較低的界面張力,溶液能均勻分布在界面上形成均勻液膜,隨后在蒸發溶劑過程中,首先在邊緣位點開始晶化,隨后在30 min內實現薄膜完全晶化。隨后直接將薄膜從溶液表面剝離,就得到了均勻一體化的柔性三明治結構薄膜。SEM表征結果顯示,薄膜的厚度~30 μm,其中上下兩層PVA的厚度都~7 μm,甘氨酸晶化層的厚度~16 μm。甘氨酸的晶疇寬度~230 μm,長度達到厘米。通過XRD表征驗證得到晶化γ-甘氨酸,在21.8°、25.3°產生γ-甘氨酸的特征衍射峰,同時未發現其他晶相。此外在19.7°發現強度較低的寬峰,對應于PVA,說明PVA的晶化程度非常弱。對比實驗發現,當不加入PVA,相同條件中得到的甘氨酸主要為不具有壓電效應的α-甘氨酸。作者通過DFT計算,發現在PVA作用條件中,甘氨酸更容易形成γ-相的結構,同時晶化取向優先以沿著(001)方向進行晶化。這種壓電薄膜器件能夠用于體內監測心跳、呼吸、血液流動、眼內壓和顱壓,以及在人體內進行精確控制器官和組織的運動。此外,這種生物相容性體內器件能通過局部電場作用治愈受傷組織。這種體內壓電能量收集裝置能夠收集人體組織和器官的運動能量,將能量累積并且存儲于生物相容電容器,能夠控制釋放電能驅動壓電器件的工作。以往發展的控制藥物釋放作用的植入型芯片理論上能與壓電器件兼容,并且用于控制傳感器、執行器、電容器、能量收集等結構單元,通過這種植入型輔助器件的幫助,能夠逐漸解決肌肉功能性損失問題。而且這種修復過程能夠以自動形式進行,直至將肌肉的功能成功修復。這種植入式壓電器件以往能夠通過無線通訊方式實時收集信號、或者向微處理器中輸入操作指令,但是與體內植入微處理器之間的無線通訊面臨著難以穿透生物組織的問題,同時需要安裝較大的天線。同時,這導致其難以植入大腦、心臟、脊髓等容易受到輻射損傷的器官和組織。Shlomo Berger, Autonomous biocompatible piezoelectrics, Science 2021, 373(6552), 278-279DOI: 10.1126/science.abj0424https://science.sciencemag.org/content/373/6552/278Fan Yang, Xudong Wang et al. Wafer-scale heterostructured piezoelectric bio-organic thin films, Science 2021, 373(6552), 337-342DOI: 10.1126/science.abf2155https://science.sciencemag.org/content/373/6552/337