第一作者:Xu Qiu, Yueqian Sang, Hao Wu
通訊作者:焦寧, K. N. Houk
通訊作者單位:北京大學, 加州大學洛杉磯分校
主要內(nèi)容
合成化學一直以來都圍繞著構(gòu)建C-C鍵進行,但是目前合成C-C鍵的方法學仍具有較高挑戰(zhàn),發(fā)展構(gòu)建C-C鍵的方法能夠有助于發(fā)展有機合成、煤的氣化、石油裂解、聚合物降解、生物質(zhì)轉(zhuǎn)化等領(lǐng)域。芳基環(huán)狀結(jié)構(gòu)是惰性化學品分子的重要結(jié)構(gòu)單元,但是由于芳香性、較弱的極性,芳基環(huán)在大量反應(yīng)過程中沒有反應(yīng)活性。在過去的一些年間僅僅發(fā)展了少數(shù)幾種方法能夠進行惰性芳環(huán)C-C鍵切斷的方法,而且此類切斷C-C鍵需要苛刻的反應(yīng)條件中進行,以化學計量比的過渡金屬有機試劑或者酶催化方法同樣非常缺乏。
有鑒于此,北京大學焦寧、加州大學洛杉磯分校K. N. Houk等報道一種Cu催化芳烴開環(huán)反應(yīng)的方法學,該反應(yīng)能夠使用氧氣作為氧化劑打開芳烴的環(huán)結(jié)構(gòu),該方法學能夠?qū)⒎及贰⒎蓟鹚帷⒎蓟B氮、芳基鹵化物、芳基三氟甲磺酸、芳基三甲基硅氧烷、芳基羥肟酸、芳基重氮鹽等通過開環(huán)反應(yīng)轉(zhuǎn)化為烯基氰化物,這種反應(yīng)方法學能夠用于修飾多環(huán)芳烴,制備工業(yè)上非常重要的己二胺、己二酸。此外,作者在一些復(fù)雜有機分子的后期官能團化反應(yīng)、稠環(huán)化合物的修飾反應(yīng)中驗證了該反應(yīng)方法學的廣泛應(yīng)用前景。
背景
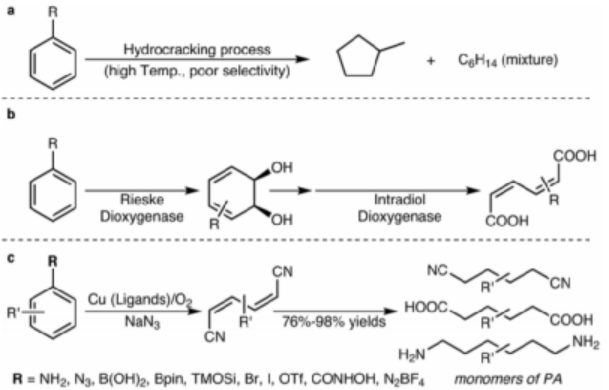
圖1. (a-b)經(jīng)典芳烴活化方法(c)本文發(fā)展的Cu催化芳環(huán)開環(huán)反應(yīng)方法學
歷史上苯是在200年前由Faraday發(fā)現(xiàn)的,隨后對芳環(huán)取代的相關(guān)研究得到很快的發(fā)展,但是與芳環(huán)C-C鍵切斷相關(guān)的擴環(huán)/開環(huán)反應(yīng)研究進展非常緩慢,工業(yè)上的石腦油(naphtha)加氫裂解處理苯的反應(yīng)需要在高溫中進行,生成甲基環(huán)戊烷和鏈狀飽和烴的混合產(chǎn)物。此外,雖然從苯出發(fā)制備C6合成子以及復(fù)雜結(jié)構(gòu)鏈狀分子具有較高的吸引力,目前仍無法在溫和條件中實現(xiàn)高效率和選擇性切斷芳環(huán)結(jié)構(gòu)。
在過去幾十年間,人們發(fā)展了幾種切斷芳環(huán)的方法學:
細菌催化。通過細菌切斷苯環(huán),經(jīng)過氧氣氧化,經(jīng)歷多步反應(yīng)將苯轉(zhuǎn)化為己二烯二酸,這種細菌催化過程難以進行模擬;
過渡金屬催化劑催化。哥倫比亞大學Gerard Parkin發(fā)展了Mo(PMe3)6催化活化氮雜芳烴、倫敦帝國理工學院Mark R. Crimmin等發(fā)展了N,N-雙齒配體穩(wěn)定的烷基Al(I)卡賓催化活化苯環(huán)。日本理化學研究所侯召民發(fā)展了三核Ti分子活化苯的方法;
卡賓、氮賓、亞磷基催化實現(xiàn)芳環(huán)的擴環(huán)生成7元環(huán)狀結(jié)構(gòu)。
除了以上三種方法之外,目前還沒有發(fā)展出能夠?qū)崿F(xiàn)切斷芳環(huán)C-C鍵合成鏈式產(chǎn)物的方法。
反應(yīng)設(shè)計
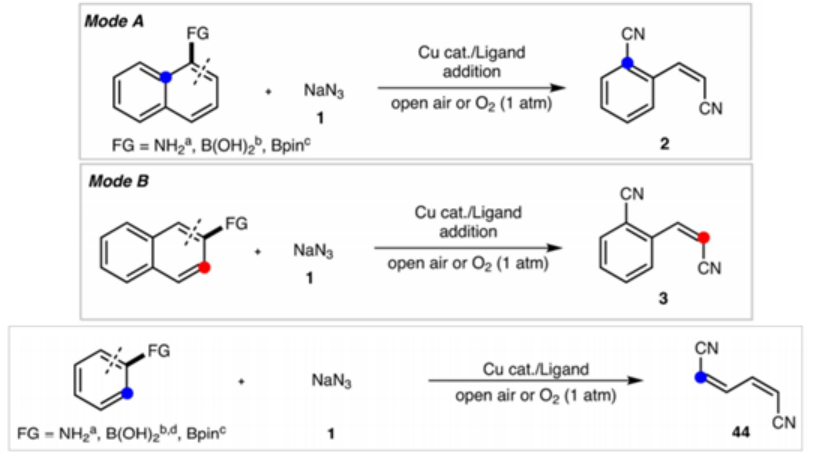
由于相關(guān)文獻中1,2-雙疊氮苯在加熱分解反應(yīng)能夠生成1,4-雙氰基-1,3-丁二烯,這個反應(yīng)現(xiàn)象說明1,2-亞苯基雙氮賓中間體能夠?qū)崿F(xiàn)苯環(huán)開環(huán)反應(yīng)。因此,作者設(shè)計了NaN3與Cu結(jié)合后,形成兩個活性N配位形成類似鄰苯二酚結(jié)構(gòu),因此可能以類似雙氮賓中間體過程進行芳基開環(huán)反應(yīng)。
因此作者通過疊氮化物NaN3作為活性N-輔酶,通過Cu催化劑進行有氧氧化反應(yīng),將萘結(jié)構(gòu)分子以較好的立體選擇性轉(zhuǎn)化為(Z)-2-氰乙烯基-苯甲氰。
反應(yīng)情況