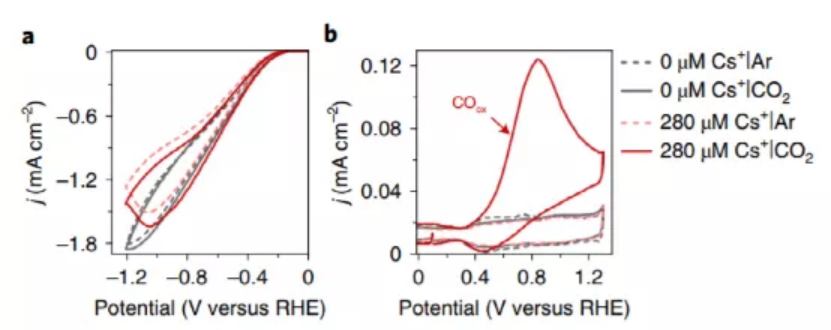
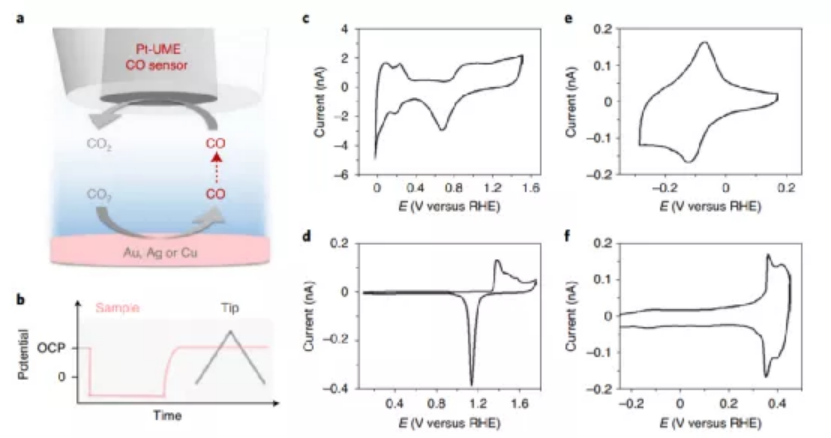
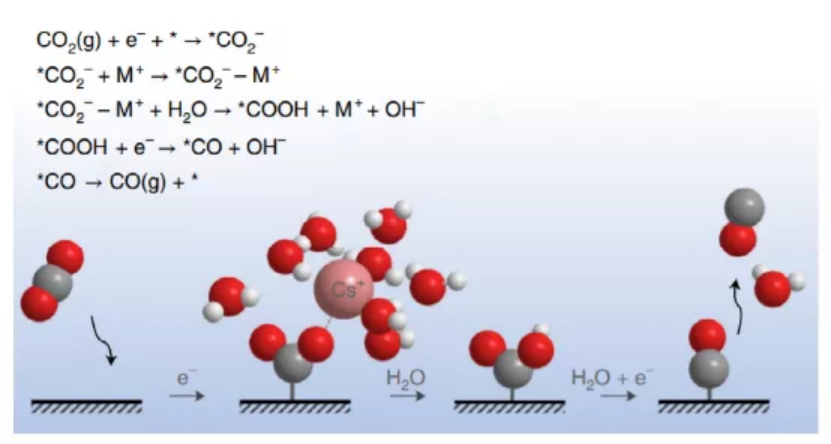
1.通過掃描電化學(xué)顯微鏡原位實(shí)驗(yàn)表征電催化CO2還原2.通過界面附近的微Pt電極測試催化劑界面生成產(chǎn)物情況3.提出了比較完整的堿金屬輔助CO2電化學(xué)還原反應(yīng)機(jī)理第一作者:Mariana C. O. Monteiro?CO2電化學(xué)還原反應(yīng)被能源�、化學(xué)品的可持續(xù)發(fā)展和制備廣泛研究,電解液中的金屬離子能夠顯著影響反應(yīng)情況�����,但是金屬離子的主要作用并未很好的揭示。有鑒于此��,荷蘭萊頓大學(xué)Marc T. M. Koper等研究Au電極的CO2電化學(xué)還原反應(yīng)情況���,通過循環(huán)伏安法電化學(xué)表征�����,發(fā)現(xiàn)反應(yīng)在沒有金屬離子存在時無法正常進(jìn)行。進(jìn)一步的�,作者分別通過掃描電化學(xué)顯微鏡和Pt超微電極作為CO���、H2氣體傳感器,測試發(fā)現(xiàn)在向電解液中加入金屬離子后,只能在Au�����、Ag�、Cu電極上形成CO。進(jìn)一步的作者通過DFT計算模擬,驗(yàn)證了部分去溶劑化的金屬離子能夠通過短程經(jīng)典相互作用穩(wěn)定CO2-中間體物種�,因此促進(jìn)CO2的還原反應(yīng)���?��?傊?�,本文相關(guān)研究結(jié)果明確了該反應(yīng)的機(jī)理,說明了電解液中的正電荷物種對于穩(wěn)定關(guān)鍵反應(yīng)中間體物種的重要作用����。電化學(xué)CO2還原反應(yīng)在近期受到非常廣泛的研究����,這種技術(shù)有望實(shí)現(xiàn)進(jìn)一步的碳平衡��,將可再生能源轉(zhuǎn)化為化學(xué)鍵并且將其存儲��。人們發(fā)現(xiàn)電解液的組成,尤其是其中的金屬離子�,對催化反應(yīng)的活性�����、產(chǎn)物分布情況產(chǎn)生非常大的影響�。比如����,當(dāng)電解液中含有堿金屬離子,Cu催化劑的催化反應(yīng)電流密度�、C2+產(chǎn)物選擇性與離子半徑有關(guān)���,更大的離子半徑導(dǎo)致更高的催化電流密度荷C2+產(chǎn)物選擇性。這種作用被稱為陽離子效應(yīng)�。目前文獻(xiàn)對這種陽離子影響電催化反應(yīng)有三種理論:對局部電場的影響���、對界面pH的緩沖作用��、穩(wěn)定反應(yīng)生成的中間體。圖1. 溶液Cs+陽離子促進(jìn)CO2電化學(xué)還原作者通過實(shí)驗(yàn)和DFT理論計算模擬相結(jié)合���,揭示電解液中的金屬離子是CO2電化學(xué)還原反應(yīng)在Cu、Au��、Ag上進(jìn)行必不可少的條件�����。作者首先在多晶Au電極上進(jìn)行CO2電化學(xué)還原反應(yīng)�����,在H2SO4中進(jìn)行電催化,考察堿金屬的加入對電催化反應(yīng)的影響,作者通過陽極氧化/陰極還原電化學(xué)循環(huán),對CO2還原生成的CO進(jìn)行定量標(biāo)定���。作者發(fā)現(xiàn)當(dāng)Cs+存在才能在Au電極上生成CO,而且作者通過對比,向Li2SO4電解液加入Cs+離子能夠引發(fā)CO2電化學(xué)還原反應(yīng)���。這個結(jié)果說明少量Cs+離子對反應(yīng)中是否生成CO產(chǎn)生顯著影響,進(jìn)一步的作者通過加入不同陽離子半徑的堿金屬離子,發(fā)現(xiàn)半徑更高的堿金屬具有更好的電催化CO2還原活性,而且如果不加入任何堿金屬離子�����,反應(yīng)中只能進(jìn)行HER反應(yīng)���,通過這項(xiàng)實(shí)驗(yàn)����,作者驗(yàn)證了堿金屬對于CO2電化學(xué)還原反應(yīng)的關(guān)鍵作用�。圖2. 掃描電化學(xué)顯微鏡原位觀測反應(yīng)作者通過掃描電化學(xué)顯微鏡(SECM)對Ag、Cu電極上的CO2電化學(xué)還原反應(yīng)情況進(jìn)行表征,通過Pt微電極探測反應(yīng)生成的微量CO�����、H2�,將Pt微電極置于電極距離50±2 μm的位置,因此能夠通過Pt電極對CO2RR�����、HER反應(yīng)生成的產(chǎn)物進(jìn)行原位表征����。分別對是否含有Cs+的電解液通過Pt微電極分別對Au、Ag���、Cu電極上的電化學(xué)反應(yīng)情況進(jìn)行表征,驗(yàn)證了僅僅當(dāng)電解液中含有Cs+才能實(shí)現(xiàn)CO2電化學(xué)還原反應(yīng)����。作者基于DFT計算�,使用分子動力學(xué)模擬AIMD�����,對室溫條件中1.5 nm×1.5 nm的Au(111)表面的電化學(xué)反應(yīng)情況進(jìn)行模擬�����,分別向體系中加入Li+,Na+���,K+,Cs+幾種堿金屬陽離子���,考察對電化學(xué)CO2還原反應(yīng)的影響,結(jié)果說明堿金屬離子的三重作用:作者發(fā)現(xiàn)Cs+比Li+表現(xiàn)了更好的CO2分子結(jié)合能力�����,通過CO2配位以短程M+-OCO形式能夠提高CO2的吸附穩(wěn)定性�,穩(wěn)定能量提高0.5 eV;通過堿金屬陽離子的配位作用���,OCO分子的角度得以從180°降低至140°,說明CO2分子很好的被活化�����;堿金屬陽離子改善了電極向表面吸附CO2分子的電荷轉(zhuǎn)移��。通過DFT計算模擬����,驗(yàn)證堿金屬陽離子改善了CO2還原反應(yīng)的進(jìn)行���,因此作者提出了新型CO2還原為CO的反應(yīng)機(jī)理����。這種新型機(jī)理中包括金屬陽離子改善CO2分子吸附、促進(jìn)電極向CO2分子的電子轉(zhuǎn)移�、水分子向CO2提供質(zhì)子�。當(dāng)電解質(zhì)中不加入金屬陽離子��,Au����、Ag�、Cu電催化反應(yīng)中都無法進(jìn)行CO2還原為CO�,現(xiàn)有的理論中認(rèn)為金屬離子起到的作用在于:調(diào)控局部電場效應(yīng)、對界面pH值變化過程實(shí)現(xiàn)緩沖�����、提高反應(yīng)的中間體穩(wěn)定����。而且以上的作用都通過實(shí)驗(yàn)或者DFT計算得以驗(yàn)證,說明在CO2電化學(xué)還原反應(yīng)中起到一些作用����。作者在本文工作中發(fā)現(xiàn)����,對局部電場的調(diào)控�、局部pH值變化的緩沖是主要的陽離子作用。比如,堿金屬陽離子通過陰陽離子相互作用穩(wěn)定*CO2-����、*OCCO-負(fù)電荷中間體�,此外作者發(fā)現(xiàn)部分脫水的金屬陽離子與CO2分子之間同樣起到類似的電荷穩(wěn)定作用�。作者發(fā)現(xiàn)當(dāng)向溶液中加入更多的Cs+,反應(yīng)能夠生成更多的CO產(chǎn)物。這種現(xiàn)象與相關(guān)報道發(fā)現(xiàn)的Cu催化劑制備乙烯的過程非常類似���。這種作用是因?yàn)?/span>Na+、K+���、Cs+金屬離子的水化殼結(jié)構(gòu)較柔軟在催化劑的界面上濃度更高,同時能夠與CO2形成穩(wěn)定配位結(jié)構(gòu)�,由此產(chǎn)生更好的穩(wěn)定作用�;Li+金屬離子的水化殼較硬��,因此難以與CO2配位��。這種金屬陽離子通過與CO2-中間體相互作用,輔助CO2電催化還原的現(xiàn)象具有非常大的意義�����。通過設(shè)計穩(wěn)定作用比Cs+效果更好的陽離子����,比如通過高價態(tài)陽離子、表面活性劑,能夠進(jìn)一步改善CO2電催化反應(yīng)�;作者發(fā)現(xiàn)電化學(xué)CO2活化的過程中陽離子�、H2O分子都起到一定的作用���。此外���,作者提出H+離子本身無法作為質(zhì)子供體活化CO2分子��,只有pH達(dá)到或者高于3��,水分子作為質(zhì)子供體同時生成OH-,因此CO2電化學(xué)還原反應(yīng)過程中不消耗H+。Monteiro, M.C.O., Dattila, F., Hagedoorn, B. et al. Absence of CO2 electroreduction on copper, gold and silver electrodes without metal cations in solution. Nat Catal (2021).DOI: 10.1038/s41929-021-00655-5https://www.nature.com/articles/s41929-021-00655-5