
第一作者:Yukun Zhao
通訊作者:章宇超,陳春城,趙進才院士
通訊單位:中科院化學所
研究背景
光電化學(PEC)技術已被廣泛研究用于太陽能轉換(例如,水的分解)和通過污染物降解進行環境修復等領域。此外,人們也利用PEC體系,通過光催化轉化有機化合物來生產精細化學品,并取得了一定的研究進展。例如,最近報道了一種以BiVO4為光陽極的PEC系統,以叔丁基氫過氧化物為氧源,實現了苯甲醇、環己烯和四氫萘的C-H鍵的活化,這些C-H鍵分別生成苯甲醛、環己酮和四酮。然而,與更傳統的電化學法和光化學法相比,目前尚無法實現高效的PEC法。如何直接獲取光生載流子(電子或空穴)以促進電化學界面上的有機轉化仍有待進一步的研究。
赤鐵礦(α-Fe2O3)因其豐度、無毒、穩定、可見光吸收等優點,被認為是PEC體系中最有前途的光陽極材料之一。以往對α-Fe2O3基PEC的研究主要集中在水裂解制氫過程中的光催化水氧化反應,但其產物氧氣(O2)的經濟價值較低。最近有研究報道表明,在α-Fe2O3光陽極上,光誘導空穴氧化富電子芳烴所形成的自由基陽離子可導致具有不同尋常的鄰位選擇性的有效芳烴C-H胺化反應。同時,在α-Fe2O3光陽極上的水氧化過程中,是捕獲在表面態的空穴(而不是價帶中的空穴)與吸附的水反應以驅動水氧化。通過原位衰減全反射傅立葉變換紅外光譜以及軟 X 射線 (O 1s) 光譜技術,這些被捕獲的空穴已被證明為高價鐵-氧中間體 (FeIV=O)。α-Fe2O3 表面捕獲空穴的高價鐵-氧特征與這種在在生物系統中普遍存在的、在催化氧化過程中被廣泛研究的高價金屬-氧物種有關。例如,已廣泛應用于生產重要醫藥中間體的氧原子轉移 (OAT) 反應通常由高價金屬-氧物種引發。在基于金屬配合物的 OAT 系統中,有機配體總是用于調節金屬中心的微環境。這些有機配體在強氧化性 OAT 條件下容易受到損壞,這使得這些金屬配合物相當不穩定。此外,高價金屬-氧物種的形成通常是在極強氧化性過氧物種的幫助下實現的。因此,很難避免產生副產品。同時,在這些均相系統中,產品分離也是一個問題。實際上,使用金屬氧化物電極的 PEC 方法有望克服這些缺點。
成果簡介
鑒于此,中科院化學研究所趙進才院士,章宇超和陳春城報道了將α-Fe2O3應用擴展到高附加值化學品的生產,并報告了其在可見光照射下作為多功能且高效的氧原子轉移催化劑的能力。以水為唯一氧源,多種有機化合物和無機陰離子被成功氧化為相應的單氧化產物,且具有高選擇性和高法拉第效率。光激發空穴在 α-Fe2O3 表面產生FeIV=O。接著,所提出的氧原子轉移過程通過協調的雙空穴轉移途徑進行,該途徑涉及氧原子從 FeIV=O 表面轉移到底物。該研究證明 α-Fe2O3 是一種優異的全無機多相催化劑,可以驅動氧原子轉移反應,因此,在合成精細和高附加值化學品方面具有巨大的應用潛力。
α-Fe2O3上的PEC氧化反應
研究人員在摻氟氧化錫玻璃襯底上制備了α-Fe2O3光陽極,并用掃描電子顯微鏡、X射線衍射光譜和X射線光電子能譜對其進行了表征。線性掃描伏安法顯示,在AM 1.5 G照射下,在含少量水(5%)的CH3CN溶液中,起始電位約為0.05 V,而Fc/Fc+在甲基苯硫醚(MPS)存在下,起始電位和起始光電流變化不大(圖1a)。但是,當偏壓大于0.25 V時,有MPS的光電流開始超過沒有MPS的光電流。為了研究MPS的氧化產物,在Ar氣中進行了0.37 V與Fc/Fc+的光電解實驗。高效液相色譜(HPLC)產物分析結果表明,在整個PEC過程中,MPS幾乎定量地轉化為甲基苯亞砜(MPSO),整個過程持續2 h,其中約86.6±1.6%的MPS被氧化(圖1b)。MPSO形成的FE為92.1±5.8%,同時,陰極處產生H2,其FE為95.0%。隨著MPS濃度的升高,FE增加(93.8±2.0%),在不同的水含量(從5%到20%)下,也觀察到MPSO的高選擇性和FE(表1)。
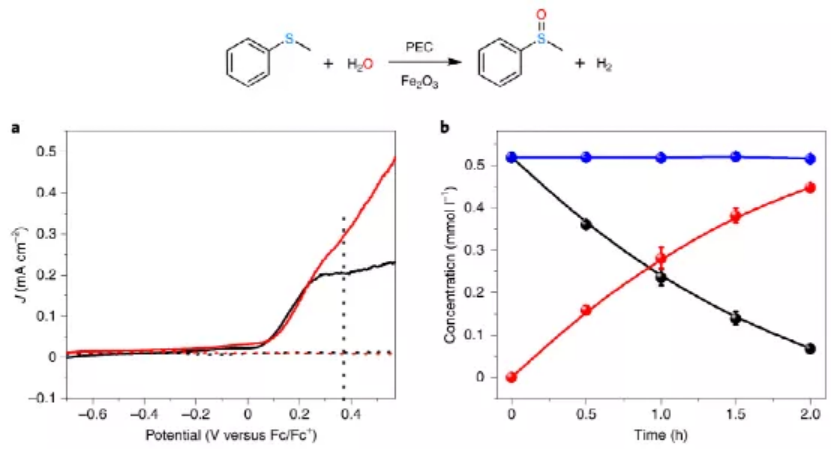
圖1 MPS氧化的線性掃描伏安法和光電解實驗
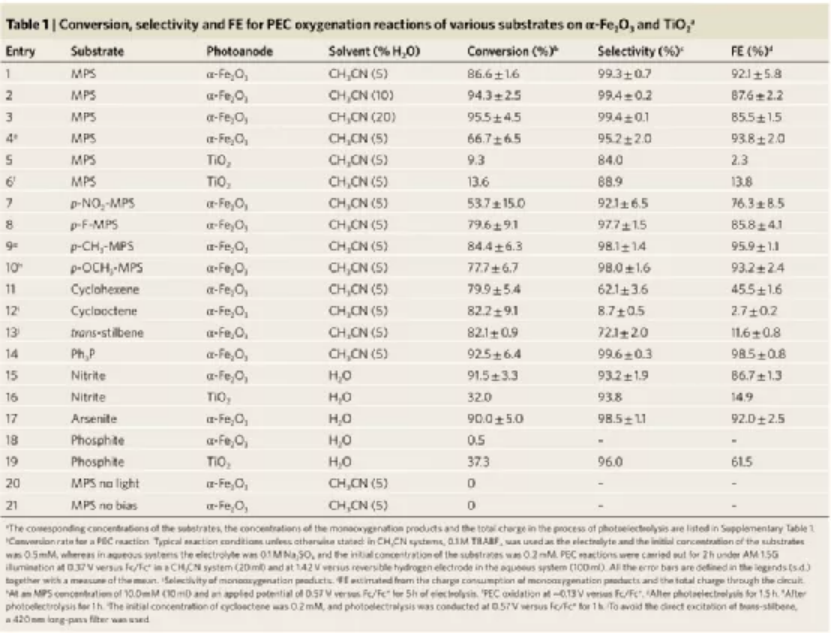
表1 α-Fe2O3和TiO2上不同底物的PEC氧化反應的轉化率、選擇性和FE
研究發現,亞硝酸鹽和亞砷酸鹽離子具有單對σ軌道(圖2),可以接受來自供體的氧原子。然而,對于亞磷酸鹽,直接與磷原子鍵合的氫原子不易電離,因此其沒有單對電子的軌道可用于O原子給體的親電攻擊。OH自由基對P-H鍵的直接單電子氧化或吸氫作用比OAT反應更有利,這可能是亞磷酸鹽在TiO2上能夠有效氧化的原因。

圖2. pKa值和結構圖
氧原子源的識別
為了進一步研究MPS的PEC氧化過程中的氧原子來源,研究人員進行了H218O同位素標記實驗(圖3)。當在Ar氣氛中使用H216O時,MPSO的突出分子離子峰出現在140.1的質荷比(m/z)處(圖3b)。在 Ar中用 H218O 替換 H216O 后(圖 3a),該峰移至 142.1,并且m/z=140.1 的相對豐度非常小(6.1%)。此外,去甲基化片段(C6H5SO片段,m/z = 125.1)的離子峰也從125.1移至127.1。這些結果表明水是α-Fe2O3上MPS氧化成MPSO的唯一氧原子來源。
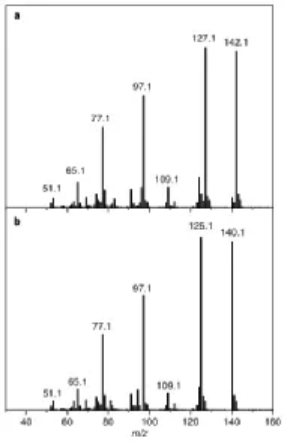
圖3. MPSO的質譜圖
表面空穴的作用
早期的工作表明,α-Fe2O3上的水氧化是通過表面俘獲空穴,而不是通過在低陽極電位下價帶的直接空穴轉移進行的。為了揭示這些表面空穴在氧化反應中的作用,研究人員接著使用電化學阻抗譜(EIS)來研究 MPS 氧化在 α-Fe2O3 上的反應動力學。研究發現,不管 MPS 是否存在,Ctrap 在低電位下隨著施加的偏壓而增加,并且由于表面空穴的積累而在相對于 Fc/Fc+ 的大約 0.25 V 處達到最大值(圖4a)。之后,由于表面俘獲空穴的消耗率增加,Ctrap開始下降。這些結果表明,與水氧化類似,MPS在α-Fe2O3上的氧化也是由表面俘獲空穴誘導而致。此外,在MPS存在下,Ctrap的減少比在純電解質中更快,證實了MPS氧化對表面俘獲空穴的消耗比水氧化更快。不同光強下基于 EIS 測量的速率定律分析進一步表明,MPS 氧化過程中表面捕獲空穴的反應順序在 α-Fe2O3 上約為 1.72,而在 TiO2 上約為 0.85 (圖 4b),因此,MPS在α-Fe2O3和TiO2上的氧化反應傾向于表面陷阱空穴的二級反應和一級反應。
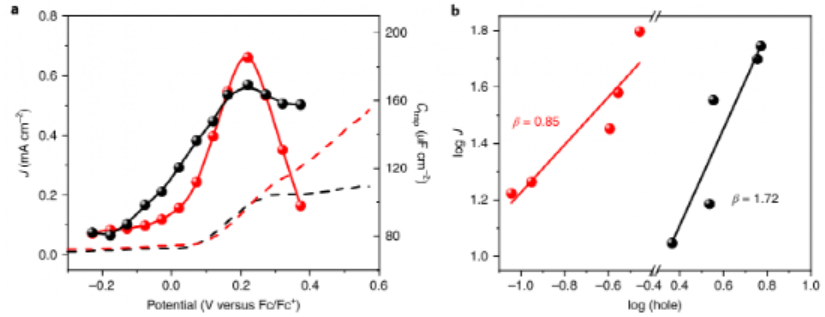
圖4. 基于EIS數據的表面-空穴捕獲態
機理分析
研究人員認為,表面陷阱孔是由空穴轉移到表面配位的羥基形成的,并伴隨著去質子化步驟(圖5中的步驟(1))。根據自旋極化密度泛函理論U對態密度的分析,這些表面態位于α-Fe2O3的中間能隙中,由雜化的O 2p和Fe 3d軌道組成。化學上,這些雜化表面態上空穴的捕獲可能導致高價鐵氧(FeIV=O)物種的形成這些鐵氧物種的化學性質類似于生物激發的血紅素和非血紅素復合物的鐵氧中心。表面陷阱空穴的積累表明,這一過程需要足夠的FeIV=O密度(圖4a)。在表面空穴的積累過程中,也有可能兩個電子從一個Fe-O位被移走,形成Fev=O物種,據報道,Fev=O物種也是驅動OAT反應的活性物質。然而,理論計算結果表明,Fev=O形成的能量增量高于相鄰的兩個FeIV=O,這表明相對于相鄰的兩個FeIV=O的形成而言,FeV=O的形成在熱力學上是不利的。因此,在本實驗條件下,相鄰的兩個FeIV=O中心應該是OAT反應的活性中心。在OAT步驟發生之前,底物對FeIV-oxo的氧原子的親核攻擊可能導致形成一個中間絡合物(圖5中的步驟(2)),這將吸引其他表面空穴跳躍到鄰近的位置。接著的OAT步驟是限速步驟,應該與α-Fe2O3表面相鄰的FeIV-oxo位的電子轉移相一致(圖5的步驟(3))。這一限速步驟包括Fe-O鍵的斷裂、X-O鍵的形成以及來自相鄰捕獲空穴的協調空穴轉移。在此過渡態之后,氧原子的釋放和氧化產物(XO)的釋放導致表面FeIII空位。水在這些位點的吸附和解離再生了表面羥基,以終止催化循環(圖5中的步驟(4))。
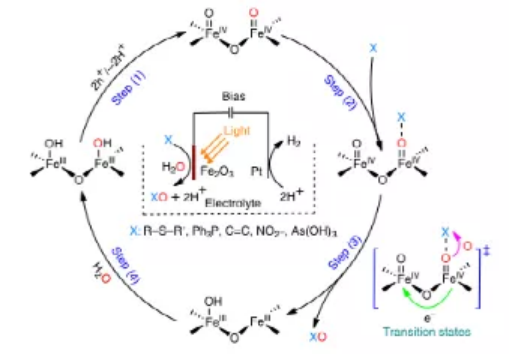
圖5. α-Fe2O3上PEC OAT與水作為氧原子源的反應過程
小結
這項研究發展了一種在溫和條件下對α-Fe2O3進行OAT反應的脈沖電化學法。以水為唯一氧原子源可以氧化多種底物,包括硫醚、烯烴、Ph3P和無機鹽。對于絕大多數襯底,優良的氧化選擇性和FE均可達到90.0%以上。此外,EIS和DFT研究證實了表面陷阱空穴在OAT機理中起著舉足輕重的作用。這種PEC策略在精細和增值化學品的各種氧化反應中具有巨大的潛力。
Zhao, Y., Deng, C., Tang, D. et al. α-Fe2O3 as a versatile and efficient oxygen atom transfer catalyst in combination with H2O as the oxygen source. Nat Catal (2021).
DOI:10.1038/s41929-021-00659-1
https://doi.org/10.1038/s41929-021-00659-1











