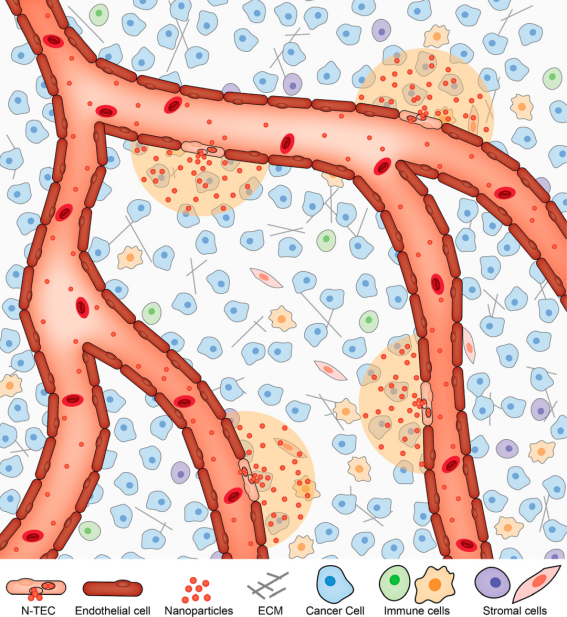
將靜脈內給藥的治療劑遞送至實體瘤取決于它們穿過腫瘤血管的能力。納米顆粒有助于將化療藥物、生物制劑和核酸等貨物運輸到腫瘤中,但它們對實體瘤的遞送效率較低。當前設計納米粒子的策略是基于我們對它們如何運輸到腫瘤中的理解。研究人員曾設計納米粒子,通過控制納米粒子的大小和形狀,通過內皮細胞之間的開放間隙被動地穿過血管進入腫瘤。然而,越來越多的證據表明,主動轉運機制介導了大部分納米顆粒通過內皮細胞跨腫瘤血管的轉運。為了設計具有主動轉運機制的納米顆粒,我們需要更深入地了解納米顆粒和腫瘤內皮界面處的相互作用。上一年在Nature Materials期刊上,加拿大多倫多大學Warren C. W. Chan等人探討了納米顆粒腫瘤滲透的現象,并質疑了納米顆粒進入實體瘤的機制。于此,不禁問道,是否所有的腫瘤內皮細胞都能運輸納米顆粒嗎?近日,加拿大多倫多大學Warren C. W. Chan課題組發現體內需要特定的內皮細胞來控制納米粒子進入實體瘤。他們確定了腫瘤內皮細胞的一個子集,稱為納米顆粒轉運內皮細胞 (N-TECs),它決定了納米顆粒從血管腔到腫瘤微環境的轉運。相關成果發表在ACS Nano上。研究人員想確定納米顆粒通過內皮細胞的轉運是否發生在整個腫瘤血管系統中。識別參與轉運過程的特定內皮細胞可能有助于了解腫瘤如何以及為何積累納米顆粒。通過尾靜脈將聚乙二醇化金納米顆粒(50 nm)注射到患有 4T1 乳腺腫瘤的小鼠體內。通過3D成像技術,并使用流式細胞術來測量含有納米顆粒的腫瘤內皮細胞的比例。結果表明,N-TECs 占腫瘤內皮細胞的比例不到 21%,并且沿腫瘤血管分布不均。也就是說,只有一部分腫瘤內皮細胞可以吸收和運輸納米顆粒。
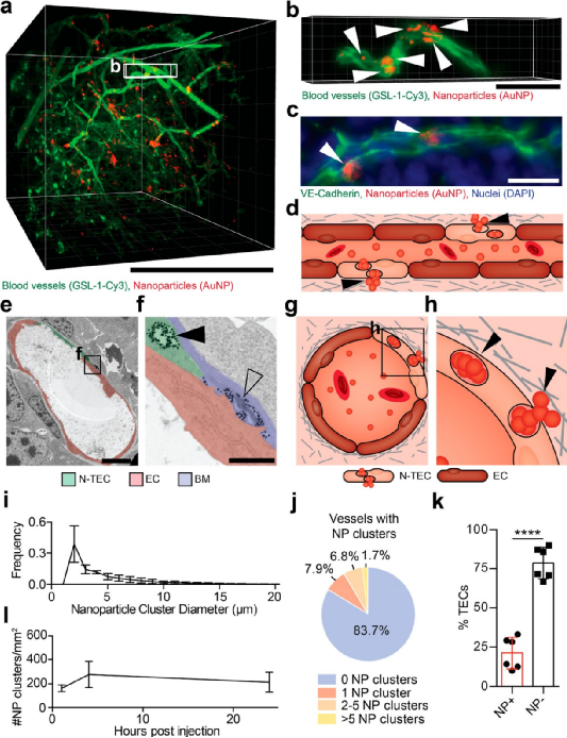
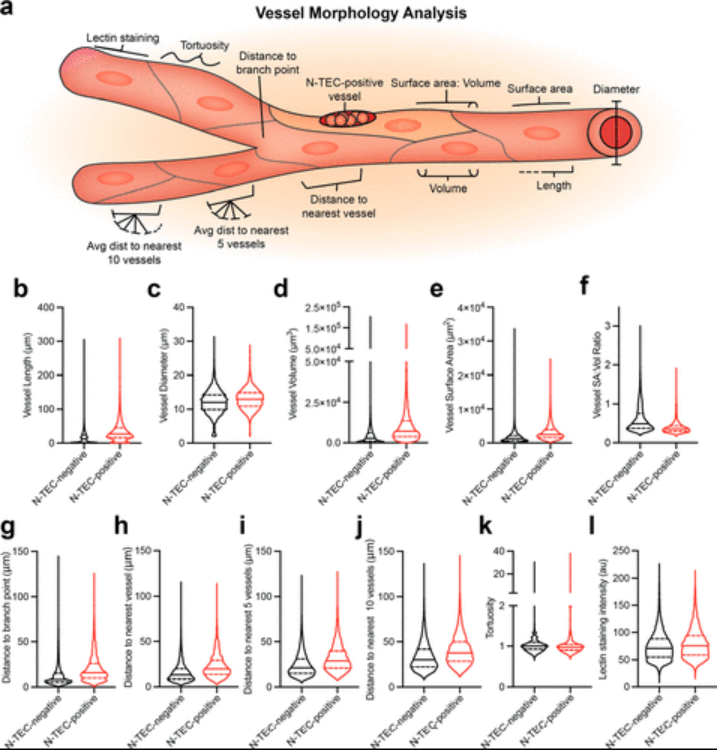
圖|特定腫瘤內皮細胞的納米顆粒局部轉運圖|具有N-TECs和無N-TECs的腫瘤血管形態此外,含有 N-TECs 的血管與不含 N-TECs 的血管在形態上也是不同。還對 N-TECs 的轉錄組進行了表征,以了解納米顆粒轉運和非轉運腫瘤內皮細胞之間的分子差異。研究發現,與其他腫瘤內皮細胞相比,N-TECs 中有 530 個基因增加,N-TECs 中有 2377 個基因減少。與其他腫瘤內皮細胞相比,N-TECs具有不同的基因表達譜,并顯示出與先前已知的血管通透性和轉運相關基因的聯系。納米粒子在癌癥應用中的效用取決于遞送到腫瘤的納米粒子的數量以及這些納米粒子在腫瘤內的分布方式。分布很重要,因為它決定了對納米顆粒載體可能靶向的選定細胞的訪問。研究表明,N-TEC 充當納米粒子進入腫瘤的守門人,并影響納米粒子的遞送效率、在腫瘤內的分布以及進入腫瘤細胞的途徑。綜上所述,研究人員確定了腫瘤內皮細胞的一個子集,這些細胞將納米粒子從血管傳輸到腫瘤微環境中。這些細胞充當腫瘤的入口,并增加了參與分子進出內皮細胞轉運的基因表達。這些細胞沿腫瘤血管不均勻分布。N-TECs 的數量和位置會影響納米顆粒的遞送效率和納米顆粒在腫瘤微環境中的分布。這些結果解釋了在腫瘤微環境中觀察到的納米顆粒的異質分布模式。該研究還開始確定和定義腫瘤細胞異質性對納米顆粒遞送的影響。識別腫瘤中有助于或抑制納米粒子傳遞的關鍵細胞類型可能有助于發現可以預測癌癥納米藥物有效性的生物標志物。Specific Endothelial Cells Govern Nanoparticle Entry into Solid Tumors. ACS Nano 2021.https://doi.org/10.1021/acsnano.1c04510