
第一作者:郝少云
通訊作者:張興旺,金松
通訊單位:浙江大學,威斯康星大學麥迪遜分校
研究背景
新興的電化學技術可以利用可再生太陽能和風能來生產燃料和化學品。由于較低的電阻損失和較少的氣體交叉,在酸性電解液中通過質子交換膜(PEM)水電解制氫可以獲得比傳統堿性電解槽更高的電流密度。目前,水分解制氫的效率受到析氧反應(OER)的顯著限制,由于涉及多個氧中間體的緩慢的四電子轉移過程,該反應具有很高的催化過電位。此外,諸多OER電催化劑在酸性溶液中的穩定性較差,這對PEM電解槽的發展提出了更大的挑戰,目前,IrOx是已知的唯一實用的工業OER電催化劑。然而,IrOx催化劑仍然存在質量活性低的問題,不能滿足商業電流密度下的高性能和長期穩定的要求。因此,需要進一步提高其催化性能并降低貴金屬的負載量,同時提高酸性OER催化劑的穩定性將使PEM電解水制氫技術更具競爭力。
先前的研究表明,OER催化活性可以根據OH*和O*中間體的吸附自由能之間的差異來預測,這與活性位點的電子結構密切相關。首先,將金屬摻雜到IrOx或Ir基鈣鈦礦氧化物中,調整Ir位點的電子結構,從而有效提高其OER活性。此外,通過應變工程也可以提高催化劑在各種類型電化學反應的活性。在精心設計的核殼或貴金屬催化劑合金納米結構中,通常存在壓縮或拉伸應變。進一步的,將類似的概念擴展到核-殼金屬氧化物納米結構或薄膜中生成壓縮或拉伸晶格應變,通過調節金屬-氧(M-O)鍵來增強OER活性。然而,在高度氧化和酸性OER環境下,這種無序的納米結構催化劑很容易被溶解或氧化,導致活性急劇下降。因此,在晶格應變下實現增強其活性的同時保持其催化穩定性一直具有挑戰性。此外,晶界(GB)可以通過在材料生長過程中的堆垛層錯(SFs)運動或定向附著引入到晶體材料中。最近的研究發現,GB的存在可以提高金屬的催化活性,GB結構中不僅可以靈活地引入和控制壓縮或拉伸應變,同時也可引入新型的應變以優化催化性能。此外,由于GB結構的可逆性,催化穩定性也可以更好地保持。
成果簡介
近日,浙江大學張興旺教授,美國威斯康星大學麥迪遜分校金松教授報道了通過使用快速熱解合成策略并將金屬(Ta和Tm)摻雜到IrO2-δ中,開發出一種扭轉應變的Ta0.1Tm0.1Ir0.8O2-δ納米催化劑,該催化劑具有豐富的晶界,在10 mA cm?2時對0.5 M H2SO4中的OER表現出198 mV的低過電位。微觀結構分析、X射線吸收光譜和理論計算表明,晶界間產生扭轉應變Ir-O鍵的協同效應和摻雜誘導的配體效應共同調節了氧中間體的吸附能,從而提高了催化活性。進一步的,質子交換膜電解槽使用0.2 mg cm-2低負載的Ta0.1Tm0.1Ir0.8O2-δ納米催化劑可在1.5 A cm-2 下穩定運行500小時,預計生產每公斤H2成本為1美元。
要點1納米催化劑的合成與表征
研究人員采用快速熱解的方法合成了扭轉應變的TaxTmyIr1?x?yO2?δ納米催化劑。通過對多種過渡金屬元素和鑭系金屬元素的實驗研究,選擇了鉭(Ta)和鉈(Tm)雙金屬摻雜作為催化劑的增強劑和穩定劑。在混合的水和乙醇溶液中,金屬鹽前驅體的混合物被氨水和檸檬酸共沉淀,然后快速加熱到450 °C,得到相互連接的納米介孔網絡(圖1a)。制備富含GB的納米催化劑的關鍵是快速加熱和熱解過程。相反,不含GB的IrO2?δ和Ta0.1Tm0.1Ir0.8O2-δ納米催化劑則是通過傳統的慢速裂解法合成(圖1a底排到1d)。晶格扭曲可應對在短時間尺度內碰撞的眾多相鄰晶體顆粒之間的晶面取向(圖1a)。因此,晶粒通過取向附著沿納米催化劑的軸向生長,并且由于晶格扭轉引起的剪切應變出現在三叉GB處,其中出現三個或更多相鄰晶粒。HRTEM圖像顯示,通過快速熱解合成的GB-Ta0.1Tm0.1Ir0.8O2?δ納米催化劑的平均粒徑約為10 nm,含大量GBs(圖1 e-g),并與緩慢熱解形成的納米催化劑形成鮮明對比(圖1b-d)。沿納米催化劑表面滑動的失配應變在三叉GBs處產生了許多SFs(圖1 f, g)。
通過幾何相位分析(GPA),研究人員進一步定量分析了GB-Ta0.1Tm0.1Ir0.8O2-δ納米催化劑中沿GB(圖1 h-k)和SF(圖1 l-O)的應變分布。在晶格扭轉作用下,GB既可以出現剪切應變,也可以出現軸向應變(可以是壓縮應變,也可以是拉伸應變)。結果顯示,軸向應變(?xx)和剪切應變(?xy)都分布在GB的兩側,最大值分別為?xx=3%(圖1 j)和?xy=6%(圖1 k)。此外,?xy沿GB方向的最大值是?xx的兩倍,表明晶格扭轉引起的剪切應變是GB-Ta0.1Tm0.1Ir0.8O2-δ納米催化劑表面的主要應變(圖1 k)。此外,在(111)面上沿著SF也存在相當大的軸向應變和剪切應變,其分別達到?xx=2%(圖1 n)和?xy=3%(圖1 o)的最大值。這進一步證實了沿SF的剪切應變占主導地位。因此,GPA分析證實了在快速熱解形成的GB-Ta0.1Tm0.1Ir0.8O2-δ納米催化劑中存在沿GB和SF方向的剪切應變,而慢速熱解形成的相同組成的納米催化劑則不存在這一點。
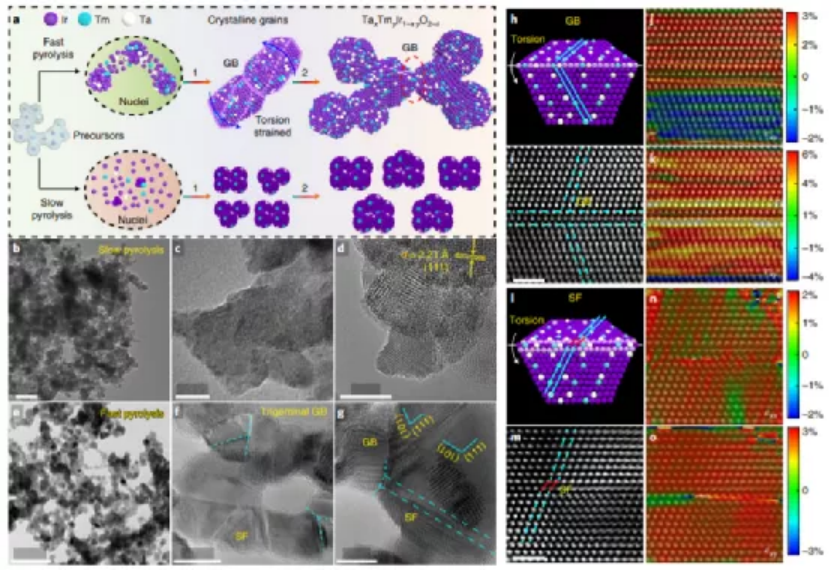
圖1 扭轉應變的TaxTmyIr1?x?yO2?δ納米催化劑的合成與表征
要點2 氧化態和鍵長分析
為了研究這些GB-TaxTmyIr1?x?yO2?δ納米催化劑的表面電子結構和化學態,利用X射線光電子能譜(XPS)對Ir 4f、Ta 4f、Tm 4d和O 1s信號進行了研究。研究發現,在GB-IrO2-δ中引入Ta和Tm,使這三組GB-Ta0.1Tm0.1Ir0.8O2-δ的雙鍵比GB-IrO2-δ的雙鍵的結合能更低(圖2a),表明在GB-Ta0.1Tm0.1Ir0.8O2-δ中Ir具有更低的價態。此外,X射線吸收近邊光譜(XANES)揭示了C-IrO2、GB-IrO2-δ和GB-Ta0.1Tm0.1Ir0.8O2-δ在應變和摻雜作用下Ir-O鍵長和價態的差異(圖2b)。結果表明Ir在GB-IrO2-δ和GB-Ta0.1Tm0.1Ir0.8O2-δ中的平均價態比+4低。因此,表面物種可能是Ir<3+< sup="">和Ir<4+< sup="">。進一步的擴展X射線吸收精細結構(EXAFS)譜揭示了C-IrO2、GB-IrO2-δ和GB-Ta0.1Tm0.1Ir0.8O2-δ的配位結構(圖2 c, d)。由于應變效應,GB-IrO2-δ的第一殼Ir-O長度為2.02 ?,略高于C-IrO2 (1.97 ?)(圖2c),GB-Ta0.1Tm0.1Ir0.8O2-δ (2.06 ?)的第一殼層Ir-O長度甚至略長于GB-IrO2-δ(圖2d)。因此,Ta和Tm也可以調節Ir-O鍵的長度。這些EXAFS結果進一步證實了在GB-IrO2-δ和GB-Ta0.1Tm0.1Ir0.8O2-δ納米催化劑中存在應變,這與HRTEM和GPA分析一致。GB-Ta0.1Tm0.1Ir0.8O2-δ納米催化劑中Ir-O鍵的伸長表明應變和摻雜協同調節Ir-O鍵的共價鍵和電子結構。
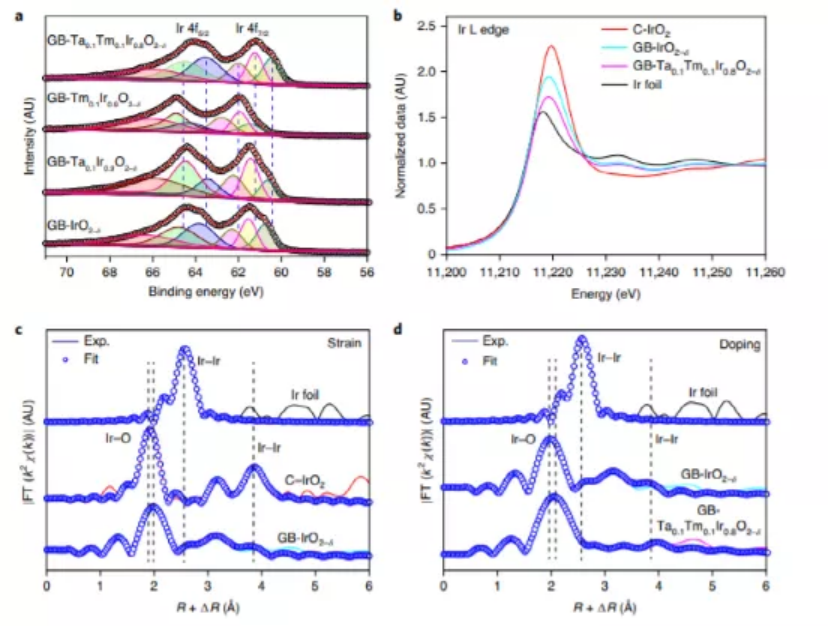
圖2不同GB-TaxTmyIr1?x?yO2?δ催化劑的XPS和EXAFS表征
要點3 酸性OER性能
研究人員在0.5 M H2SO4中,研究了TaxTmyIr1?x?yO2?δ納米催化劑的OER催化活性,并與其他對照樣品進行了比較(圖3)。實驗結果顯示,無GB的IrO2-δ和TaxTmyIr1?x?yO2?δ納米顆粒用于電催化OER的過電位(η10)分別為299和226 mV,才可獲得10 mA cm?2的電流密度。相比之下,GB-IrO2-δ和GB-Ta0.1Tm0.1Ir0.8O2 -δ納米催化劑所需的η10值分別為253 mV和198 mV。因此,應變顯著提高了GB-IrO2-δ和GB-Ta0.1Tm0.1Ir0.8O2 -δ納米催化劑的OER活性。此外,不同組成的GB系列納米催化劑的OER活性(圖3b)遵循GB-Ta0.1Tm0.1Ir0. 8O2-δ >GB-Ta0.1Ir0.9O2?δ ≌ GB-Tm0.1Ir0.9O2?δ > GB-IrO2?δ >C-IrO2,從而揭示了引入Tm和Ta協同優化了GB-IrO2-δ中的OER活性。
研究人員在η = 266 mV時,計算了催化劑的質量活性。結果顯示,GB-Ta0.1 Tm0.1 Ir0.8O2-δ具有3,126 mA mgIr?1的最高質量活性,遠遠高于無GB(圖3c左)或加GB(圖3c右)的納米催化劑的質量活性,從而證實了應變和摻雜分別顯著提高了OER活性。這些結果清楚地證實了扭轉應變的GB-Ta0.1Tm0.1Ir0.8O2-δ顯著提高的酸性OER活性是應變和摻雜的協同結果。優化后的納米催化劑的OER活性高于目前報道的最先進的酸性OER電催化劑。此外,在循環伏安加速降解試驗中進一步進一步證實了GB-Ta0.1Tm0.1Ir0.8O2-δ納米催化劑在酸性OER中具有良好的穩定性。
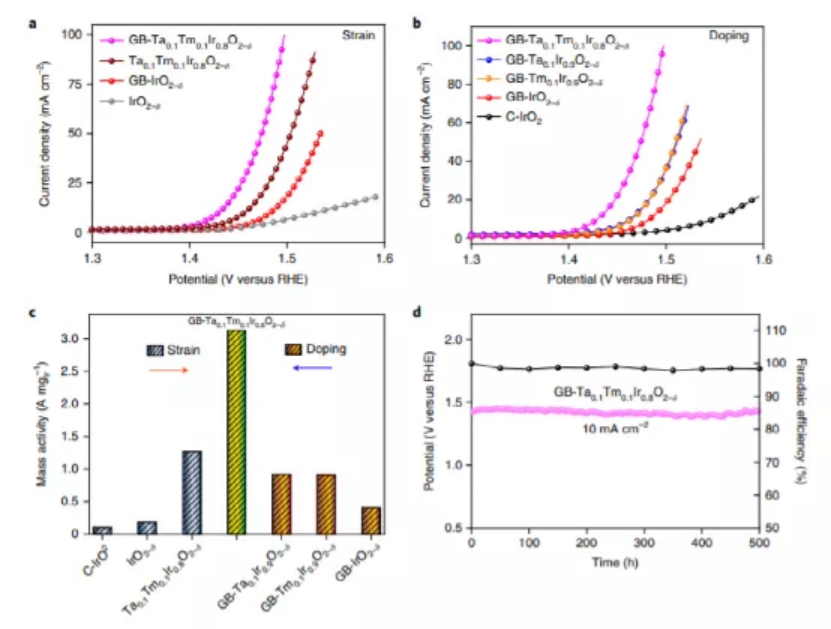
圖3 不同TaxTmyIr1?x?yO2?δ納米催化劑在0.5 M H2SO4電解質中的電催化性能
要點4 DFT計算
密度泛函理論(DFT)計算結果顯示,IrO2上的催化中間體的能量可以通過應變和摻雜誘導的配體效應來調節(圖4a),以增強電催化活性。此外,與Ta0.1Ir0.9O2-δ、Tm0.1Ir0.9O2-δ和IrO2相比,Ta0.1Tm0.1Ir0.8O2-δ的電位決定步驟的能量最低(圖4b),進一步,DOS結果顯示,在引入Ta和Tm后,催化劑的p帶中心分別向費米能級移動(圖4b),這表明摻雜效應調諧了活性中心的電子結構。因此,在IrO2結構中同時引入Ta和Tm可以調節電子結構,從而優化氧中間體在Ir位上的吸附。同時,GB-Ta0.1Tm0.1Ir0.8O2-δ的p帶中心中距離費米能級的能帶處于合適的位置(圖4c),表明扭轉應變的Ta0.1Tm0.1Ir0.8O2-δ具有與氧中間體的合適結合能。DFT計算結果表明,GB-Ta0.1Tm0.1Ir0.8O2-δ具有最低的OER能壘(圖4b)。同時,應變和摻雜協同效應使得GB-Ta0.1Tm0.1Ir0.8O2-δ的ΔG2 (= ΔGO - ΔGOH)更接近1.23 eV。這些結果表明,可以通過應變和摻雜相結合的方法來調節IrO2的非最佳氧結合能,從而調節催化勢壘,優化酸性OER催化活性。
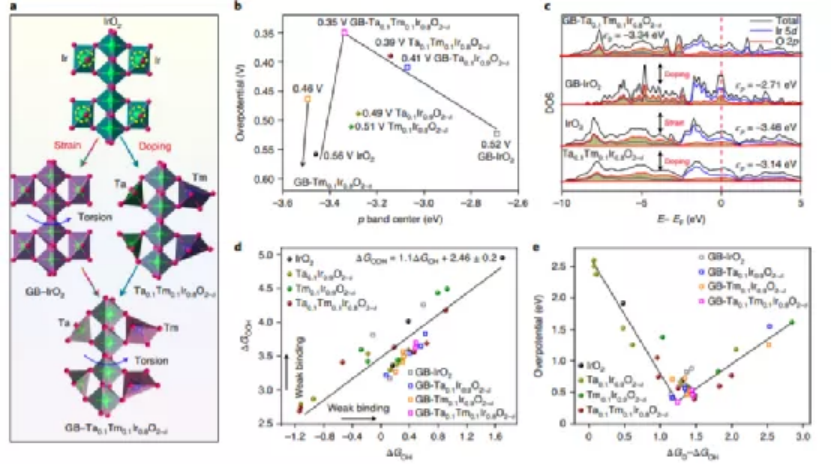
圖4 通過應變和摻雜調節IrO2-δ增強OER活性的DFT計算
要點5 PEM電解槽中的酸性OER性能
研究人員最后將優化后的GB-TaxTmyIr1?x?yO2?δ納米催化劑和對比催化劑應用于Nafion117膜的酸性(0.5 M H2SO4)質子交換膜電解槽中,其中催化劑的負載量為0.2 mg cm?2(圖5a)。在50 °C下的極化曲線表明,這些催化劑性能遵循GB-Ta0.1Tm0.1Ir0.8O2-δ > GB-Ta0.1Ir0.9O2-δ ≌ GB-Tm0.1Ir0.9O2-δ > GB-IrO2-δ。同時,使用GB-Ta0.1Tm0.1Ir0.8O2-δ(1.766V)達到1 A cm-2電流密度所需的電池電壓(1.766 V)低于GB-IrO2-δ(1.946V),GB-Tm0.1Ir0.9O2-δ(1.915V)和GB-Ta0.1Ir0.9O2-δ(1.897V)(圖5b)。此外,基于GB-Ta0.1Tm0.1Ir0.8O2-δ催化劑的質子交換膜電解槽在1.5 A cm?2時的裝置效率達到71%(圖5c)。同時,質子交換膜電解槽在1.5A cm?2下可運行至少500 h,性能沒有明顯的衰減(圖5d)。根據美國能源部(DOE)的計算,該PEM電解槽產生的1千克H2的估計成本約為US$1,遠低于每千克H2 US$2的目標。
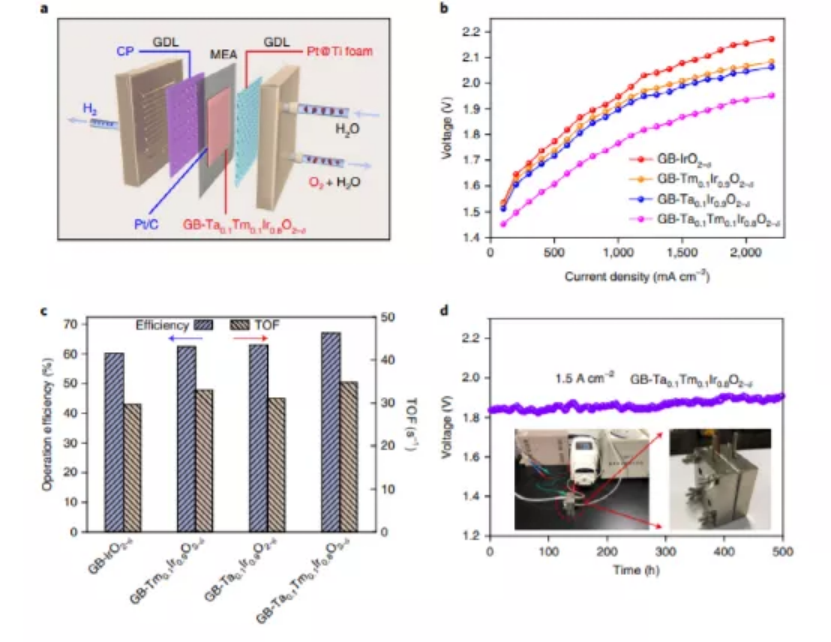
圖5 采用GB-TaxTmyIr1?x?yO2?δ納米催化劑作為陽極催化劑,在0.5 M H2SO4電解液中,50°C進行電解水
小結
1)提出了一種新型的扭應變Ta0.1Tm0.1Ir0.8O2-δ納米催化劑,由于晶界致應變和摻雜的協同作用,該催化劑對酸性OER表現出優異的活性和穩定性。
2)Ta0.1Tm0.1Ir0.8O2-δ納米催化劑的晶界應變主要扭轉調整了Ir–O鍵長,優化了活性位點Ir對氧中間體的吸附能并降低了OER的能壘,同時使催化劑保持了優秀的催化劑穩定性。此外,過渡金屬Ta和稀土元素Tm共摻雜IrO2-δ引起的摻雜效應也調整了活性位點的電子結構,優化了活性位點對催化中間體的結合能。
3)在工業運行條件下,這種新型扭轉應變Ta0.1Tm0.1Ir0.8O2-δ納米催化劑應用在了PEM電解槽中,實現了穩定的電解水制氫。
該項研究工作不僅僅展示了一種高效的OER納米催化劑來促進PEM電解槽的工業應用,而且還提出了一種使用扭應變納米結構催化劑來提高電化學和其他催化反應的催化活性的新策略。
參考文獻
Hao, S., Sheng, H., Liu, M. et al. Torsion strained iridium oxide for efficient acidic water oxidation in proton exchange membrane electrolyzers. Nat. Nanotechnol. (2021).
DOI:10.1038/s41565-021-00986-1
https://doi.org/10.1038/s41565-021-00986-1











