
第一作者:Wu Li?
通訊作者:雷愛文、Matthias Beller、Angelika Brückner
通訊作者單位:武漢大學、萊布尼茨催化研究所
同位素標記(特別是氘代標記),是發展新型藥物的重要手段,比如具體的用于代謝產物的鑒定和定量。因此人們發展了多種多樣的方法學能夠進行小批量合成選擇性氘代化合物。
目前,由于發展氘代化合物能夠作為活性藥物,因此人們對大規模分子氘代方法學非常感興趣。對于工業量級的氘代標記方法,需要發展可靠的、高活性、大規模合成方法學。

圖1. 氘代的應用及氫氘交換方法
有鑒于此,萊布尼茨催化研究所Matthias Beller和Angelika Brückner,以及武漢大學雷愛文等報道通過纖維素和Fe鹽合成的納米鐵催化劑能夠對苯胺類、酚類、吲哚類,以及其他雜環化合物通過D2O作為氘代試劑,在氫氣氣氛中選擇性的進行分子氘代標記。這種方法學具有容易大規模化合成的優勢,能夠進行千克量級大量合成氘代有機分子。反應中使用的催化劑具有空氣氣氛和水溶液穩定性,因此為高效率對有機分子進行氘代標記提供了一種直接有效的方法。

圖2. 雜芳烴選擇性氘代
研究背景
同位素標記是發展藥物分子和農藥的重要方法,比如在醫藥領域通常制備含同位素的活性藥物分子,用于理解分子的代謝過程,鑒定其中特定的代謝物分子。氘原子是最常見的同位素標記原子,對于研究切斷C-H、C-D鍵的動力學同位素效應(KIE)非常合適。與未標記的化合物相比,氘原子標記的化合物具有不同的分子量,因此能夠作為內標試劑用于LC-MS分析。因此合成氘代有機分子具有非常重要的意義。特別是對芳基/雜芳基/有機胺進行標記變的非常重要,因為這種結構在大量的有機分子中都存在。
酸介導H/D交換是最古老的芳烴標記方法,但是這種反應只能通過親電取代反應修飾結構簡單的芳烴。基于均相金屬催化C-H鍵活化,人們發展了一系列金屬有機催化劑,能夠對芳烴、脂肪胺的α,β位點進行H/D交換。比如Ir金屬的Crabtree或者Kerr催化劑能夠通過D2氣體進行C(sp2)-H化學鍵的同位素標記,Fe的金屬有機催化劑能夠通過D2或者T2對藥物活性分子的芳烴C-H鍵進行氘代或者氚代。最近MacMillan等發展了光催化同位素標記方法,能夠對N-烷基胺藥物分子標記。
除了光催化劑和有機金屬均相催化劑,異相貴金屬催化劑同樣發展能夠作為氘代標記催化,比如Pd/C和Pt/C催化劑能夠對芳烴或者雜芳烴進行H/D交換。Ru或者Ir催化劑也得到發展用于D2進行標記,展示了非常吸引人的標記能力。
新發展
目前除了Ni金屬,基本上目前發展的各種氘代標記異相催化劑都是基于貴金屬,因此發展非貴金屬催化劑具有更好的發展前景;同時,發展溫和的氘代試劑,比如更加便宜安全和操作方便的D2O替代D2,是非常好的發展方向。
萊布尼茨催化研究所Matthias Beller和Angelika Brückner,以及武漢大學雷愛文等報道發展了異相非貴金屬Fe基催化劑,對芳烴和雜芳烴實現了普適性的氘代反應。反應避免使用價格昂貴的D2,能夠在H2氣氛中以D2O作為氘代標記試劑,能夠對一些代表性的藥物和天然產物分子進行氘代反應。
反應情況
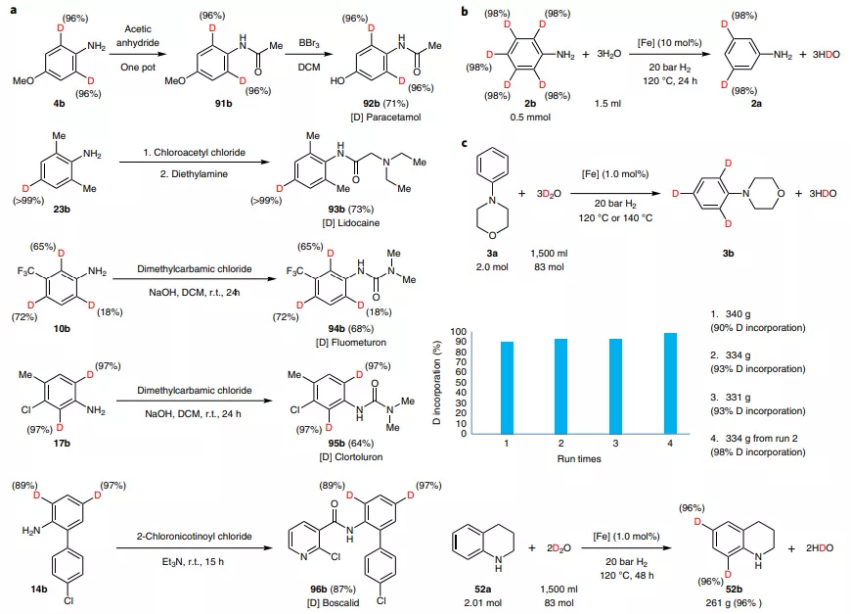
圖3. 催化反應
催化劑的制備。通過熱解Fe(NO3)3·9H2O和纖維素的混合物,得到高催化活性的選擇性氫化試劑。
催化反應。這種催化劑能夠對芳基環的鄰位和對位實現氘代,而且催化劑的性能比Pt/C、Au/C、Ru/C催化劑具有更好的催化活性。當反應在氫氣氣氛中進行,氫化反應的性能進一步提高。通過XPS表征催化劑在催化反應過程中的界面變化情況,發現催化劑的表面部分還原為Fe(0)。優化反應條件,該反應能夠在120 ℃的氫氣中進行反應,以D2O作為氘代試劑,實現接近100 %的轉化。
反應機理
通過動力學同位素效應(KIE)、ESR對反應機理進行研究,對比實驗結果顯示,H2O的反應速率比D2O的反應速率高4倍,在氘代反應的決速步驟是D-OD切斷。通過對比苯胺、3,5-二氘代苯胺的氘代反應,發現微弱的二級KIE效應,這種區別來自于氘代與非氘代底物之間的配位環境有微弱區別導致。
通過ESR表征該反應是否通過自由基機理過程進行,發現使用DMPO自旋捕獲劑,監測發現捕獲··OD的DMPO-OD產物信號,說明催化劑能夠促進一部分D2O分子以均裂方式切斷D-OD。
通過相關表征提出反應的可能機理。首先催化劑以均裂方式切斷D2O分子的D-OD化學鍵,生成的自由基物種吸附在催化劑表面轉化為D*和OD*,隨后與底物分子進行反應,*OD能夠與芳環的氫反應生成HDO,生成苯環自由基,隨后苯環自由基與D*生成氘代芳基產物。該反應中表現的鄰位/對位選擇性來自于電子濃度較高的鐵催化劑能夠向界面吸附芳烴傳遞電子濃度,因此能夠促進親電反應,實現鄰位/對位取代。
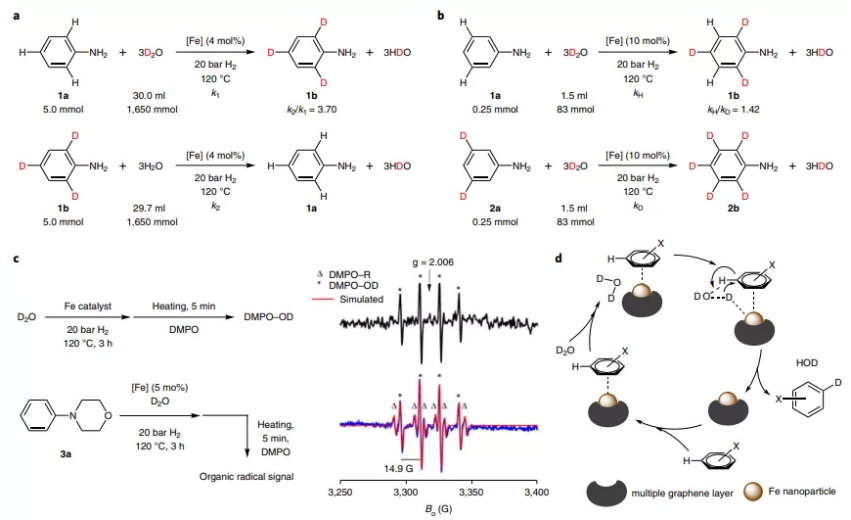
圖4. 催化反應機理
參考文獻及原文鏈接
Li, W., Rabeah, J., Bourriquen, F. et al. Scalable and selective deuteration of (hetero)arenes. Nat. Chem. (2022).
DOI: 10.1038/s41557-021-00846-4
https://www.nature.com/articles/s41557-021-00846-4











