免疫系統 T 細胞的任務是識別和破壞體內已感染入侵病原體的細胞。CAR T細胞是專門設計用于識別癌細胞并摧毀它們的 T 細胞。CAR T細胞已經在臨床上用于治療淋巴瘤,許多臨床試驗正在進行中,以評估 CAR T 細胞治療對其他形式癌癥的使用。
CART 細胞療法在對抗表達 CD19 的 B 細胞惡性腫瘤方面取得了前所未有的成功,這一成功已獲得 FDA 的兩項批準,并激發了數百項正在進行的臨床試驗。然而,盡管 CAR T 細胞療法在治療人類惡性腫瘤方面具有革命性的潛力,但與生產臨床級 CAR T細胞相關的復雜程序和成本是廣泛臨床應用的主要障礙。
治療性 CAR-T 細胞的制造需要一系列廣泛的步驟,包括:
(1)通過白細胞分離術從患者身上收集 T 細胞并將其運送到制造中心;
(2) 在良好生產規范條件下使用病毒載體激活、擴增和改造 T 細胞的勞動密集型程序;
(3) 生產細胞的質量控制;
(4) 將最終的CAR-T 細胞產品運送到醫院并重新輸注到患者體內。整個制造過程的成本可能高達 50 萬美元,并且可能需要數周時間。
這也導致了CAR T 細胞治療的一個主要缺點是它非常昂貴——每劑數十萬美元(約120萬RMB)。由于其成本,許多人被排除在這種治療之外。
因此,全球都迫切希望解決與制造時間和成本相關的 CAR T 治療挑戰。
鑒于此,北卡羅來納大學教堂山分校/北卡羅來納州立大學Yevgeny Brudno等研究人員描述了一種用于 T 細胞工程和釋放的可植入多功能藻酸鹽支架(Multifunctional Alginate Scaffold for T Cell Engineering and Release, MASTER),它簡化了體內 CAR-T 細胞的制造并將處理時間從幾周縮短到一天。

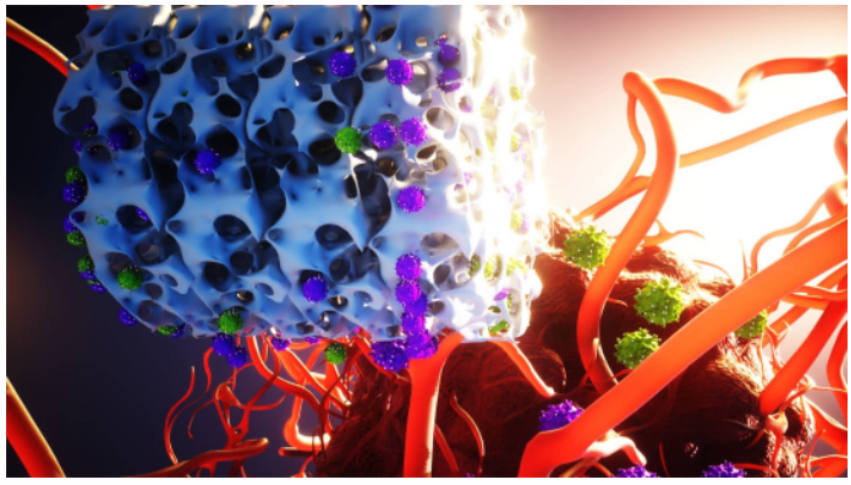
設計目的
MASTER可以直接裝載患者來源的 T 細胞和編碼 CAR 的病毒顆粒,并在同一天植入以在體內生成 CAR-T 細胞。MASTER技術旨在 (1) 裝載T細胞和病毒顆粒;(2)刺激T細胞活化和增殖;(3)促進T細胞轉導;(4) 局部擴增 CAR-T細胞和 (5) 可持續釋放功能齊全的 CAR-T細胞以控制腫瘤生長。
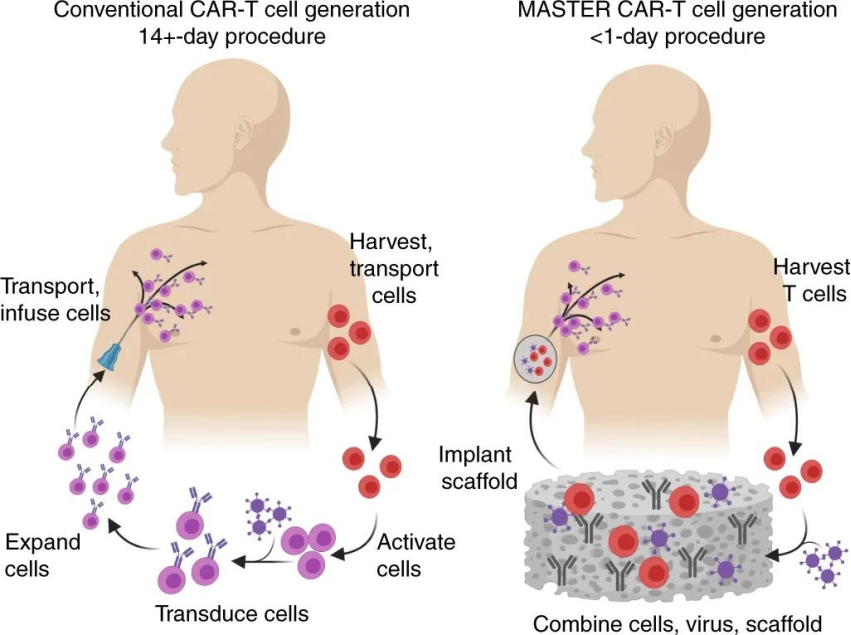
圖|兩種技術對比
材料構建
海藻酸鹽因其生物相容性、生物降解性、溫和的凝膠化要求以及作為細胞培養的三維 (3D) 結構的廣泛應用而被選為該多功能支架 (MASTER) 的基礎。最初需要在支架中使用大孔,以便為細胞和逆轉錄病毒(RV)之間的有效接觸提供界面,隨后將營養物質大量轉移到增殖的 CAR-T 細胞。在 MASTER 中通過溫和的冷凍凝膠化實現了大孔隙率。
為了促進支架內的 T 細胞活化,環辛炔偶聯的抗CD3和抗CD28抗體通過溫和有效的無銅點擊化學固定在疊氮化物修飾的海藻酸鹽上。此外,為了激活和擴展支架內的 T 細胞,細胞因子 IL-2 被物理封裝在支架中,物理封裝使IL-2 能夠在 5 天內持續釋放,同時保持釋放的 IL-2 的生物活性。植入后,這些白細胞介素開始滲出,促進 CAR-T 細胞的快速增殖。

圖|MASTER 促進原代人 T 細胞的活化和逆轉錄病毒介導的轉導
生物指導性支架可作為體內CAR-T 細胞工廠
研究人員經過體內淋巴瘤異種移植腫瘤模型,在淋巴瘤再攻擊模型和更成熟的淋巴瘤腫瘤模型進行了體內抗腫瘤研究,在前倆個模型中,MASTER在控制腫瘤生長和顯著提高存活率方面更有效。在挑戰MASTER極限的更成熟的淋巴瘤腫瘤模型中,發現使用 MASTER 生產的 CAR-T 細胞在控制腫瘤生長方面同樣與傳統 CAR-T 細胞具有相同的功能,但具有更好的擴增和持久性。值得注意的是,MASTER 大大降低了 CAR-T 細胞生產的時間、復雜性和成本。

圖|皮下植入的 MASTER 在淋巴瘤異種移植模型中產生并釋放功能齊全的 CAR-T 細胞

圖|在淋巴瘤的再攻擊模型中,皮下植入的 MASTER 優于靜脈注射的 CAR-T 細胞
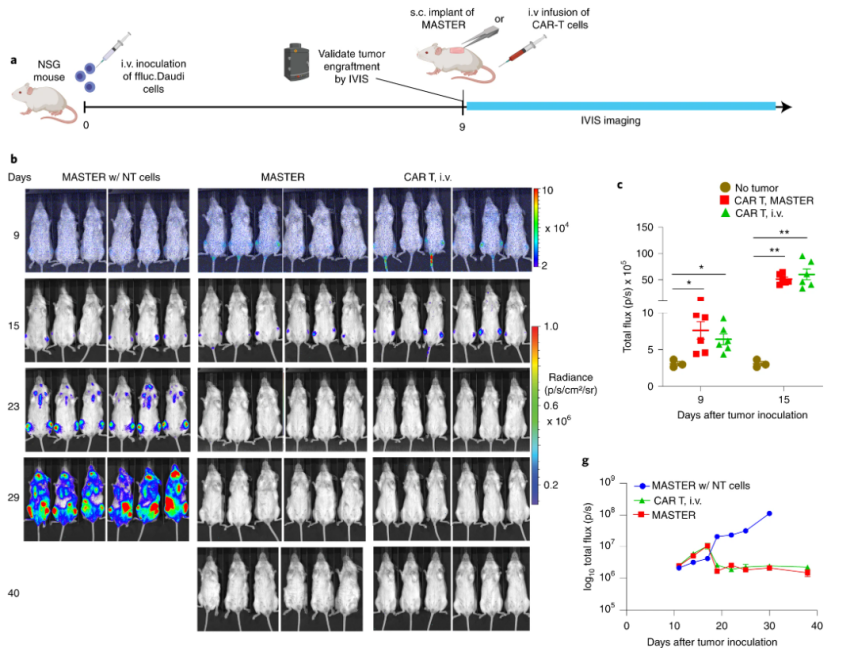
圖|MASTER 和常規 CAR-T 細胞對體內已建立的腫瘤表現出相同的抗腫瘤功效
小結:
綜上所述,本文介紹了一個多功能支架,將 CAR-T 細胞制造和遞送的關鍵方面整合到一個平臺下,將 CAR-T 細胞制造的整個過程縮短到一天。該支架使用 FDA 批準的非免疫原性材料,為 αCD3 介導和 αCD28 介導的細胞活化和白介素介導的增殖創造了一個局部的培育環境。
MASTER提供了一種模塊化平臺技術,可用于重新編程其他免疫細胞或提供免疫調節因子以協同支持細胞功能。除了其在癌癥治療方面的潛力之外,MASTER 技術可能會激發新的治療方法,利用重新編程和釋放治療細胞的能力。
參考文獻:
Agarwalla,P., Ogunnaike, E.A., Ahn, S. et al. Bioinstructive implantable scaffolds forrapid in vivo manufacture and release of CAR-T cells. Nat Biotechnol (2022).
https://doi.org/10.1038/s41587-022-01245-x











