可充電鋰離子電池是以兩種不同的能夠可逆地插入及脫出鋰離子的嵌鋰化合物分別作為電池的正極和負極的二次電池體系。
從最根本的定義來說:發生氧化反應的是陽極,發生還原反應的是陰極;電勢高的是正極,低為負極。正負極是固定不變的,充放電過程不同,陰陽極則會發生變化。一般原電池說正負極,電解池說陰陽極,所以電池記正負極就好。
陽極(Anode):失電子被氧化。
陰極(Cathode):得電子被還原。
正極(Cathode):電勢高的一邊。
負極(Anode):電勢低的一邊。
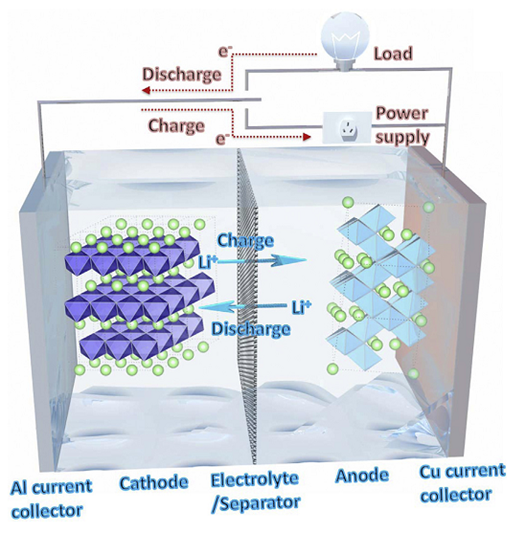
充電時
鋰離子從正極材料的晶格中脫出,經過電解質后插入到負極材料的晶格中,使得負極富鋰,正極貧鋰;
充電過程可當做電解池:正極=陽極。
電解是被動過程,汲取能量,和原電池互為逆反應,陽極失電子,發生氧化反應,陰極得電子,發生還原反應。
放電時
鋰離子從負極材料的晶格中脫出,經過電解質后插入到正極材料的晶格中,使得正極富鋰,負極貧鋰。
放電過程可當做原電池:正極=陰極。
原電池是自發過程,釋放能量,正極得電子,發生還原反應,負極失電子,發生氧化反應,電子從負極到正極,電流從正極到負極;
這樣正負極材料在插入及脫出鋰離子時相對于金屬鋰的電位的差值,就是電池的工作電壓。











