甲烷(CH4)中C-H鍵的活化是催化劑的主要目標。基于過渡金屬配合物和多金屬氧酸鹽的均相催化劑可以激活CH4中的C-H鍵。這些催化體系嚴重依賴腐蝕性很強的試劑,如硫酸和三氟乙酸,以穩定反應的CH4,從而對環境產生重大影響。此外,需要高壓(通常>20bar)才能使足夠的CH4溶解在溶液中。受自然界中CH4單加氧酶的啟發,鐵或銅交換沸石被應用于促進CH4中C-H鍵的活化。然而,這些工藝需要高溫和高壓,因此屬于高耗能。雖然過氧化氫的使用可以在較溫和的條件下推動預期的反應,但其高昂的成本阻礙了大規模應用。另一方面,O2是一種廉價的、容易獲得的氧化劑,但經常導致CH4過度氧化為CO2作為主要產物。
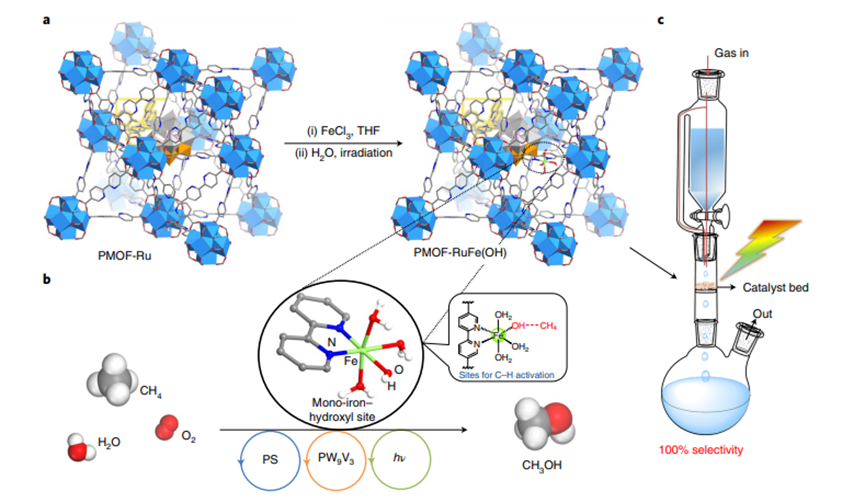
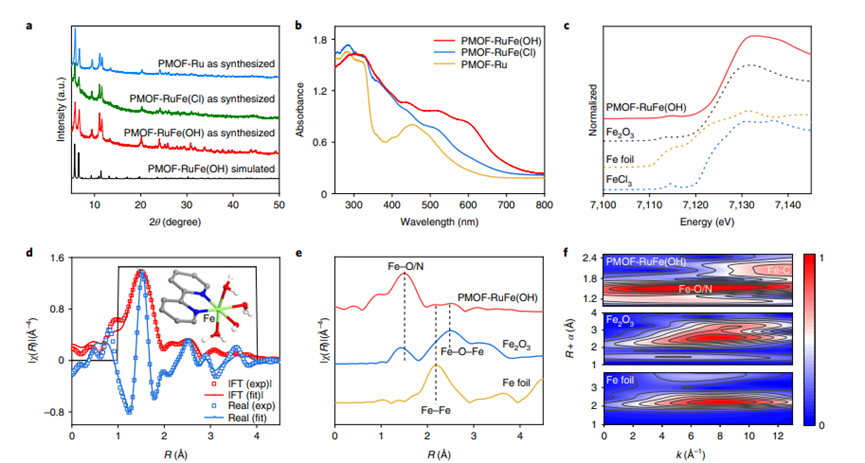
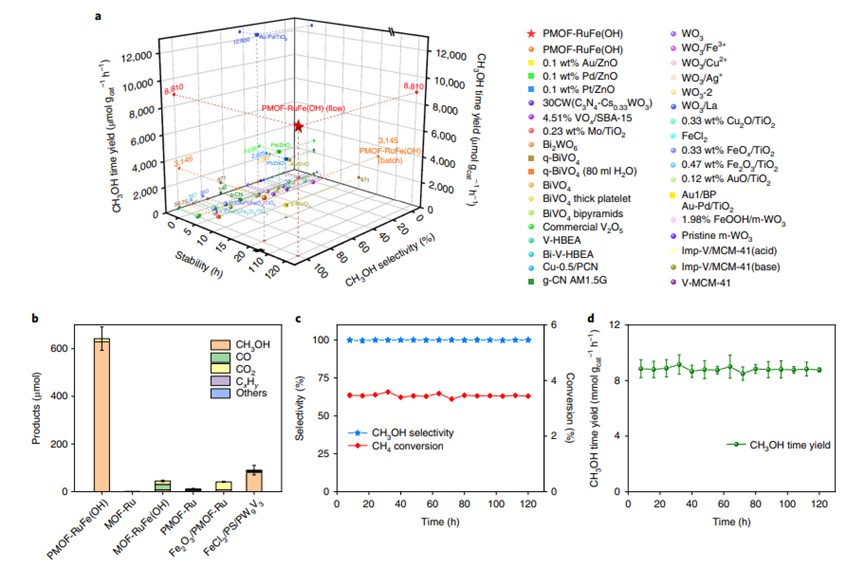
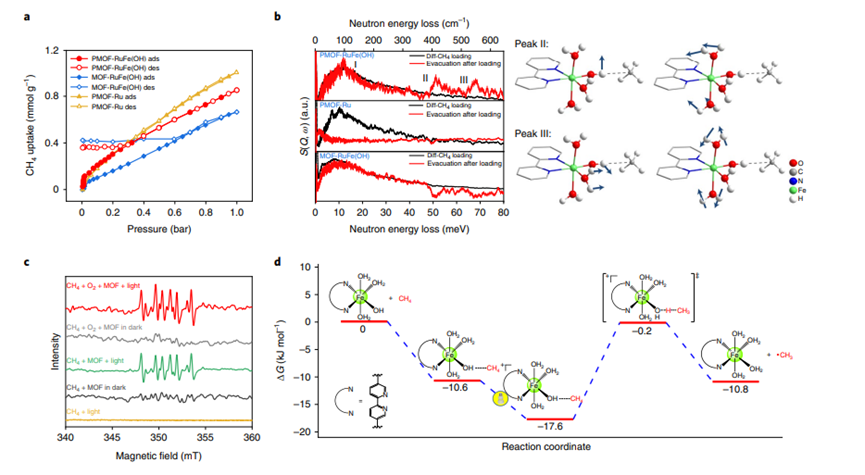
以BiVO4、WO3或TiO2和ZnO負載貴金屬(如Au、Ag、Pt、Pd)的催化劑在室溫下可促進CH4的活化。錨定催化活性中心的多孔金屬-有機骨架(MOFs)材料可以作為CH4活化的熱催化劑,盡管高溫和壓力仍然是催化C-H鍵活化的關鍵。迄今為止,在MOF催化劑上還尚未實現光催化CH4部分氧化。近日,曼徹斯特大學楊四海教授,Martin Schr?der報道了在金屬-有機骨架,PMOF-RuFe(OH)中錨定的單鐵羥基中心上CH4的直接光氧化。通訊作者:楊四海, Martin Schr?deri)集成多組分的光催化系統可以協同支持觀察到的催化性能。研究人員在環境條件下,以H2O和O2為氧化劑,在MOF中的單鐵羥基中心上,實現CH4直接光氧化為CH3OH的高效反應。ii)基于operando光譜和計算技術,研究人員發現受限的單鐵羥基位點通過形成[Fe–OH???CH4]中間體結合CH4,從而降低了C–H鍵活化的勢壘。i)在存在H2O和O2的環境和流動條件下,CH4以100%的選擇性轉化為CH3OH,時間產率為8.81±0.34 mmol gcat-1 h-1(相比之下,甲烷單加氧酶的時間產率為5.05 mmol gcat-1 h-1)。ii)使用CH4的這種直接光化學方法和通過使用商業Cu/ZnO/Al2O3催化劑的合成氣(CO/CO2/H2)的最新工業工藝合成CH3OH進行經濟分析比較,突出了PMOF-RuFe(OH)在實際應用中的巨大前景。研究人員選擇UiO-67作為光催化劑的功能平臺來整合光催化劑的三個關鍵成分:吸收光的光敏劑(PS),[RuII(bpy)2(bpydc)] (L), (bpy: 2,2′-bipyridine; H2bpydc: 2,2′-bipyridine-5,5′-dicarboxylic acid)、激活O2的多電子氧化還原活性聚釩酸鹽([PW9V3O40]6?,PW9V3)以及激活CH4的單鐵羥基位點(圖1a)。在一鍋合成中將PS和PW9V3結合到多孔UiO-67中以產生PMOF-Ru,然后通過用FeCl3·6H2O的合成后金屬化引入鐵位點以產生PMOF-RuFe(Cl),(((PW9V3)0.1@Zr6(μ3-O)6.1(μ3-OH)1.9(H2O)0.24(bpydc)3.7[(bpydc)FeCl2(THF)2]1.9(L)0.28)。結合熱重分析和元素分析,通過核磁共振、紅外(IR)和XAS (X射線吸收)光譜,并通過考慮電荷平衡,確定了PMOF-RuFe(Cl)的結構。此外,還通過非彈性中子散射(INS)和密度泛函理論(DFT)計算確定了PMOF-RuFe(Cl)的結構。圖1. CH4光氧化制CH3OH的PMOF-RuFe(OH)催化劑和流動反應器的設計與合成粉末X射線衍射圖案和掃描電子顯微鏡(SEM)圖像證實了PMOF-RuFe(Cl)保留了UiO型結構和形態(圖2a),同時由于金屬到配體的電荷轉移,在UV-vis光譜中以370 nm為中心的明顯吸收帶證實了FeIII與bpydc2-的結合(圖2b)。在水中用光預處理PMOF-RuFe(Cl)2小時時,生成活性催化劑PMOF-RuFe(OH),與PMOF-RuFe(Cl)催化的CH3OH形成的誘導期一致。PMOF-RuFe(OH)的擴展X射線吸收精細結構(EXAFS)光譜與扭曲的八面體配合物[(bpy)Fe(OH)(H2O)3]2+完全一致。研究人員以CH4/O2(v/v=1/1,1atm)為原料,在25 °C的可見光(λ=400-780 nm)照射下,首次考察了催化劑的光催化性能。結果顯示,PMOF-RuFe(OH)作為唯一的液體產物,光照20 h后CH3OH產量為629±68 μmol,CH3OH的產率是3145±340 μmol gcat?1 h?1,累積的Fe周轉數(Fe-TON)為135±16。優于當前所有最先進的催化劑(圖3a)。在常溫下,以水和氧氣為氧化劑,PMOF-RuFe(OH)催化劑對甲醇的選擇性為98%,生成的溶液中甲醇的濃度為210 mmol l?1。使用13C標記的13CH4的反應只獲得13CH3OH的唯一產物,并且在不存在CH4的情況下進行的實驗沒有產生含碳產物。因此,CH4是這些實驗中唯一的碳源。對照實驗:(1)不加任何催化劑;(2)無光;(3)無光但加熱至100 ℃:都產生可忽略的產物,證實了反應的光催化特性。研究人員接下來研究了缺少三種整合組分中的一種或兩種的材料的催化性能,以及這些不同組分的物理混合物。基于此,制備了MOF-Ru(具有PS [RuII(bpy)2(bpydc)]但沒有PW9V3的UiO-67)、MOF-RuFe(Cl)和MOF-RuFe(OH),并對其進行了表征和研究。結果在所有可能的情況下,只獲得了微量的CH3OH(圖3b)。此外,也檢測了Fe2O3納米顆粒和Fe2O3/PMOF-Ru,但是沒有得到產物,因此排除了Fe2O3納米顆粒作為活性物質的可能性。因此,三個組分在PMOF-RuFe(OH)中的位點錨定和它們之間的協同作用共同導致了高光催化活性。研究人員接下來確定CH4分子的結合位點。PMOF-RuFe(OH)和MOF-RuFe(OH)中CH4的吸收等溫線(即在沒有PW9V3的情況下)也都表現出對CH4的強烈吸附,表現為最初的急劇上升和明顯的滯后解吸(殘渣為0.5 CH4/Fe)。而在PMOF-Ru中沒有觀察到這種行為(圖4a),這表明單FeIII物種是CH4的結合位點。此外,通過INS光譜和DFT計算來直接可視化CH4在該體系中的結合動力學(圖4b)。當PMOF-RuFe(OH)中CH4處于低負載(0.22和0.45 CH4/Fe)時,由于CH4分子吸附的振動和反沖,其在<40 meV處的強度增加。峰II(50-55 meV)和III(65-70 meV)歸因于MOF吸附CH4的INS強度的變化,特別是(i)H垂直和平行于[(bpy)Fe-OOH]平面移動的-OH基團的振動,(ii)位于[(bpy)Fe-OOH]平面之外和之內的H2O搖擺模式,(iii)位于[(bpy)Fe-OOH]平面的H2O搖擺模式和H垂直于O-H移動的OH的振動(圖4b)。DFT計算表明[(bpy)Fe(OH)(H2O)3]2+與CH4在PMOF-RuFeOH)中的相互作用主要基于氫鍵(Fe–OH???CH4 = 2.39?)。研究人員結合DFT計算的EPR光譜自旋俘獲實驗獲得了對C–H活化過程的進一步認識。在水中加入DMPO后,經CH4加載的PMOF-RuFe(OH)的EPR譜顯示了典型的DMPO-CH3自由基加合物的典型信號,表明在光誘導下形成了甲基自由基(圖4c)。還觀察到一種次要成分,DMPO-OH,推測是由于水的分解。相比之下,在沒有催化劑的情況下或者如果反應在PMOF-Ru上進行,則沒有觀察到自由基加合物(圖4c)。這表明吸附在Fe-羥基位點的CH4達到了較低的能量態,降低了?CH3自由基形成的活化勢壘(圖4d)。有趣的是,DFT計算表明,自由基并不是完全“游離”的,而是被Fe-羥基位點穩定化,形成Fe(OH2)????CH3相互作用[HH2O???CCH3 = 2.02?],從而嚴重抑制C-C偶聯反應。研究人員指出,光催化循環是由[Ru(bpy)2(bpydc)]*激發態PS*的光誘導電子轉移引發的,以產生還原的PW9V3IV/V,這得到了原位EPR光譜、光致發光和電化學研究的證實。光電流響應和電化學阻抗譜研究證實,與部分功能化的體系相比,PMOF-RuFe(OH)中的電荷分離效率顯著提高。富含電子的PW9V3IV/V然后通過質子耦合(來自H2O)電子轉移驅動O2到H2O2的光還原,并且在O2存在下照射PMOF-Ru 5小時后可以檢測到H2O2。相反,在PMOF-RuFe(OH)上沒有檢測到H2O2,這是因為在光照下,原位生成的H2O2迅速轉化為被{Fe-OH}部分促進的·OH自由基。因此,C-H活化通過吸附的CH4與單鐵羥基部分相互作用的途徑進行,并容易被氧化成由鐵中心穩定的·CH3自由基。然后通過·CH3和·OH自由基偶聯生成CH3OH,并用水從MOF中提取。而CH3OH的高選擇性歸因于其在有水存在的情況下在MOF基質中的吸附相對較弱而快速脫附。此外,光照射有效地猝滅·OH中間體,以避免CH3OH的過度氧化。而為了實現CH3OH的最佳生產,循環內的所有組成部分(即MOF、光敏劑、多釩鎢酸鹽和單鐵羥基)必須協同工作。UiO-67則提供了一個穩定的平臺來實現這種協同作用,以提供比含有雙鐵中心的可溶性甲烷單加氧酶更高的活性。在觀察到PMOF-RuFe(OH)高活性的基礎上,研究人員開發了一種連續流動光氧化過程,其中流動的CH4/O2-飽和水(15 ml h?1)在照射下通過PMOF-RuFe(OH)催化劑的填充層(圖1C)。重要的是,在PMOF-RuFe(OH)上反應的CH4既包括水溶的CH4,也包括通過滴管分支的部分氣態CH4。因此,這創造了一個動態的氣/固/液界面,以最大限度地增加CH4、O2、H2O與催化劑之間的接觸。采用這種簡單的裝置,在水中得到了唯一的選擇性為100%的CH3OH,累積的Fe-TON為2269±88,催化劑在120 h內具有很高的穩定性。因此,在完全環境條件下獲得了前所未有的8.81±0.34 mmol gcat?1 h?1(或18,908±730 mmol molFe?1h?1)CH3OH時間產率。1)CH4是一種非常豐富的碳基能源,但作為一種溫室氣體,它對環境有重大影響。而CH4直接光轉化產物CH3OH是一種液體燃料和碳原料,是利用這種碳原料的重要替代途徑。然而,這是一個極具挑戰性的過程,CH4通常會過度氧化為CO2。2)這項研究展示了PMOF-RuFe(OH)將單鐵羥基限制在多孔金屬-有機骨架中,與光活性受體相連,可以激活CH4中的C-H鍵,實現了在不使用H2O2的情況下驅動CH3OH的直接光合作用。3)未來的研究工作將致力于實際的高催化穩定性和高轉化率的光氧化CH4制CH3OH。An, B., Li, Z., Wang, Z. et al. Direct photo-oxidation of methane to methanol over a mono-iron hydroxyl site. Nat. Mater. (2022).DOI:10.1038/s41563-022-01279-1https://doi.org/10.1038/s41563-022-01279-1