特別說明:本文由學研匯技術中心原創撰寫,旨在分享相關科研知識。因學識有限,難免有所疏漏和錯誤,請讀者批判性閱讀,也懇請大方之家批評指正。
原創丨愛吃帶魚的小分子
編輯丨風云
現實與挑戰
固體催化劑具有容易與液態產品分離的特性,可以顯著降低制造成本,因此目前,固體催化劑催化反應占全球工業化學品制造流程的80%以上,基于固體催化劑(即非均相催化劑)的改進也一直是學術和工業化學研究的主題。但受限于非均相催化劑不理想的選擇性,一些重要的工業過程仍然使用可溶性(均相)催化劑。
此外,由于非均相催化劑(特別是負載型催化劑中的雙功能活性位點)潛在活性位點結構的分布、動態重構和所需的非平均場動力學描述復雜,闡明非均相催化劑的功能反應機制仍具有挑戰性。例如,在金屬氧化物沉積在金屬納米顆粒上時形成的界面處,或通過控制金屬納米顆粒在由納米顆粒形成的復合催化劑中的負載和定位時,由于活性位點的潛在結構沒有很好地定義,也因為活性位點在反應過程中會發生結構變化,通常很難闡明反應機制。

解決方案
基于此,美國加州大學圣巴巴拉分校Insoo Ro和Phillip Christopher教授報告了一種固體催化劑,合成負載型原子分散的銠-鎢氧化物(Rh-WOx)對位點催化劑克服了這些限制,表明了可以通過建立配對位點克服這些限制。
通過對位點結構的相對簡單性和平均場建模的充分描述使實驗動力學與基于第一原理的微動力學模擬相關聯。Rh-WOx對位點通過雙功能機制催化乙烯加氫甲酰化,包括:
1)Rh輔助WOx還原,從而與乙烯分子結合;
2)乙烯從WOx轉移到Rh和一個氫分子(H2)在銠和(iii)WOx之間的界面處解離成兩個氫原子。
這一系列過程啟動了配對位點,使一氧化碳分子能夠插入到結合的乙烯中,從而形成丙醛。催化劑的雙功能行為還取決于Rh-WOx界面的幾何形狀、反應過程中重新配置對位點配位的能量學以及在對位點的活性中心之間轉移分子的能力。在該反應中(氣相乙烯羰基化反應)中可以實現0.1?g cm-3 h-1的形成率下的>95%丙醛選擇性。
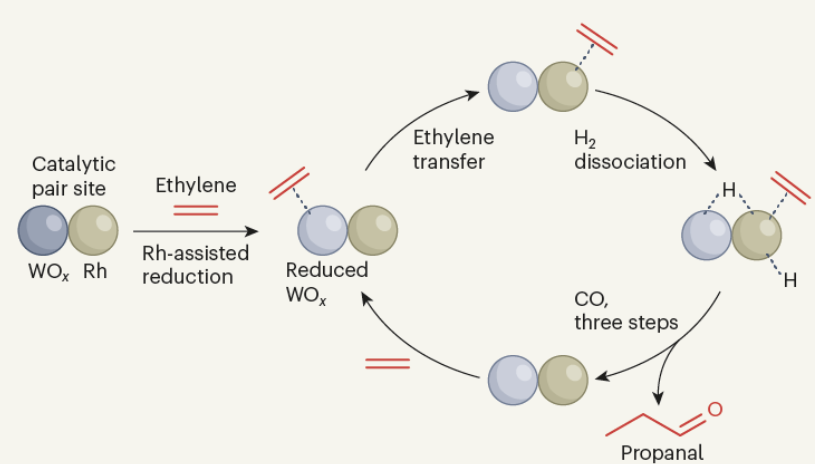
圖1. 催化對位點促進加氫甲酰化反應示意圖
【你若在,我必相隨。你離不開我,我離不開你,這不就是愛情的味道嗎?】
重要結論
單原子催化劑由分散在非催化固體(載體)上的單個金屬原子或化學物質(活性位點)組成。該研究開發的催化劑類似于單原子催化劑,但涉及兩種類型的活性位點,這兩個催化位點可以促進催化循環中的不同步驟并共同定位以形成稱為對位點的孤立對。因此,每一對位點都是雙功能的——它的兩個活性中心協同工作以催化反應的不同步驟。
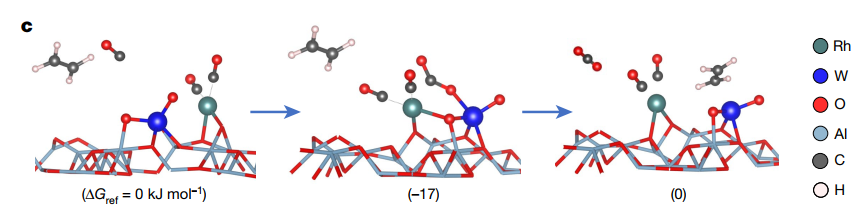
圖2:Rh-WOx對位點催化反應過程及機制
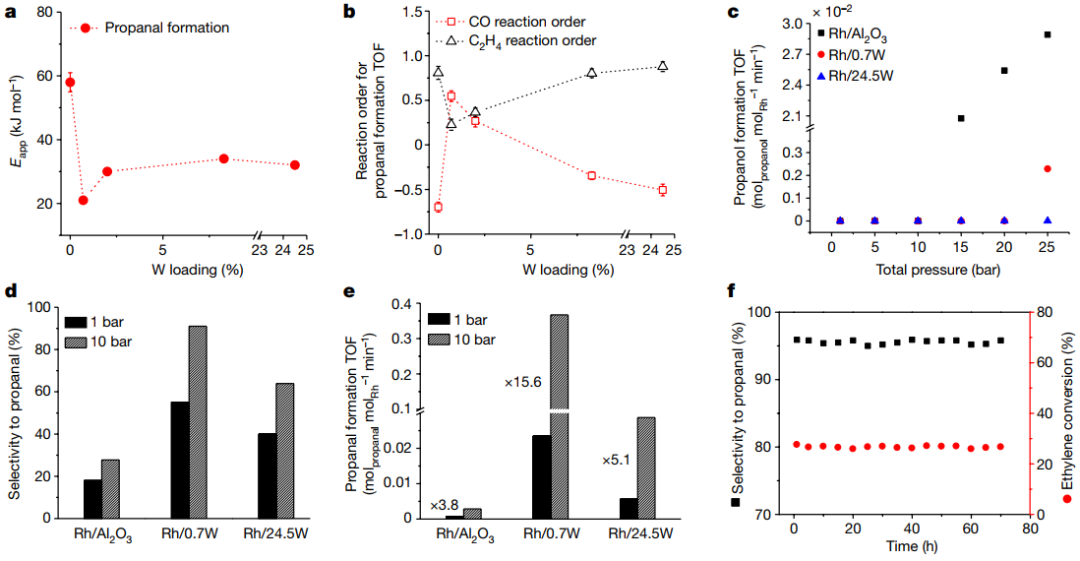
研究人員發現催化劑結構取決于WOx負載量。當負載量為0.7?wt%時,WOx以孤立物質的形式存在;在2?wt%的負載下,也會形成二維低聚物(少量WOx物質的簇);和負載量大于8?wt% 時形成3D WOx結構。表征表明,原子分散的Rh-WOx對位點的產生量為0.7?wt% WOx(圖3)。各種催化劑結構各自對乙烯加氫甲酰化表現出不同的催化性能。Rh-WOx對位點具有最好的反應活性,比具有2D低聚物和3D結構的催化劑促進了更高的反應速率和產物選擇性,這是由于銠和WOx活性位點協同工作的結果。
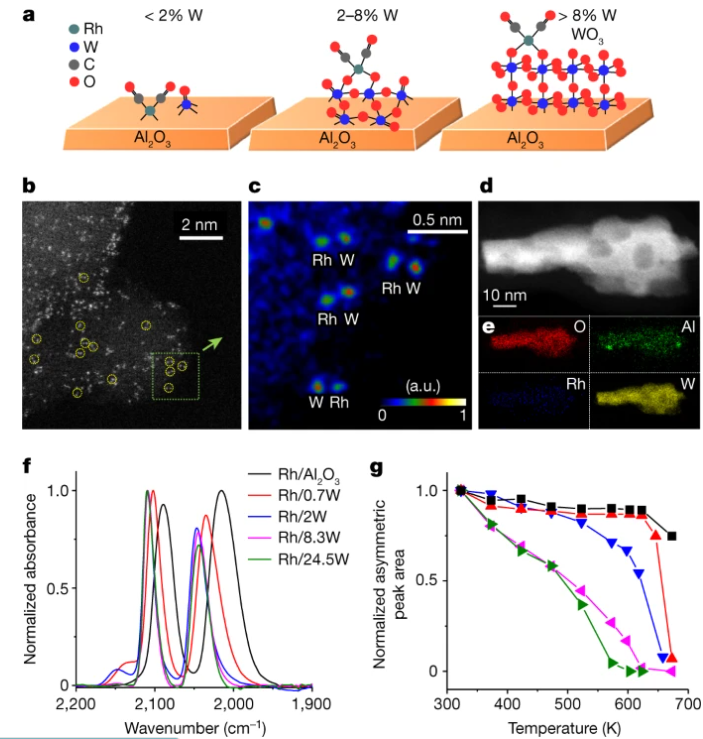
圖3:原子分散的Rh與具有不同結構的WOx的配位