口服胃腸道給藥由于其患者依從性高,無創性,簡單性和低成本,一直是藥物給藥最廣泛使用的方法之一。盡管口服藥物制劑具有潛在的優勢,但在胃腸道內仍面臨一些障礙,包括藥物在胃液的穩定性差,以及與腸道內壁的相互作用有限。而微馬達代表的一類納米機器人使用是主動運輸藥物到特定部位的一種有希望和有效的方法。各種合成微馬達,能夠推進到體內難以到達的位置,用于活性藥物輸送和其他生物醫學應用,包括生物傳感和顯微外科手術。基于化學反應的微馬達雖然可以有效提高輸送效率,但其使用壽命較短,限制了它們的滯留能力,從而導致藥物生物利用度降低。為了解決這一限制,需要開發具有改進特性的基于活性微運動的胃腸道藥物遞送系統。
近日,美國圣地亞哥分校的特聘教授Joseph Wang和張良方教授等人9月份在Nature materials(Joseph Wang/張良方教授最新Nature Materials!)發表藍衣藻載藥納米機器人用于細菌性肺炎治療的相關工作后,僅僅一周后,他們又在Science Robotics上發表了載藥藍藻納米機器人膠囊用于胃腸道疾病治療的工作。這是一種基于藻類的高效運動平臺,該平臺利用天然微藻在腸液中的快速和持久的游泳行為來延長藥物胃腸道內的局部潴留。

設計理念:
作者團隊選藍衣藻C. reinhardtii作為在胃腸道中主動遞送的納米機器人,因為它具有許多有吸引力的特性,包括細胞相容性,在各種水環境中具有良好的適應性和運動性,高豐度的可用于功能化的表面基團,以及易于在體內跟蹤的自發熒光。為了保護藻類馬達免受惡劣的胃環境的影響,將它們嵌入一個膠囊內以實現保護,該膠囊的內部為疏水涂層來儲存維持藻類活力的水溶液,其外部為pH響應型腸溶聚合物涂層。從膠囊中釋放出來后,藻類在腸液中顯示出穩定的運動,并且在體溫下保持運動超過12小時。這種長時間的運動其搭載阿霉素(Dox)在腸道分布得到顯著改善,并且延長了Dox的滯留時間。
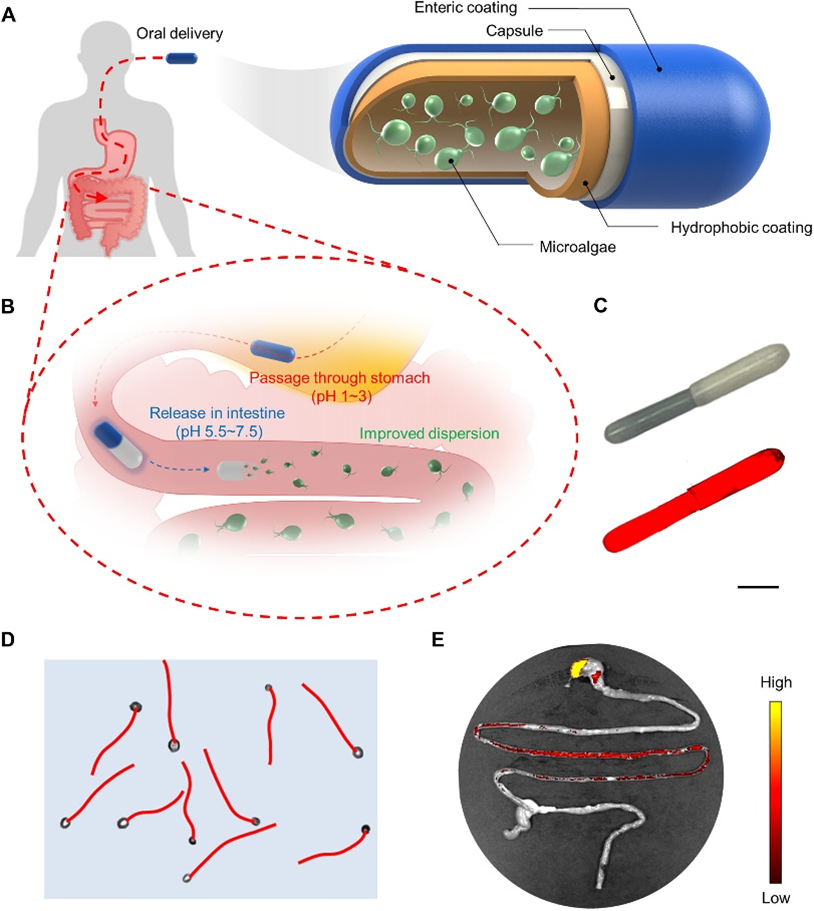
圖|示意圖
模擬腸液中藍衣藻納米機器人的微運動:
首先研究了藍衣藻的運動特性,并將它們與先前報道的Mg馬達的運動特性進行了比較。在模擬腸液(SIF)中,藍衣藻納米機器人表現出約120μm / s的穩定速度曲線,持續至少12小時。這種運動行為歸因于藻類鞭毛的協調、持續運動。而Mg馬達在推進過程中的快速溶解和耗竭,最后在15min之后停止運動。
為了證明它們具有藥物遞送的潛力,用兩種不同的藥物負載在藍衣藻納米機器人上:熒光染料和聚合物納米顆粒(NPs)。綠色染料熒光素化學共軛到藻類表面,對藻類進行熒光跟蹤。從100個單獨的藻類計算的中位速度幾乎與未修飾的藻類相同。同樣,紅細胞(RBC)膜包被的聚乳酸-共乙醇酸(PLGA)NPs通過點擊化學與藻類相連。同樣的NP負載的納米機器人在SIF中表現出相似的游泳模式和速度分布曲線。這里的數據證實,從小分子到NP的不同有效載荷可以成功地加載到藻類馬達上,而不會影響它們的推進特性,進一步突出了基于藻類的運動馬達系統的主動遞送藥物潛力。
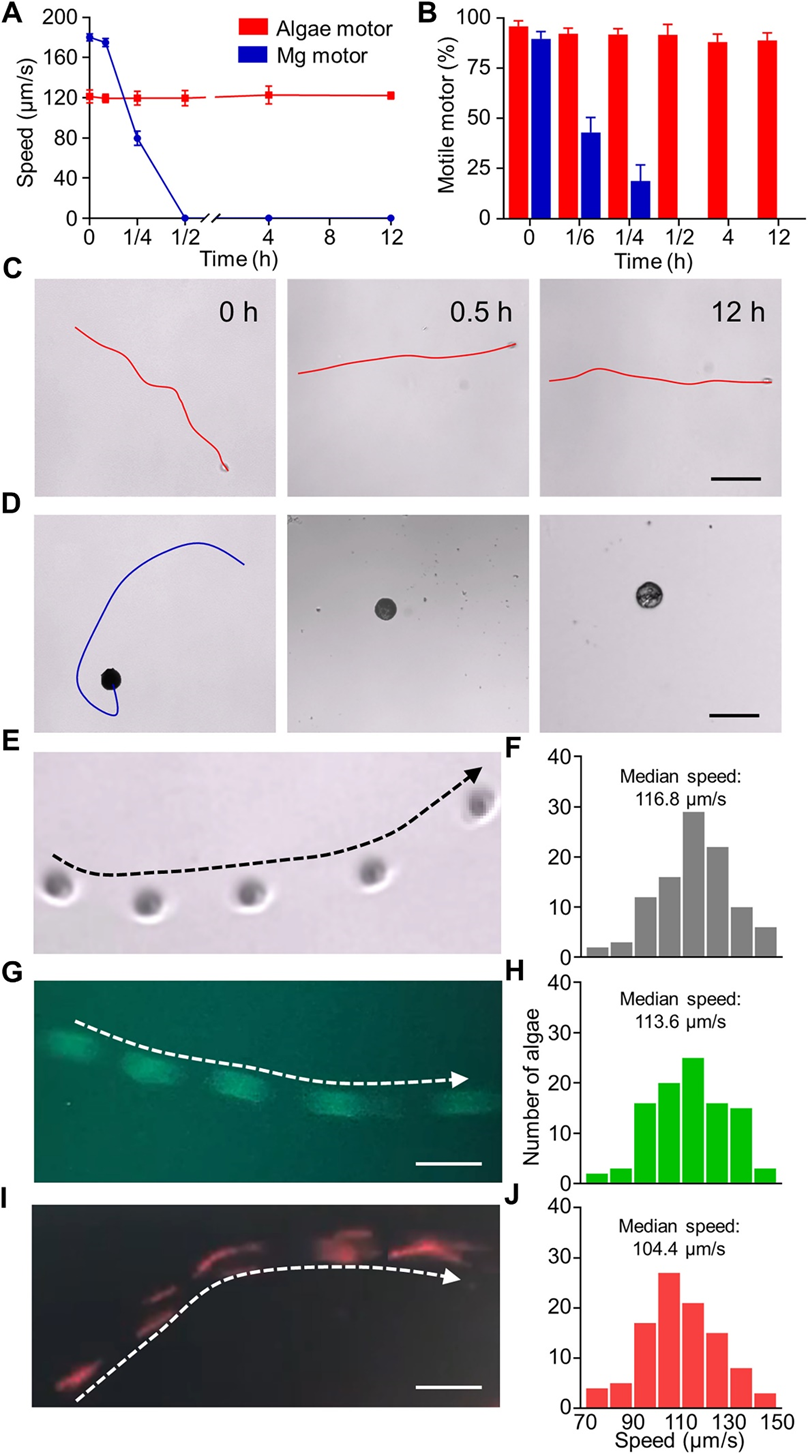
圖 室溫下SIF中藻馬達和鎂馬達的運動性。
將藍衣藻納米機器人配制成膠囊:
為了有效地使藍衣藻納米機器人輸送到胃腸道,有必要克服胃的惡劣酸性環境,這種環境可以在藻類到達小腸之前降解它們。為了解決這個問題,作者團隊改進了一種商業膠囊,將活的藻類封裝在內部水性培養基中,以便安全地通過胃。膠囊的外表面涂有pH響應聚合物,通常用于保護口服藥物免受惡劣的胃酸條件的影響。
進一步研究藻類在修飾膠囊中的封裝及其在體外釋放。將藻類懸浮在三醋酸磷酸酯(TAP)培養基中,并加載到膠囊中。在熒光顯微鏡下,觀察到兩個涂層的強信號以及藻類的自發熒光,證實了藻類馬達成功封裝到制造的膠囊平臺中。在模擬胃液(SGF)中,證明沒有藻類從膠囊中釋放出來,而藻類馬達可以在SIF中隨著時間的推移而釋放。在SIF中,大部分藻類在45分鐘后被釋放,釋放的藻類總數達到9.15×105。這些數據表明,藻類馬達可以被有效地封裝,然后從修飾的膠囊中釋放出來,對其運動能力的影響可以忽略不計。
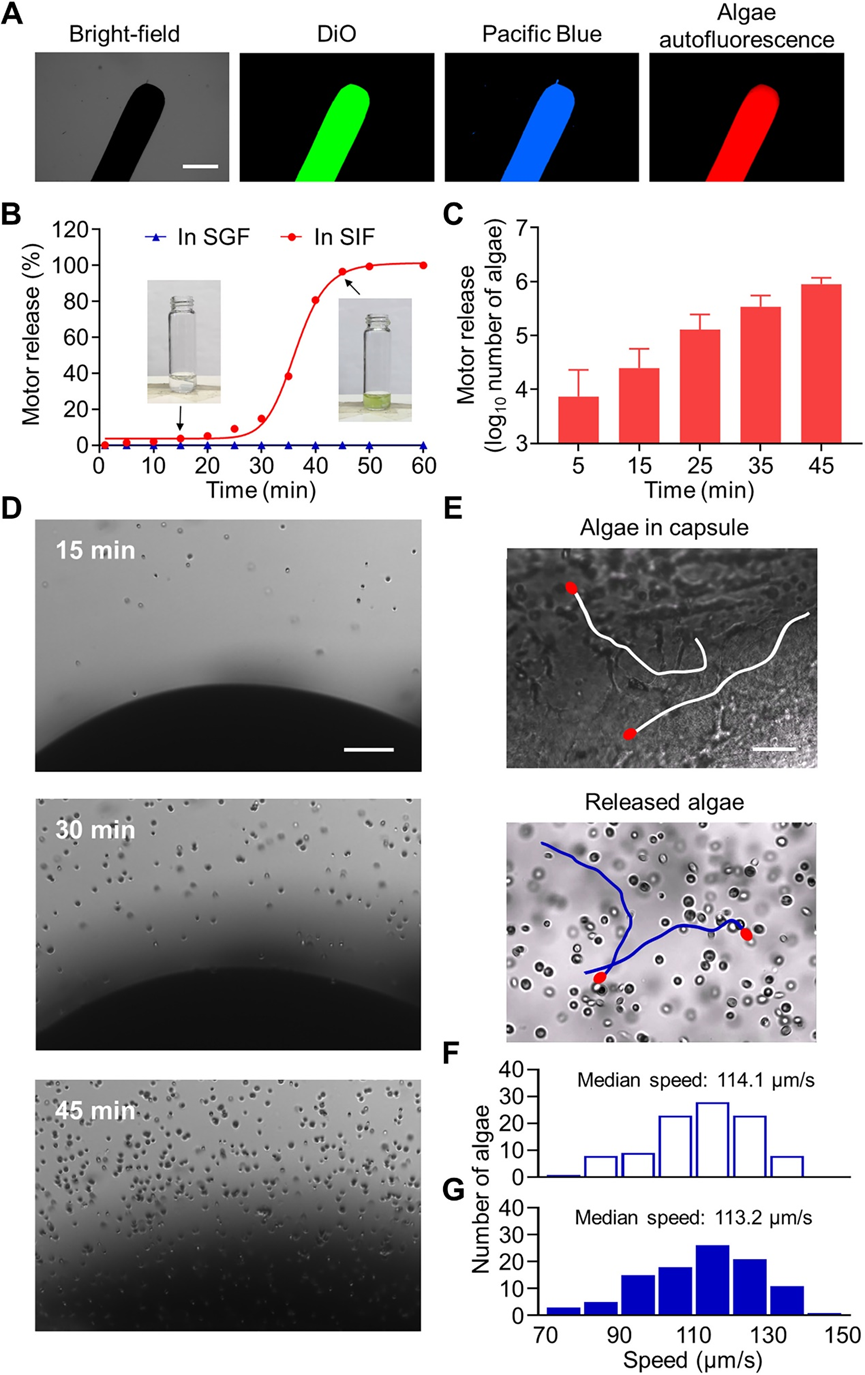
圖 像在體外膠囊中加載和釋放藍衣藻納米機器人
藍藻納米機器人的胃腸道運動與分布:
接下來,評估體外條件下藻類馬達在胃腸道內的遞送能力。首先,模仿腸道的生理條件,在SIF中37℃下評估藻類馬達和Mg馬達的運動行為。藍衣藻的活性在37℃下會受到影響,運動速度在自推進的15分鐘內下降到83μm/s,12小時后進一步下降。在實驗終點,大約70%的藻類保持運動,表明即使在不利的條件下,它們也可以長時間存活。
在體外試驗之后,評估以膠囊形式口服時藻類馬達的體內生物分布和保留。將藻類馬達和Mg馬達嵌入保護膠囊并強飼,在小鼠體內對其胃腸道進行成像。相比Mg馬達狹窄分布的熒光信號,藻類馬達的信號在腸道中分布更加的廣泛。觀察到的生物分布差異表明,藻類具有持久的運動特性,可以有效地在胃腸道內局部傳遞藥物有效載荷。
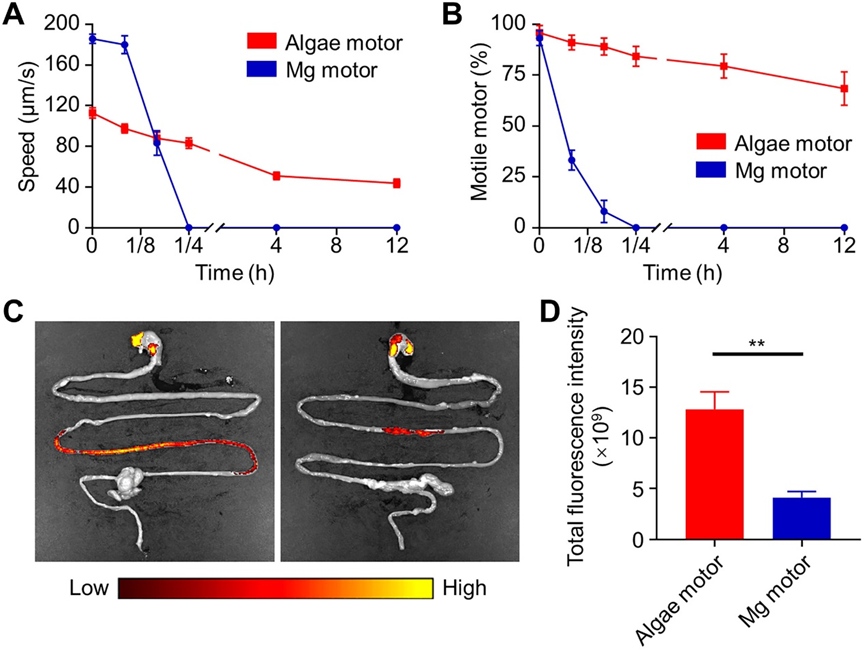
圖 藻類馬達和Mg馬達在胃腸道中的分布比較
藍衣藻納米機器人膠囊的體內藥物遞送:
為了更好地了解藻類運動在小腸內改善生物分布和滯留的機制,將不同狀態的藍衣藻用于載藥,包括僅含培養基的膠囊,沒有膠囊的游離藻類和含靜態藻類的膠囊。在口服給藥后5小時,與包封靜態藻類的膠囊相比,輸送藻類馬達的膠囊可以更廣泛地促進藥物分布在腸道中。這一結果強調了自推進的重要性,這可能有助于增加藻類與腸壁的相互作用,從而導致增強的保留。此外,在給予游離藻類后,腸道中幾乎沒有觀察到任何信號,這表明使用膠囊來防止刺激性胃酸的必要性。
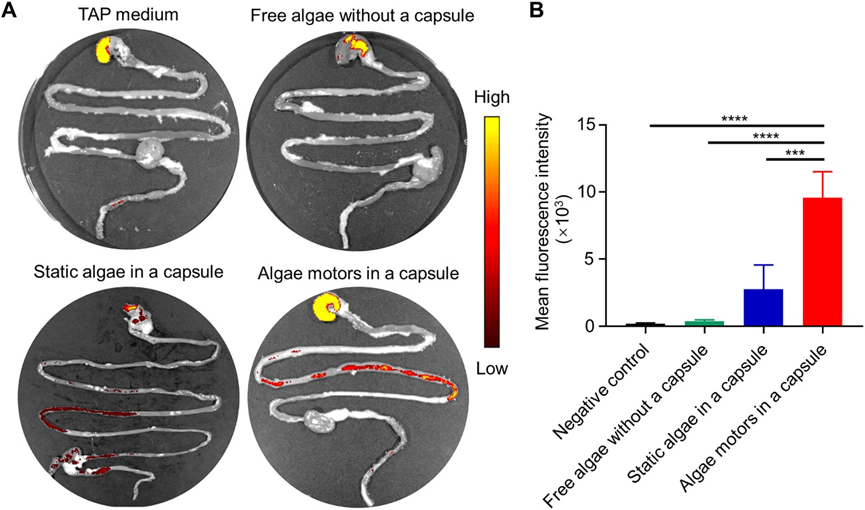
圖 胃腸道輸送不同藻類馬達
作者團隊接下來探討了使用藻類馬達在小鼠胃腸道遞送藥物的可行性。Dox是一種常用的一線化療藥物,被選為模型藥物有效載荷。通過點擊化學將PLGA-NP(Dox)與藍衣藻相交聯,在加載到藻類馬達上后,NP(Dox)有效載荷并保持其細胞毒性活性,藻類-NP(Dox)可以在體外抑制B16F10黑色素瘤細胞系的生長。
然后將藻類-NP(Dox)和NP(Dox)都裝入保護膠囊中,施用后提取腸道以量化Dox濃度。與用NP(Dox)給藥的小鼠的組織勻漿相比,接受藻類-NP(Dox)的小鼠在測試的所有時間點都表現出顯著更高的藥物水平。這些數據進一步支持了使用藻類馬達介導的長期自推進,可以有效增強小腸疾病治療中藥物的有效遞送和延長滯留。未來的研究將側重于評估藻類馬達在藥物遞送中的潛力,以治療合適動物模型中的疾病,例如炎癥性腸病和細菌性胃腸炎。
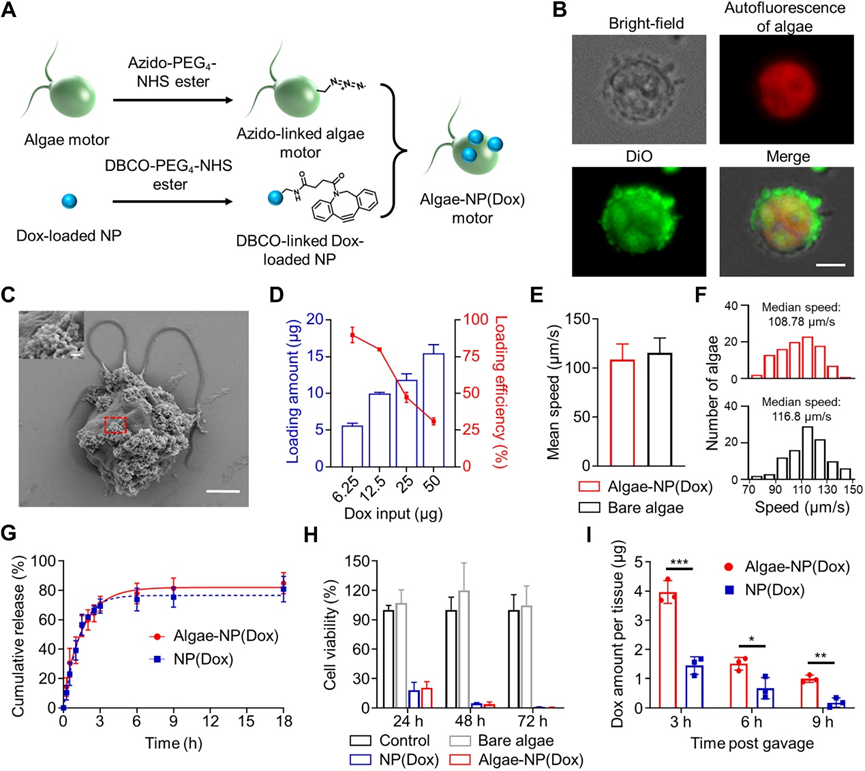
圖 藥物負載的藻類馬達表征
藍衣藻納米機器人膠囊的體內毒性評價:
對于微生物載體的應用,其體內安全性的評價至關重要。在給藥后24小時后,接受藍衣藻納米機器人膠囊治療的小鼠中所有血清生化標志物和血細胞的數量保持在正常水平。在長期安全性研究中,第0、2、4、6天施用膠囊的小鼠也有相似的結果,從而代謝生物和血細胞指標的微小變化中可以發現藍藻膠囊的毒性可以忽略不計。施藥小鼠胃腸道組織切片的組織學分析顯示,腸道結構完整性得以保留,并且沒有免疫細胞浸潤到粘膜或粘膜下層。來自其他主要器官的H&E染色切片上也沒有可觀察到明顯的炎癥或病理變化。總體而言,這些結果表明,藍衣藻納米機器人膠囊平臺可以安全地用于口服藥物給藥。

圖 口服給藥后藻類馬達的體內安全性分析。
小結:
目前用于解決關鍵醫療保健問題的基于微生物的微馬達的開發仍處于起步階段。盡管各種體外研究已經說明了基于細菌的藥物遞送系統有著顯著的開發潛力,但在考慮致病性或免疫原性等因素時,其體內使用仍然存在重大風險。相比細菌與病毒等備選開發載體,微藻是致病性使是有限的,可惜的是微藻的醫療價值開發仍待更多人投身。
膠囊制劑中藻類馬達的主要特性在于其持久的自推進,可用于胃腸道疾病治療或診斷等領域的微機器人生物醫學應用。可以進一步賦予藻類馬達更多的功能,以提高其對胃腸道輸送應用的實用性。如,加入成像劑可以直接可視化藻類在腸道內工作時的運動。又或通過將磁性微粒共軛到藻類表面,通過外加磁場來精確地引導藻類馬達到達目標部位。雖然目前的工作重點仍然是證明藻類馬達膠囊在增強腸道藥物遞送方面的潛力,但未來的工作將需要確認該平臺在臨床相關疾病模型中的治療優勢,例如細菌胃腸道感染,腸易激性疾病或結腸癌等等。膠囊的性質也可以調整為更精確地靶向胃腸道的特定區域。總體而言,功能化的藻類馬達,加載在保護膠囊內,代表了一種有吸引力的生物混合馬達系統,可以應用于廣泛的生物醫學應用。
參考文獻:
Fangyu Zhang, Zhengxing Li, Yaou Duan, et al. Gastrointestinal tract drug delivery using algae motors embedded in a degradable capsule. Sci Robot. 2022 Sep 28;7(70):eabo4160.
https://www.science.org/doi/10.1126/scirobotics.abo4160











