
第一作者:Hongmin Chen
通訊作者:Hongmin Chen、Gang Liu、Jin Xie、Xiaoyuan Chen
通訊單位:廈門大學(xué)、佐治亞大學(xué)、美國國立衛(wèi)生研究院
研究亮點(diǎn):
1. 利用溶劑熱法量化制備具有紅光發(fā)射的內(nèi)嵌釓碳點(diǎn),弛豫率增強(qiáng)4倍以上。
2. 單線態(tài)氧量子產(chǎn)率超過0.5。
3. 活體上實(shí)現(xiàn)熒光成像、磁共振成像以及光動力治療(PDT)。
傳統(tǒng)的光敏劑多數(shù)是疏水小分子,其缺點(diǎn)在于水分散性差,光穩(wěn)定性低和在腫瘤區(qū)域的富集不夠。雖然目前大部分研究將光敏劑和成像劑一起負(fù)載到納米載體上,但這些成像劑或光敏劑易脫落,并且很多納米載體具有潛在的毒性且難以快速有效地清除。此外,納米載體或成像試劑被發(fā)現(xiàn)也會干擾光動力治療過程,降低活性氧物種(ROS)的產(chǎn)量。
有鑒于此,在前期研究基礎(chǔ)上,廈門大學(xué)陳洪敏課題組近日完成量化制備“釓穩(wěn)定”碳點(diǎn),用于腫瘤雙模態(tài)成像和成像指導(dǎo)的光動力治療。
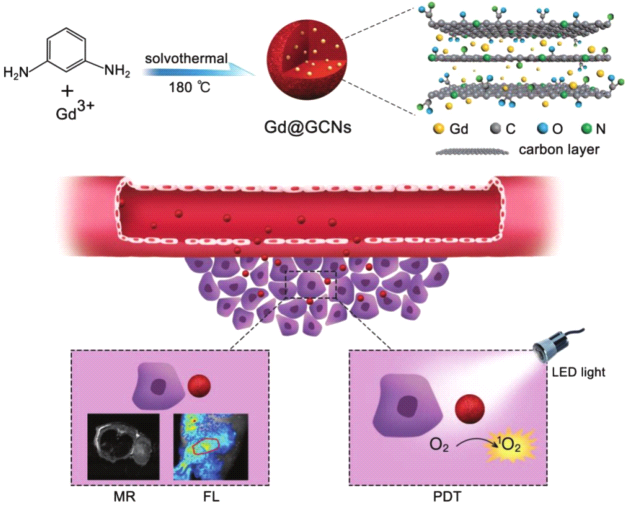
圖1 “釓穩(wěn)定”碳點(diǎn)用于雙模態(tài)成像指導(dǎo)的PDT示意圖
此前,針對傳統(tǒng)的釓配合物磁共振造影劑存在的穩(wěn)定性差和成像效能差的基本科學(xué)問題,陳洪敏博士借鑒釓富勒烯主-客結(jié)構(gòu)能夠增強(qiáng)釓穩(wěn)定性和提高磁性能的原理,通過直接煅燒釓噴普銨(Gd-DTPA)和利用介孔二氧化硅孔道作為模板,成功制備出“釓穩(wěn)定”的內(nèi)嵌釓碳點(diǎn)。
以上“釓穩(wěn)定”的內(nèi)嵌釓碳點(diǎn)實(shí)現(xiàn)了高釓穩(wěn)定性、有效增強(qiáng)弛豫率(比Gd-DTPA提高了一倍以上),靜脈注射能夠在腫瘤區(qū)域有效富集實(shí)現(xiàn)活體腫瘤成像,能夠有效通過腎臟代謝清除。相關(guān)成果發(fā)表在Advanced Materials (2014, 26, 6761), Advanced Functional Materials (2016, 26, 3973.封面文章),Theranostics(2013, 3, 650)。
在以上研究的基礎(chǔ)上,研究者進(jìn)一步通過溶劑熱法量化制備了具有紅光發(fā)射的內(nèi)嵌釓碳點(diǎn)。
與傳統(tǒng)的碳點(diǎn)相比,該碳點(diǎn)展現(xiàn)出高結(jié)晶度,強(qiáng)烈的紅色熒光,高效的釓摻雜率和表面一定的還原特性;與常用的Gd-DTPA造影劑相比,由于碳層的包裹,釓碳點(diǎn)表現(xiàn)出極高的縱向弛豫效率(r1=16 mM-1 S-1, 7T);更重要的是該釓碳點(diǎn)在LED燈輻射下能夠有效的產(chǎn)生單線態(tài)氧(量子產(chǎn)率達(dá)到0.51)。
此外,該碳點(diǎn)具有較小的尺寸(約5納米),可以通過EPR效應(yīng)積累在腫瘤部位,并且,釓碳點(diǎn)能夠通過腎臟代謝掉,因而具有較低的毒性。
活體實(shí)驗(yàn)證明此釓碳點(diǎn)成為集熒光成像、磁共振成像和光動力治療于一體的納米診療探針。這一研究工作在深入探索“釓穩(wěn)定”納米探針與金屬摻雜增強(qiáng)光化學(xué)作用的機(jī)制以及設(shè)計(jì)具有高ROS產(chǎn)率和優(yōu)異穩(wěn)定性診療一體化納米探針中提供了新的研究思路。
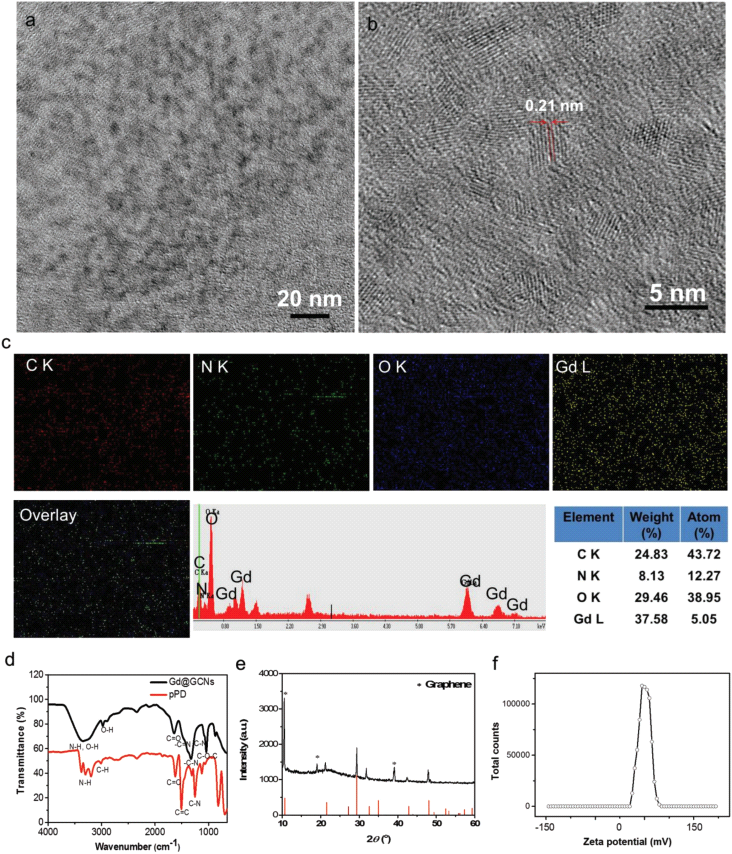
圖2 “釓穩(wěn)定”碳點(diǎn)的材料表征
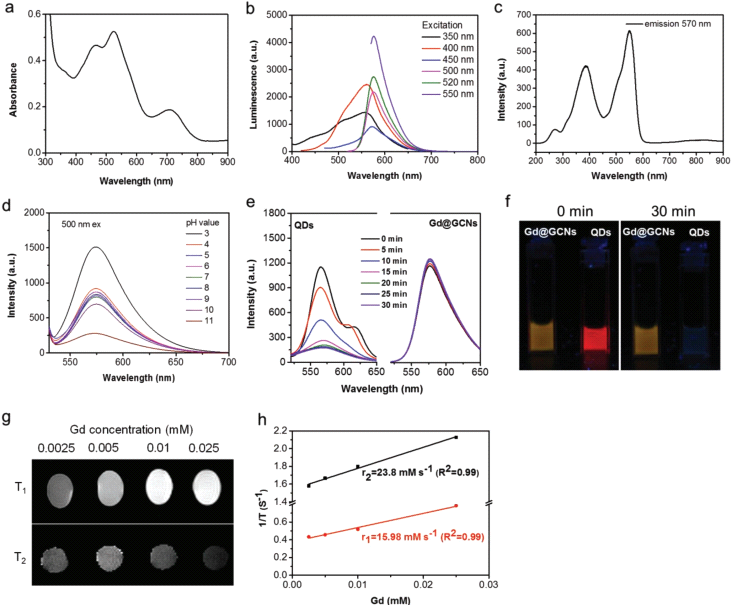
圖3 “釓穩(wěn)定”碳點(diǎn)的光學(xué)性質(zhì)和體外磁共振對比效果
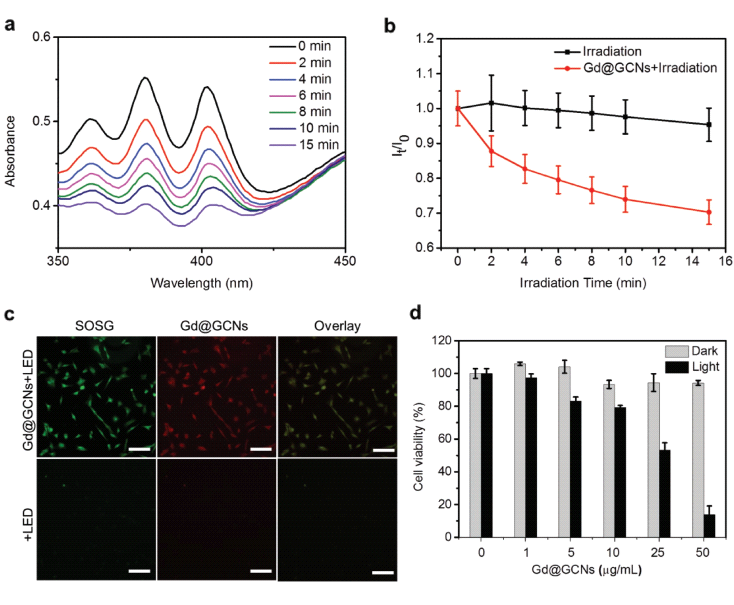
圖4 體外的成像和PDT效果

圖5 活體成像效果
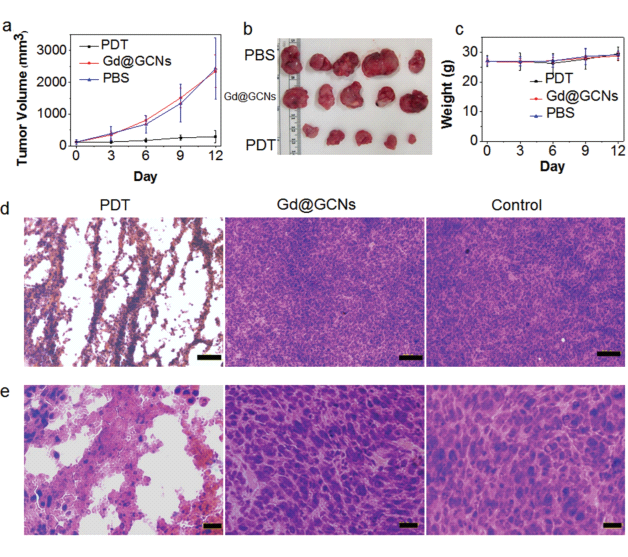
圖6 活體治療效果
總之,該研究量化制備了具有紅光發(fā)射的內(nèi)嵌釓碳點(diǎn),是集合熒光成像、磁共振成像和PDT功能于一體的腫瘤納米診療探針,具有突出的臨床轉(zhuǎn)化應(yīng)用的價(jià)值。
參考文獻(xiàn):
Chen H, Qiu Y, Ding D, et al. Gadolinium‐Encapsulated Graphene Carbon Nanotheranostics for Imaging‐Guided Photodynamic Therapy[J]. Advanced Materials, 2018: 1802748.
DOI: 10.1002/adma.201802748
https://onlinelibrary.wiley.com/doi/10.1002/adma.201802748
課題組簡介:
陳洪敏博士2017年入職廈門大學(xué)分子影像暨轉(zhuǎn)化醫(yī)學(xué)研究中心,主要研究方向?yàn)榉肿佑跋窈图{米醫(yī)學(xué)領(lǐng)域,多年來主要圍繞“分子探針多模態(tài)影像與協(xié)同治療的高效融合”關(guān)鍵科學(xué)問題,致力于新型多功能分子影像探針在癌癥診斷與治療的研究,取得了一系列創(chuàng)新性的、并具有較高臨床應(yīng)用前景的重要研究成果:1) 高效融合放射治療和光動力治療,構(gòu)建了無機(jī)閃爍體增敏體系,實(shí)現(xiàn)了低輻射劑量有效抑制深層原位腫瘤;2) 研究制備了“釓穩(wěn)定”多功能磁共振成像探針;3) 建立了藥物高效封裝、緩釋示蹤和快速藥物敏感性測試的方法。包括2篇封面文章,2篇ESI(熱點(diǎn))高被引論文。
其中,2013年以來,相關(guān)研究成果相繼刊發(fā)在Adv. Mater.、Nano Lett.、Adv. Funct. Mater.、Mater. Horiz.、Theranostics等期刊上。受邀為Nat. Rev. Mater. (IF=51.941)、Mater. Sci. Eng. R: Rep. (IF=24.4) 撰寫綜述。成果受邀參編美國NIH癌癥研究所的“Cancer Nanotechnology Plan 2015”。現(xiàn)擔(dān)任Chem. Soc. Rev., J. Am. Chem. Sci., Adv. Mater., Small, Nanoscale, Theranostics等國際學(xué)術(shù)期刊的審稿人。擔(dān)任學(xué)術(shù)期刊 Current Medicinal Chemistry (IF 3.469)的 Guest Editor(2017)。
課題組主頁:











