需要靈敏的技術(shù)來表征大腦的回路,并識別和治療任何潛在的病理。與報告基因相結(jié)合的光學(xué)成像已經(jīng)成為一種杰出的技術(shù),能夠針對特定的神經(jīng)細胞群體。然而,使用光學(xué)成像探測腦回路存在相關(guān)的挑戰(zhàn),因為它需要用光學(xué)活性基因轉(zhuǎn)導(dǎo)神經(jīng)細胞,以及植入一種裝置以將光遞送穿過寬區(qū)域以激發(fā)經(jīng)轉(zhuǎn)導(dǎo)的神經(jīng)細胞中的發(fā)色團。需要對所有目標(biāo)組織進行適當(dāng)照明,以確保精確測量大腦活動或操縱大腦回路。此外,這些測量值很難通過建模或其他方式獲得,但對這些表征和操作的成功有很大影響。
近日,麻省理工學(xué)院Alan Jasanoff等人開發(fā)出了光敏脂質(zhì)體造影劑,通過磁共振成像(MRI)對腦組織中光照模式的空間分布進行全面表征。
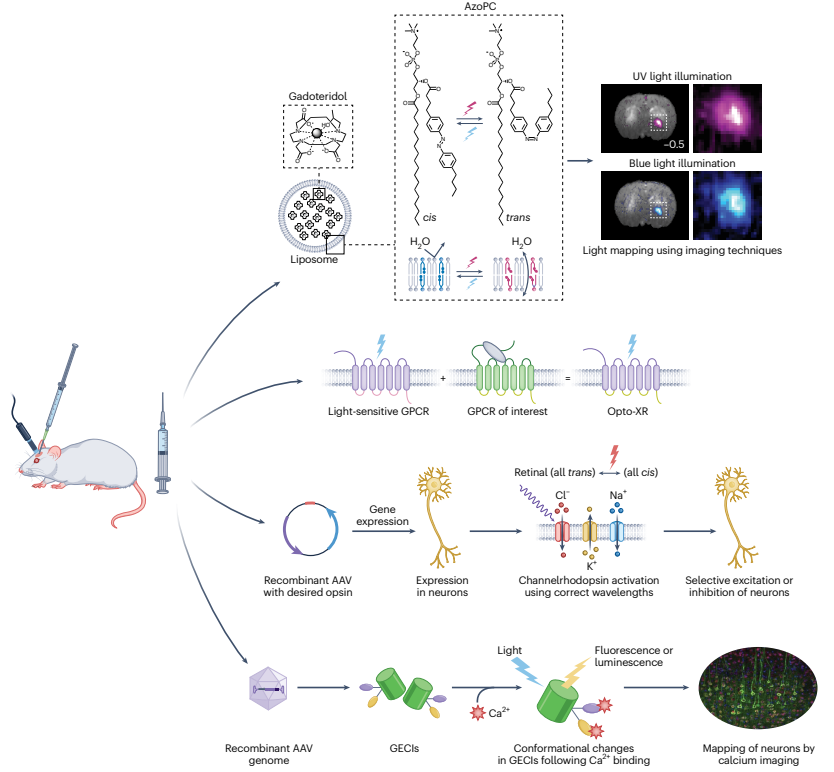
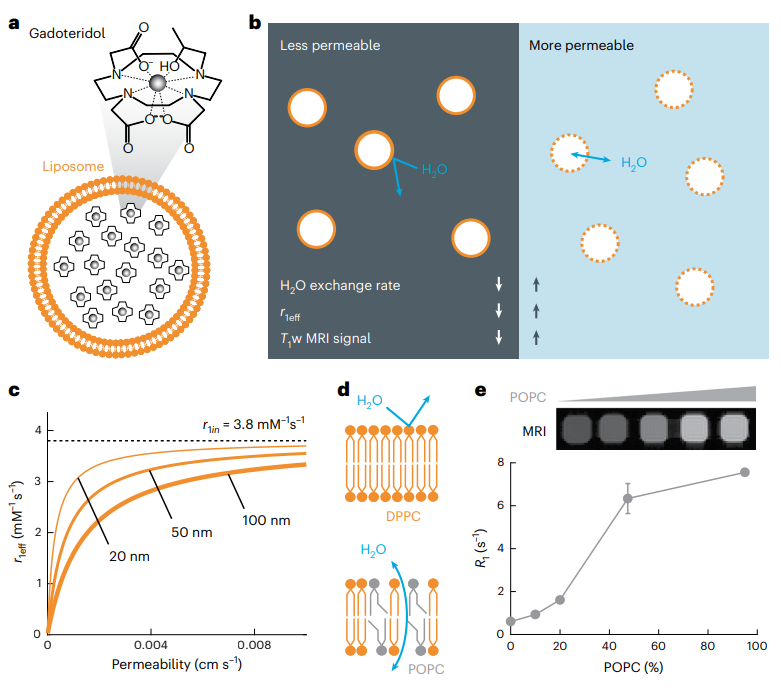
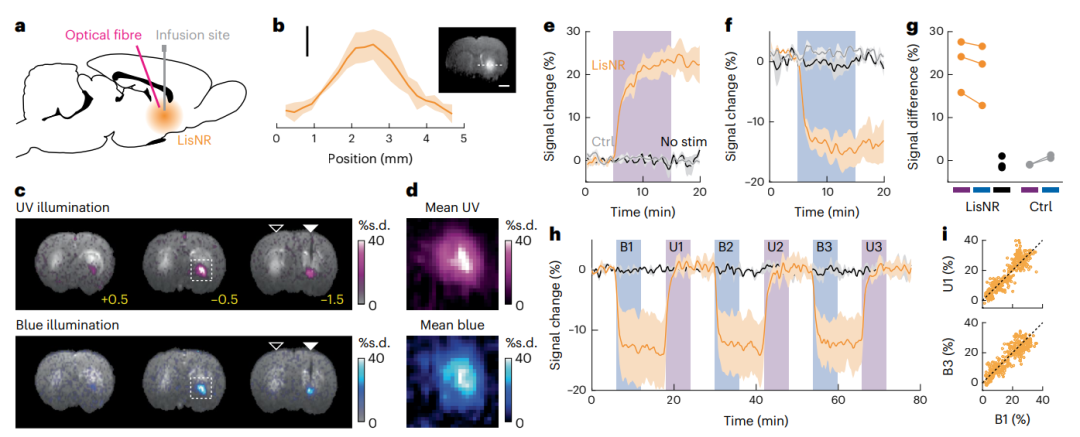
臨床前廣泛使用光學(xué)成像。通常使用在膜電位或鈣離子(Ca2+)濃度改變后改變其反應(yīng)的熒光染料對神經(jīng)元活動進行成像。細胞活性的光學(xué)檢測也可以通過報告基因?qū)崿F(xiàn),例如編碼與Ca2+傳感或電壓傳感結(jié)構(gòu)域融合的熒光蛋白的基因,其被轉(zhuǎn)導(dǎo)到特定的細胞類型中。對于光遺傳學(xué)研究,光感受器基因也可整合到細胞群中,以使光活化或沉默轉(zhuǎn)染細胞中的特定功能。光遺傳學(xué)中最常見的發(fā)色團是在離子通道、基于四吡咯的光感受器和黃素結(jié)合系統(tǒng)中發(fā)現(xiàn)的視網(wǎng)膜視蛋白。工程化的G蛋白偶聯(lián)受體,如谷氨酸受體,也可以通過光來打開和關(guān)閉。研究人員描述了包裹gadoteridol(一種基于順磁性釓的MRI造影劑)的脂質(zhì)體納米顆粒的設(shè)計和性能,其透水性可通過共價共軛于納米粒子脂質(zhì)中磷脂酰膽堿部分(AzoPC)的偶氮苯的光異構(gòu)化作用進行可逆調(diào)節(jié)。含有緊密堆積的飽和脂質(zhì)的脂質(zhì)體納米顆粒傾向于阻止水交換,而加入更多的流動脂質(zhì)有助于納米顆粒外部和內(nèi)腔之間的水交換。光會導(dǎo)致偶氮苯的結(jié)構(gòu)變化,從而增強gadoteridol對大量水的接觸,從而開啟納米顆粒探針的MRI對比度。研究人員通過改變脂質(zhì)體雙層的組成并通過調(diào)節(jié)流化脂質(zhì)1-棕櫚酰基-2-油酰基-sn-甘油-3-磷酸膽堿和非流化脂質(zhì)1,2-二棕櫚酰基-sn-葡萄糖-3-磷酸膽堿的量,優(yōu)化了高濃度(220mM)gadoteridol脂質(zhì)體的可切換縱向弛豫時間(T1)。紫外(UV)光觸發(fā)苯環(huán)從順式構(gòu)象轉(zhuǎn)換為反式構(gòu)象,這導(dǎo)致脂質(zhì)體優(yōu)化配方的MRI對比度存在強烈差異。通過暴露于藍光,MRI對比度可以快速反轉(zhuǎn),這促進了苯環(huán)的順式構(gòu)象。通過比較交替模式下藍光和紫外光照射的縱向相對性(R1),作者表明對比度隨時間穩(wěn)定。作者隨后表明,經(jīng)過優(yōu)化的AzoPC脂質(zhì)體納米粒子可以在體內(nèi)繪制光圖。納米粒通過緩慢的局部輸注進入大鼠腦中給藥。注射納米顆粒后觀察到的磁共振信號變化表明通過對流在腦中有效擴散。藍色和UV光周期上的磁弛豫性變化提供了納米粒子探針對包含探針的個體體素的光的敏感性的度量。探針對紫外線和藍光以及兩種波長相對于初始基線的響應(yīng)產(chǎn)生顯著的MRI信號均值差異。在活體動物中,光響應(yīng)率的分布在重復(fù)光照周期內(nèi)也是一致的。此外,作者表明,通過將實驗數(shù)據(jù)擬合到一個由光束擴展函數(shù)與光子擴散項線性組合而成的模型,可以生成分辨率約為200微米的光分布定量圖。綜上所述,該研究的結(jié)果表明了基于偶氮PC的脂質(zhì)體納米顆粒在體內(nèi)繪制深部組織中光子分布圖的魯棒性。正如研究人員所建議的,通過將共軛偶氮苯發(fā)色團改為替代光開關(guān),可以將偶氮PC光開關(guān)的作用光譜外推到更長的波長,從而為該方法適應(yīng)其他應(yīng)用提供了空間,并有可能改善吸收截面。脂質(zhì)體還可以包括替代的R1造影劑和在其外部的靶向特定位點的靶向基團。然而,納米顆粒在深層組織中的均勻分布可能受到限制,因為納米顆粒清除率的差異可能取決于免疫微環(huán)境。此外,與許多光學(xué)技術(shù)一樣,該方法需要手術(shù)注入納米顆粒,并且手術(shù)過程可能會導(dǎo)致光傳輸?shù)牟町悺?/span>廣泛的光學(xué)基因可用于表征和操縱神經(jīng)元活動,其波長范圍從紅外到紫外。光遺傳學(xué)最近也在早期患者試驗中進行了測試;在第一個使用案例中,它幫助失明近40年的患者恢復(fù)了視覺功能。需要更多的研究來開發(fā)更好的病毒載體和光學(xué)裝置,并進一步表征其安全性。由于光學(xué)成像的廣泛應(yīng)用,該脂質(zhì)體納米顆粒提供的基于微創(chuàng)MRI的光映射方法可能有助于計劃實驗程序,并在使用光學(xué)成像表征或操縱腦回路時解釋實驗結(jié)果。Simon, J., Schwalm, M., Morstein, J. et al. Mapping light distribution in tissue by using MRI-detectable photosensitive liposomes. Nat. Biomed. Eng (2022). https://doi.org/10.1038/s41551-022-00982-3