
大型設(shè)備的小型化是工程學(xué)永恒的課題之一,雖然直接簡單地減小其部件的尺寸一定程度上可以實(shí)現(xiàn)機(jī)器的增量小型化,但徹底的小型化往往需要重新評(píng)估控制機(jī)器運(yùn)行的物理原理。在傳統(tǒng)的電動(dòng)機(jī)中,通過電磁感應(yīng)將電場轉(zhuǎn)換為旋轉(zhuǎn)運(yùn)動(dòng),但使用靜電驅(qū)動(dòng)在亞毫米范圍內(nèi)產(chǎn)生旋轉(zhuǎn)運(yùn)動(dòng)已經(jīng)是最好的。在納米尺度上,生物分子馬達(dá)使用化學(xué)反應(yīng)來偏置隨機(jī)位移的方向,以高精度和高效率運(yùn)行。盡管偏置擴(kuò)散機(jī)制已經(jīng)在純合成分子系統(tǒng)中實(shí)現(xiàn),但沒有一個(gè)與生物馬達(dá)的精度和效率相匹配,這最終可以歸因于后者具有通過進(jìn)化優(yōu)化的結(jié)構(gòu)。
幾個(gè)世紀(jì)以來,利用流體流過手性物體用為機(jī)器中的旋轉(zhuǎn)運(yùn)動(dòng)提供動(dòng)力已經(jīng)成為范式。相比之下,納米級(jí)生物或化學(xué)系統(tǒng)中的旋轉(zhuǎn)運(yùn)動(dòng)多是通過循環(huán)化學(xué)反應(yīng)引導(dǎo)布朗運(yùn)動(dòng)產(chǎn)生的。近日,美國伊利諾伊大學(xué)厄巴納-香檳分校的Aleksei Aksimentiev教授率領(lǐng)其團(tuán)隊(duì)展示了當(dāng)沿手性生物分子——DNA雙鏈體施加電場時(shí),其可以每分鐘數(shù)十億轉(zhuǎn)的速度單向旋轉(zhuǎn)。這種旋轉(zhuǎn)的方向由雙鏈體的手性決定,由電滲透流的拖曳力驅(qū)動(dòng)的,實(shí)現(xiàn)了宏觀渦輪機(jī)在納米尺度上的工作原理。由此產(chǎn)生的扭矩足以為球體和棒狀納米粒子的旋轉(zhuǎn)提供動(dòng)力,為構(gòu)建由電場驅(qū)動(dòng)的納米級(jí)系統(tǒng)提供了工程原理。
電場中的DNA雙鏈體旋轉(zhuǎn):
為了研究DNA雙鏈單體是否會(huì)在外部電場中單向旋轉(zhuǎn),作者團(tuán)隊(duì)構(gòu)建了一個(gè)浸沒在1M KCl電解質(zhì)溶液中的16堿基對(bp)DNA雙鏈體的全原子模型,模擬雙鏈體沿其螺旋軸施加電場時(shí)的行為。雙鏈體的磷原子被限制在圓柱體的表面,使得DNA雙鏈體可以自由地繞其軸旋轉(zhuǎn)。100 mV/nm電場沿其螺旋軸定向,觀察到DNA雙鏈體繞其軸旋轉(zhuǎn),旋轉(zhuǎn)矢量指向施加的場。在使用替代水模型進(jìn)行的模擬中觀察到類似的單向旋轉(zhuǎn)。反轉(zhuǎn)外加磁場的方向反轉(zhuǎn)了DNA旋轉(zhuǎn)的方向。
在對照計(jì)算實(shí)驗(yàn)中,使用DNA鏡像立體異構(gòu)體形的左手雙鏈單體l-DNA重復(fù)模擬,發(fā)現(xiàn)左手雙鏈體以與常規(guī)DNA雙鏈體相同的速度旋轉(zhuǎn),但方向相反。最后,使用A型RNA雙鏈體重復(fù)模擬,發(fā)現(xiàn)RNA與常規(guī)B-DNA雙鏈體旋轉(zhuǎn)方向相同,盡管旋轉(zhuǎn)速率降低。對不同的電場值進(jìn)行重復(fù)實(shí)驗(yàn),得出平均旋轉(zhuǎn)速率對電場強(qiáng)度的依賴性。在100 mV/nm電場下,核酸雙鏈體以每分鐘約10億轉(zhuǎn)的速度旋轉(zhuǎn),比已知最快的分子轉(zhuǎn)子的旋轉(zhuǎn)速度高出幾個(gè)數(shù)量級(jí)。
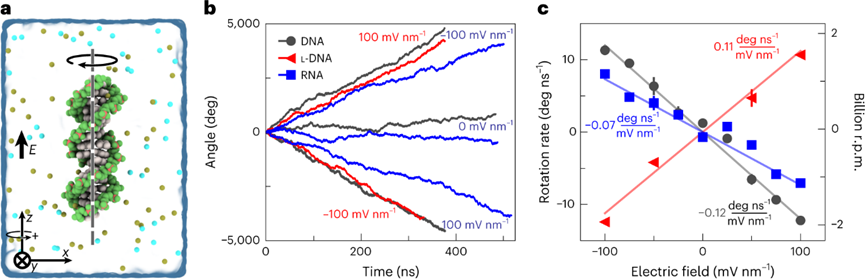
圖1 DNA和RNA分子在外部電場中的單向旋轉(zhuǎn)
扭矩產(chǎn)生機(jī)制:
為了確定外加電場賦予核酸結(jié)構(gòu)的扭矩與產(chǎn)生機(jī)制,進(jìn)一步構(gòu)建了全原子系統(tǒng)模型。在外部電場的作用下,磷原子相對于其初始坐標(biāo)的平衡位移測量核酸雙鏈體所經(jīng)歷的有效力和扭矩。發(fā)現(xiàn)有效力與DNA分子標(biāo)定電荷的預(yù)期力相比大大降低,減少部分是由電滲透流的阻力引起的,而電滲透流又是由DNA表面附近的反離子運(yùn)動(dòng)產(chǎn)生的。
通過將約束每個(gè)磷原子的諧波力乘以從雙軸到該原子的距離來確定有效扭矩。對所有磷原子的扭矩值和模擬軌跡求平均值得出有效扭矩對外加電場的依賴性。在相同的電場下,發(fā)現(xiàn)DNA雙鏈體比RNA雙鏈體每bp經(jīng)歷更大的扭矩,這可能是由于分子的不同形狀,與B型DNA相比,A型RNA具有更大的半徑,更小的間和更容易接近溶劑的中心。
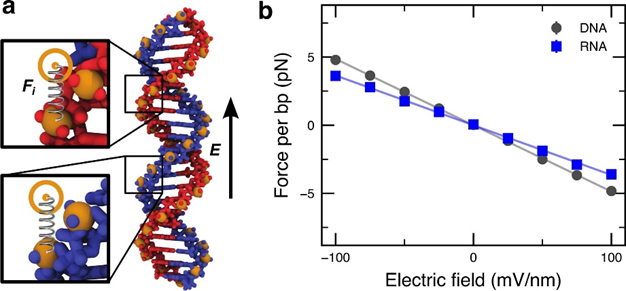
圖 電場對DNA和RNA分子的有效力
扭矩τ和角速度ω由ω = μτ相關(guān),其中μ是旋轉(zhuǎn)遷移率,即旋轉(zhuǎn)摩擦系數(shù)的倒數(shù)。發(fā)現(xiàn)DNA雙鏈體的旋轉(zhuǎn)遷移率略高于相同核苷酸組成的RNA雙鏈體。在相同的電場下,預(yù)計(jì)RNA雙鏈體的旋轉(zhuǎn)速度比DNA雙鏈體慢,因?yàn)榍罢弋a(chǎn)生的有效扭矩較低,旋轉(zhuǎn)遷移率較低。
為了研究扭矩的產(chǎn)生機(jī)制,進(jìn)一步確定了沿雙相軸線的切向流體速度以及流體的局部密度。由于DNA凹槽的存在,DNA雙鏈體附近和內(nèi)部水通量的切向分量雖然很小但具有統(tǒng)計(jì)學(xué)意義。水和離子分別攜帶的方位質(zhì)量通量的比值表明,水占驅(qū)動(dòng)DNA旋轉(zhuǎn)的方位動(dòng)量的近80%,如果可以避免動(dòng)量通過水耗散,DNA旋轉(zhuǎn)速率和有效扭矩都將增加五倍。
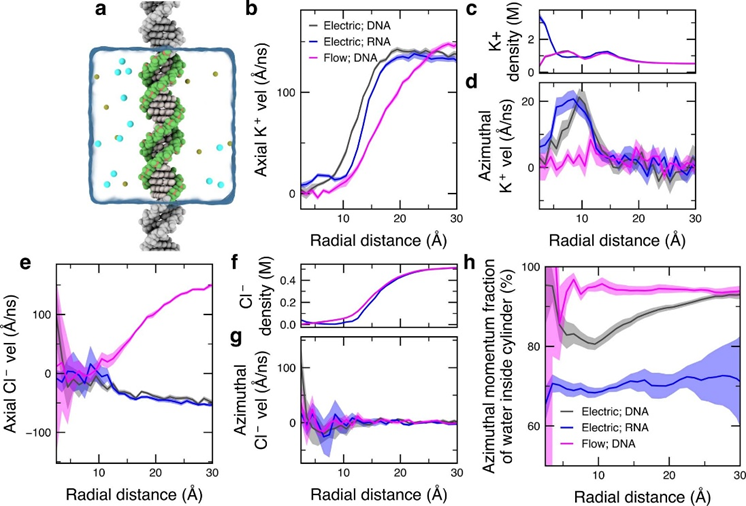
副圖 核酸分子周圍的離子流動(dòng)
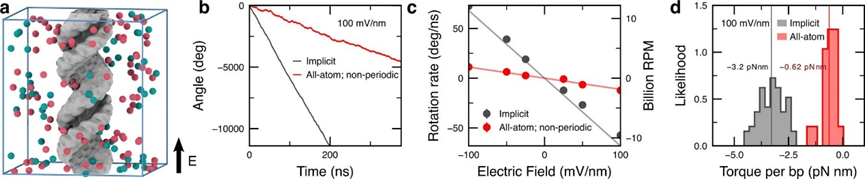
副圖 DNA旋轉(zhuǎn)的隱式溶劑模擬
如果雙鏈體在電場中的旋轉(zhuǎn)可以由溶劑的流動(dòng)引起,那么應(yīng)該可以在沒有外加電場的情況下在有流動(dòng)的系統(tǒng)中觀察到這種旋轉(zhuǎn)。為了驗(yàn)證這一假設(shè),沿著DNA軸對每個(gè)水分子施加一個(gè)小的力,產(chǎn)生周期性通過DNA系統(tǒng)的穩(wěn)態(tài)水流。旋轉(zhuǎn)速率與靜水壓力梯度呈線性關(guān)系,盡管壓力驅(qū)動(dòng)模擬中的溶劑凈通量比由電滲透效應(yīng)引起的溶劑凈通量大得多,但兩種情況下的旋轉(zhuǎn)速率幅度相似,這可能是DNA雙鏈體表面附近流動(dòng)曲線的相似變化。
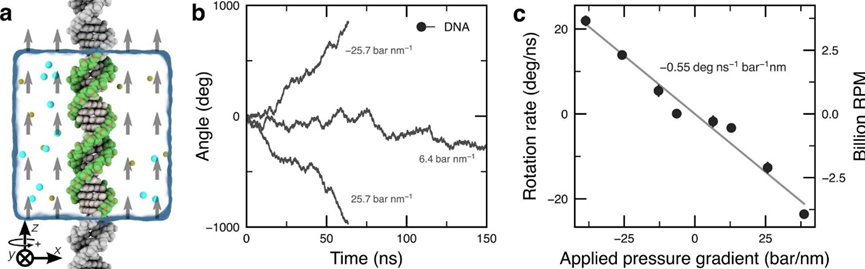
副圖 水流誘導(dǎo)的DNA分子旋轉(zhuǎn)
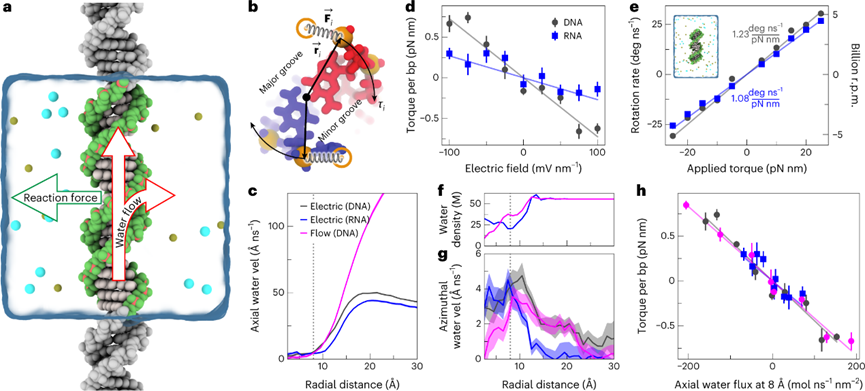
圖2 扭矩產(chǎn)生機(jī)制
納米孔旋轉(zhuǎn):
DNA產(chǎn)生扭矩的一種實(shí)用方法是將DNA分子穿過薄膜中的納米孔,通過在DNA雙鏈體一端橋接負(fù)載,在阻止其穿越納米孔的同時(shí)攜帶負(fù)載旋轉(zhuǎn)。在197 mV偏壓下,當(dāng)水以0.42nm/ns的平均速度通過納米孔時(shí),觀察到DNA以3.2度/納秒的平均速率旋轉(zhuǎn)。已知DNA雙鏈體的旋轉(zhuǎn)遷移率,估計(jì)在這些模擬中施加到DNA的有效扭矩為3.4pN/nm。忽略耗散,根據(jù)電流和電壓的乘積估計(jì)功率輸入約為200pW,能量轉(zhuǎn)換效率約為0.1%。
為了闡明負(fù)載阻止DNA易位和膜表面之間的摩擦效應(yīng),模擬DNA雙鏈體被外力壓向石墨烯層的自發(fā)擴(kuò)散。在不松開與石墨烯接觸的情況下,雙鏈體在150 ns的時(shí)間尺度上經(jīng)歷了明顯的平移和旋轉(zhuǎn)擴(kuò)散。進(jìn)一步構(gòu)建DNA T-bar模型,在394mV偏壓下,觀察到T-bar在沒有任何外部約束的情況下以0.58度/納秒的速率在碳納米孔中旋轉(zhuǎn)。注意,增加納米孔電滲流的大小既減少了拉動(dòng)DNA通過的有效力,又增加了有效扭矩,這使得光滑且?guī)ж?fù)電的納米孔成為使用DNA產(chǎn)生扭矩的理想選擇。
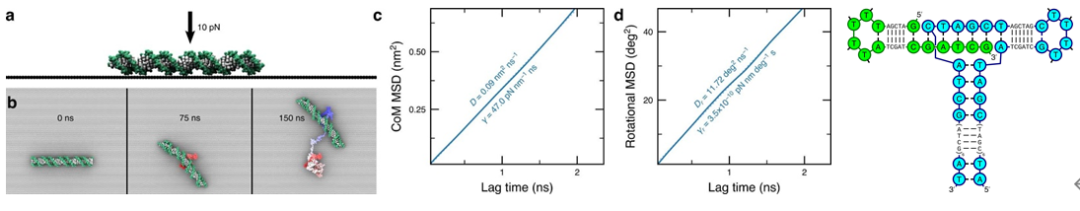
副圖 DNA壓在石墨烯表面的隨機(jī)位移與DNA T-bar模型
利用球形和棒狀顆粒流體動(dòng)力阻力的理論表達(dá)式,并假設(shè)雙相上的扭矩為1 pN/nm,確定了附著在DNA分子末端負(fù)載的穩(wěn)態(tài)旋轉(zhuǎn)速度。隨著顆粒半徑從10納米增加到40納米,球形粒子的平均旋轉(zhuǎn)速率從每分鐘數(shù)百萬轉(zhuǎn)降低到數(shù)千轉(zhuǎn)。桿狀負(fù)載的類似計(jì)算得出的旋轉(zhuǎn)速率隨著桿的長度而減小,并且對于200nm長的桿,旋轉(zhuǎn)速率在每分鐘數(shù)萬轉(zhuǎn)的范圍內(nèi)。
在典型的納米孔易位實(shí)驗(yàn)中,DNA分子會(huì)承受相當(dāng)大的扭矩。鑒于扭轉(zhuǎn)沿DNA分子的傳播速度比張力快得多,施加在納米孔內(nèi)DNA上的扭矩可能會(huì)誘導(dǎo)納米孔上游DNA結(jié)構(gòu)中結(jié)節(jié)的形成。結(jié)節(jié)通過納米孔將記錄為阻塞電流深度的瞬時(shí)三倍增加,這種電流阻塞特征類似于DNA結(jié)通過產(chǎn)生的電流阻塞特征。在實(shí)驗(yàn)上,可以通過附著剛性熒光標(biāo)記棒,不對稱等離子體納米顆粒或磁珠來檢測納米孔中DNA的旋轉(zhuǎn)。
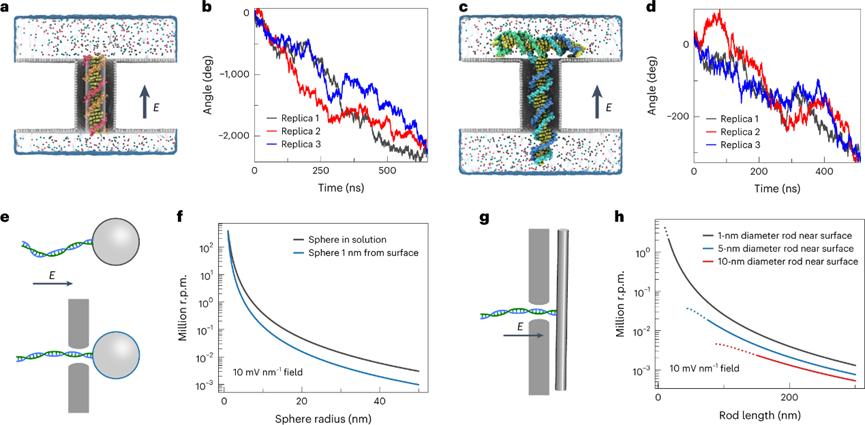
圖3 DNA驅(qū)動(dòng)的流體動(dòng)力載荷旋轉(zhuǎn)
小結(jié):
DNA不僅僅是遺傳密碼的載體,可編程自組裝的特性使得其已經(jīng)成為納米技術(shù)的強(qiáng)大工具,能夠制造各種系統(tǒng)。作者團(tuán)隊(duì)表明,當(dāng)溶劑通過時(shí),DNA雙鏈體的手性形狀足以產(chǎn)生旋轉(zhuǎn)運(yùn)動(dòng),DNA分子的螺旋形狀可以使其作為最簡單的電動(dòng)機(jī)發(fā)揮作用。這種流體運(yùn)動(dòng)可以通過沿DNA螺旋施加電場,利用電動(dòng)效應(yīng)方便地產(chǎn)生。該效應(yīng)產(chǎn)生的扭矩足夠大,可以驅(qū)動(dòng)10-200 nm級(jí)負(fù)載的旋轉(zhuǎn),其速率與生物分子馬達(dá)相當(dāng)或超過。然而,與分子馬達(dá)相比,DNA渦輪機(jī)中的扭矩產(chǎn)生機(jī)制與宏觀渦輪機(jī)非常相似,這表明其他依靠流體流動(dòng)進(jìn)行操作的宏觀機(jī)器可以縮小到納米級(jí)。
參考文獻(xiàn):
Christopher Maffeo, Lauren Quednau, James Wilson, et al. DNA double helix, a tiny electromotor. Nat Nanotechnol. 2022 Dec 23.
https://www.nature.com/articles/s41565-022-01285-z











