19世紀(jì)末���,紐約紀(jì)念醫(yī)院的外科醫(yī)生William Coley觀察到一名同時(shí)感染鏈球菌的肉瘤患者的自發(fā)性腫瘤緩解�����。受這一觀察的啟發(fā)���,Coley 制備了化膿性鏈球菌和粘質(zhì)沙雷氏菌的組合�����,并將其用作患者的抗癌療法。雖然這種方法從未在大型隨機(jī)試驗(yàn)中進(jìn)行過(guò)測(cè)試����,而且敗血癥并發(fā)癥有時(shí)會(huì)掩蓋抗腫瘤活性�����,但已經(jīng)積累了大量證據(jù)證明所謂的Coley毒素的作用,并且這種療法在 1960 年代之前一直被系統(tǒng)地用于治療癌癥患者���。如今,人們對(duì)使用類(lèi)似方法引發(fā)抗腫瘤免疫反應(yīng)的興趣仍然很高�����。Coley的開(kāi)創(chuàng)性工作是一個(gè)重要的標(biāo)志����,表明免疫系統(tǒng)的激活在根除癌癥方面發(fā)揮作用。盡管當(dāng)時(shí) Coley 毒素的作用機(jī)制尚不清楚����,但現(xiàn)在很清楚��,免疫反應(yīng)是由被稱(chēng)為病原體相關(guān)分子模式(PAMP)的保守細(xì)菌基序激活模式識(shí)別受體(PRR)觸發(fā)的。通過(guò)利用納米技術(shù)����,現(xiàn)在可以設(shè)計(jì)材料來(lái)展示 PAMP 以誘導(dǎo)免疫反應(yīng)�����,而不會(huì)出現(xiàn)嚴(yán)重?cái)⊙Y的風(fēng)險(xiǎn)。近日��,密歇根大學(xué)James J. Moon等人報(bào)告了一種納米顆粒的設(shè)計(jì)和開(kāi)發(fā)�����,該納米顆粒結(jié)合了源自真菌釀酒酵母的多糖甘露聚糖的結(jié)構(gòu)。通過(guò)與樹(shù)突狀細(xì)胞上眾所周知的 PRRs dectin-2 和 Toll 樣受體 4 (TLR4) 結(jié)合,修飾有甘露聚糖基序的納米顆粒作為PAMPs有效地誘導(dǎo)了先天性和適應(yīng)性免疫系統(tǒng)反應(yīng)的激活�����,并且不會(huì)引起明顯的毒性����。

真菌甘露聚糖是 T 輔助細(xì)胞 17 (TH17)反應(yīng)的有效誘導(dǎo)劑。研究人員表明,展示甘露聚糖的納米顆粒強(qiáng)烈誘導(dǎo)TH17介導(dǎo)的淋巴細(xì)胞分化�,使TH17和調(diào)節(jié)性 T (Treg) 細(xì)胞之間的平衡偏向激活細(xì)胞免疫反應(yīng)并遠(yuǎn)離Treg細(xì)胞的抑制作用���。值得注意的是���,納米粒子激活TH17和先天免疫細(xì)胞的能力導(dǎo)致了CD8細(xì)胞和NK細(xì)胞的瘤內(nèi)刺激�,并產(chǎn)生了有效的抗腫瘤作用��,正如作者在用納米粒子進(jìn)行瘤內(nèi)治療的小鼠身上所證明的那樣�����。作者還表明,在結(jié)腸癌和黑色素瘤的小鼠模型中�,通過(guò)將納米顆粒與 OX40 共刺激受體的激動(dòng)性抗體結(jié)合�,進(jìn)一步增強(qiáng)了納米顆粒的抗腫瘤作用�。
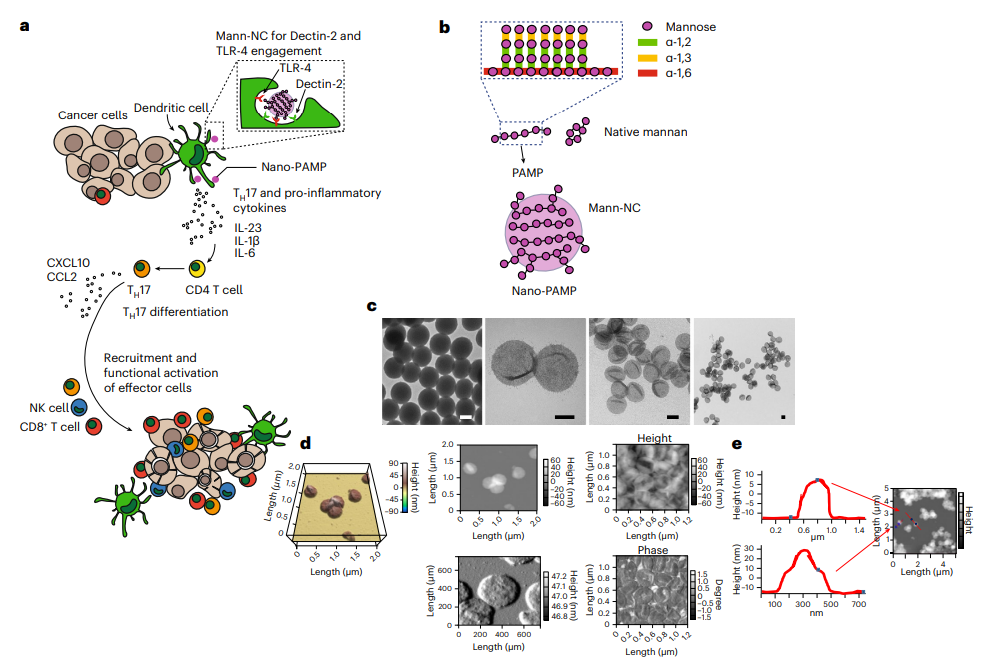
各種免疫細(xì)胞群對(duì)腫瘤的浸潤(rùn)是癌癥的標(biāo)志。根據(jù)它們的類(lèi)型和功能,腫瘤中的免疫細(xì)胞對(duì)疾病進(jìn)展有不同的影響����,并且它們的功能受到腫瘤微環(huán)境的影響�。事實(shí)上����,癌癥導(dǎo)致骨髓細(xì)胞生成增加�����,特別是單核細(xì)胞�、巨噬細(xì)胞和中性粒細(xì)胞的生成�����,這些細(xì)胞可以在腫瘤周?chē)e聚并改變其表型以促進(jìn)腫瘤生長(zhǎng)�����。這種免疫抑制性骨髓細(xì)胞也是檢查點(diǎn)抑制劑對(duì) CD8 激活和腫瘤消除產(chǎn)生有益影響的主要障礙�。此外�����,CD4淋巴細(xì)胞群(TH1����、TH2和TH17)釋放影響抗腫瘤免疫作用的內(nèi)源性介質(zhì)(如細(xì)胞因子)����。TH1 CD4淋巴細(xì)胞的作用與免疫監(jiān)視程序密切相關(guān),但人們對(duì)TH17淋巴細(xì)胞在癌癥中的作用及其作為免疫治療靶標(biāo)的潛力知之甚少。最近表明�,過(guò)繼轉(zhuǎn)移的TH17 細(xì)胞可減少腫瘤生長(zhǎng)����,并且腫瘤相關(guān)白細(xì)胞介素17 (IL-17) 與癌癥患者的生存相關(guān)����。但是如何在體內(nèi)誘導(dǎo)這種抗腫瘤作用尚不清楚。
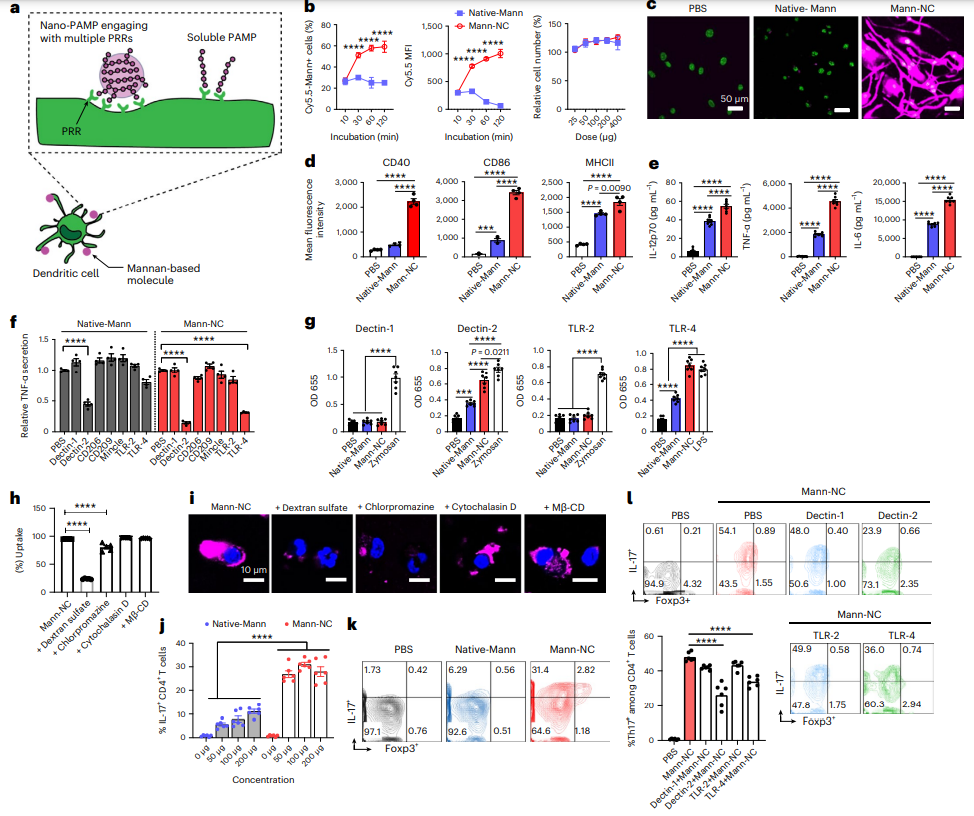
圖|Mann NC激活Dectin-2和TLR-4并誘導(dǎo)IL-17+CD4+T細(xì)胞
該研究的發(fā)現(xiàn)在多個(gè)層面帶來(lái)了新的見(jiàn)解���。在病理生理水平上���,他們通過(guò)激活CD8和NK細(xì)胞驗(yàn)證了TH17反應(yīng)在誘導(dǎo)抗腫瘤機(jī)制中的重要性���;這為未來(lái)的免疫治療方法打開(kāi)了大門(mén)����。研究人員還報(bào)告了dectin-2 和 TLR4 在此過(guò)程中的作用;這可能有助于開(kāi)發(fā)作用于這些受體水平的調(diào)節(jié)療法�����,用于以免疫抑制(通過(guò)刺激劑)或炎癥和自身免疫(通過(guò)抑制方法)為特征的病癥����。在技術(shù)層面,作者展示了設(shè)計(jì)含有復(fù)雜微生物聚糖(在他們的例子中是甘露糖酵母)的納米顆粒的可能性���,并且納米顆粒顯示出重要的抗腫瘤作用。其他真菌聚糖��,尤其是 β-葡聚糖�,已被證明在癌癥實(shí)驗(yàn)?zāi)P椭邪l(fā)揮有效的抗腫瘤作用,但這些作用被歸因于誘導(dǎo)訓(xùn)練有素的先天免疫��。甘露聚糖納米顆粒對(duì)先天免疫激活的誘導(dǎo)很可能導(dǎo)致長(zhǎng)期訓(xùn)練免疫誘導(dǎo)(除了TH17分化)�;是否是這種情況需要在后續(xù)研究中進(jìn)行調(diào)查。并且�����,在治療水平上����,作者展示了由甘露聚糖修飾的納米顆粒誘導(dǎo)的TH17分化和激動(dòng)性抗體激活 OX40 的強(qiáng)烈協(xié)同作用��。這支持了這樣一種觀點(diǎn)����,即一般來(lái)說(shuō)�,聯(lián)合癌癥免疫療法可能比單一療法更有效。
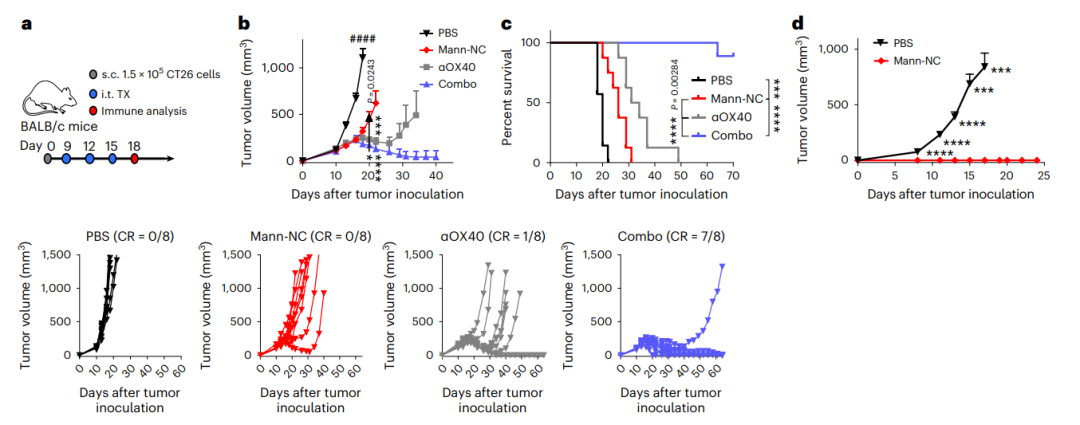
圖|Mann-NC 和 αOX40 組合引發(fā)強(qiáng)大的免疫激活和強(qiáng)大的抗腫瘤作用甘露聚糖是復(fù)雜的結(jié)構(gòu),可與各種先天性和適應(yīng)性免疫細(xì)胞上的多個(gè) PRR 相互作用�����。甘露聚糖修飾的納米粒子發(fā)揮其作用的任何其他潛在機(jī)制的相關(guān)性��,包括先天免疫系統(tǒng)水平的作用����,例如誘導(dǎo)受過(guò)訓(xùn)練的免疫力(也可以誘導(dǎo)抗腫瘤反應(yīng)),需要進(jìn)一步研究�����。此外��,需要區(qū)分納米粒子本身的免疫刺激和抗腫瘤作用�����。其他納米顆粒系統(tǒng),例如 COVID-19 疫苗中使用的脂質(zhì)納米顆粒��,可以引起強(qiáng)烈的炎癥反應(yīng)���。因此��,需要研究任何炎癥介導(dǎo)的不良反應(yīng)�����。甘露聚糖修飾的納米顆粒和抗 OX40 激動(dòng)性抗體的組合似乎在轉(zhuǎn)化方面很有前景��,因此值得優(yōu)化納米顆粒用于靜脈內(nèi)給藥����。此外�����,重要的是要研究納米粒子是否也可以增強(qiáng)抗體對(duì)免疫檢查點(diǎn)(例如PD-1 或CTLA-4)的影響�,以及其他類(lèi)型免疫治療的作用����。帶有激活 PRR 的 PAMPS 的納米顆粒可能會(huì)導(dǎo)致新的免疫療法。Son, S., Nam, J., Kim, A.S. et al. Induction of T-helper-17-cell-mediated anti-tumour immunity by pathogen-mimicking polymer nanoparticles. Nat. Biomed. Eng (2022).https://doi.org/10.1038/s41551-022-00973-4