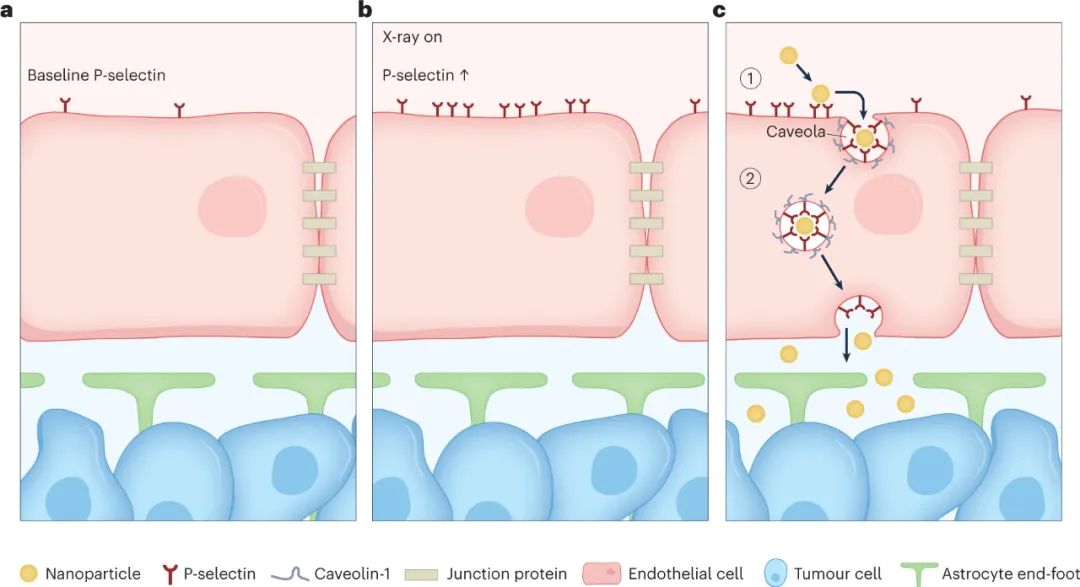
髓母細胞瘤是小腦實體惡性腫瘤的一種����,是最常見的小兒腦腫瘤��。四種髓母細胞瘤亞型中的三種表現出完整的功能性血腦屏障��。血腦屏障是一個受到嚴格調控的神經血管單元,由連續的內皮細胞層組成����,在細胞-細胞界面�����、周細胞和星形膠質細胞端足處具有緊密連接蛋白���,它們共同維持正常的腦功能和體內平衡�。這個神經血管單元創造了一個生物屏障,限制了質量運輸和藥物向大腦的有效輸送。為了安全有效地治療腦腫瘤,例如髓母細胞瘤��,需要新的藥物輸送技術來克服血腦屏障��。當前的臨床挑戰是將腫瘤治療藥物有效地輸送到大腦中�����。血腦屏障極大地限制了到達大腦的藥物量,導致治療效果降低和在健康組織和器官中脫靶藥物積累,這會引起嚴重的毒性相關副作用���。解決這一遞送挑戰是正在進行的臨床前和臨床研究的主要焦點,這些研究使用:(1)分子策略,例如受體介導的轉胞吞作用、載體介導的轉胞吞作用或擴散和細胞旁路轉運����;(2) 物理和化學策略���,如聚焦超聲與微泡�����、納米粒子或滲透傳遞;(3) 基于細胞和病毒的策略���,例如免疫和干細胞遞送,或腺病毒介導的基因療法。然而,這些新興戰略仍需進一步發展����,迫切需要更具體�����、更高效的遞送方式。一種有前途的方法是內皮轉胞吞作用,將抗癌納米藥物輸送到大腦中��。近日���,斯隆—凱特林癌癥研究所Daniel A. Heller�、G. Praveen Raju等人在 Nature Materials 上描述了褐藻糖膠(fucoidan)納米顆粒通過內皮細胞跨細胞機制,即通過觸發納米顆粒在血腦屏障這些細胞內部的運輸,有效地將癌癥藥物維莫德吉(vismodegib)輸送到髓母細胞瘤組織�。

在對超聲刺猬髓母細胞瘤小鼠模型進行給藥后��,納米顆粒與 P-選擇素結合,P-選擇素是一種細胞表面受體,其在腫瘤相關內皮細胞上的表達先前已通過 X 射線照射得到增強。納米顆粒通過褐藻糖膠與 P-選擇素受體結合���,觸發轉胞吞作用過程,導致載藥納米顆粒從腫瘤內皮細胞腔內轉運至腫瘤內皮腔外側,從而使vismodegib能夠更有效地輸送到髓母細胞瘤腫瘤����。內皮細胞在報道的遞送策略中起著核心作用����,因為這些細胞表達 P-選擇素受體�����,并通過轉胞吞作用進一步主動將納米顆粒轉運穿過腫瘤內皮細胞�。其他細胞表面受體已在文獻中報道�����,用于大腦中基于轉胞吞作用的藥物遞送應用���。例如包括轉鐵蛋白受體�����、胰島素受體����、低密度脂蛋白受體 (LDLR) 和 LDLR 相關蛋白1 受體。然而����,這些受體無處不在�����,導致外周和脫靶遞送,從而損害治療的安全性和有效性�。腫瘤相關內皮細胞上高水平的特異性受體表達對于最大限度地減少脫靶遞送和毒性至關重要���。研究人員將 P-選擇素鑒定為激活的腦腫瘤相關內皮細胞上的候選受體����。P-選擇素是一種細胞粘附分子�,可與循環白細胞上的 P-選擇素糖蛋白配體-1 結合,將它們募集到發炎部位�。P-選擇素進一步結合多糖�,如硫酸乙酰肝素和褐藻糖膠��。P-選擇素表面受體的表達發生在受炎癥細胞因子或輻射刺激的活化內皮細胞上���。研究人員通過X射線照射增強了腫瘤相關內皮細胞中P-選擇素的表達��,同時保留了鄰近的健康腦組織。所證明的輻射治療提供了對P-選擇素表達的時空控制�。
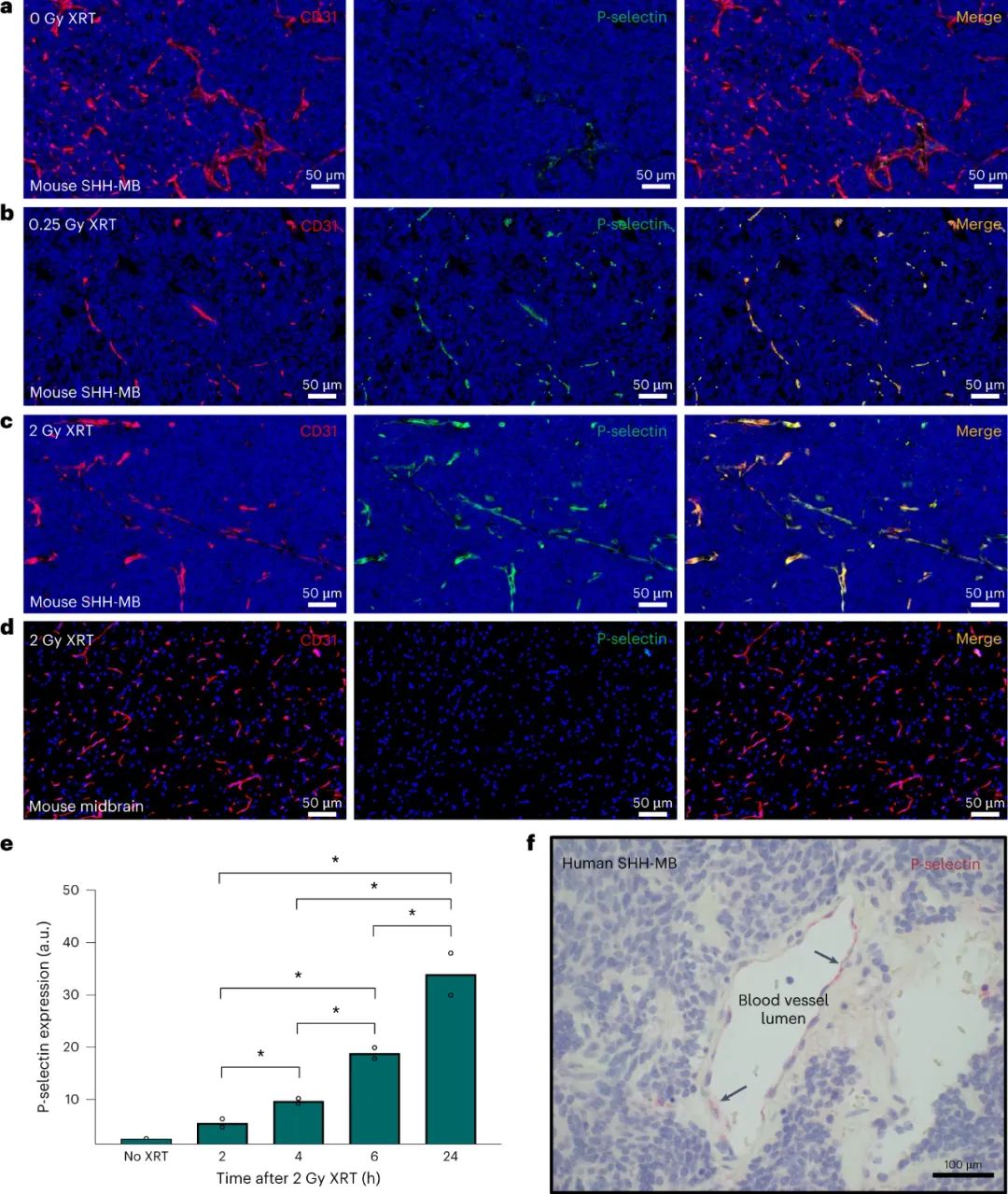
圖|低劑量照射誘導髓母細胞瘤腫瘤血管中P-選擇素的表達
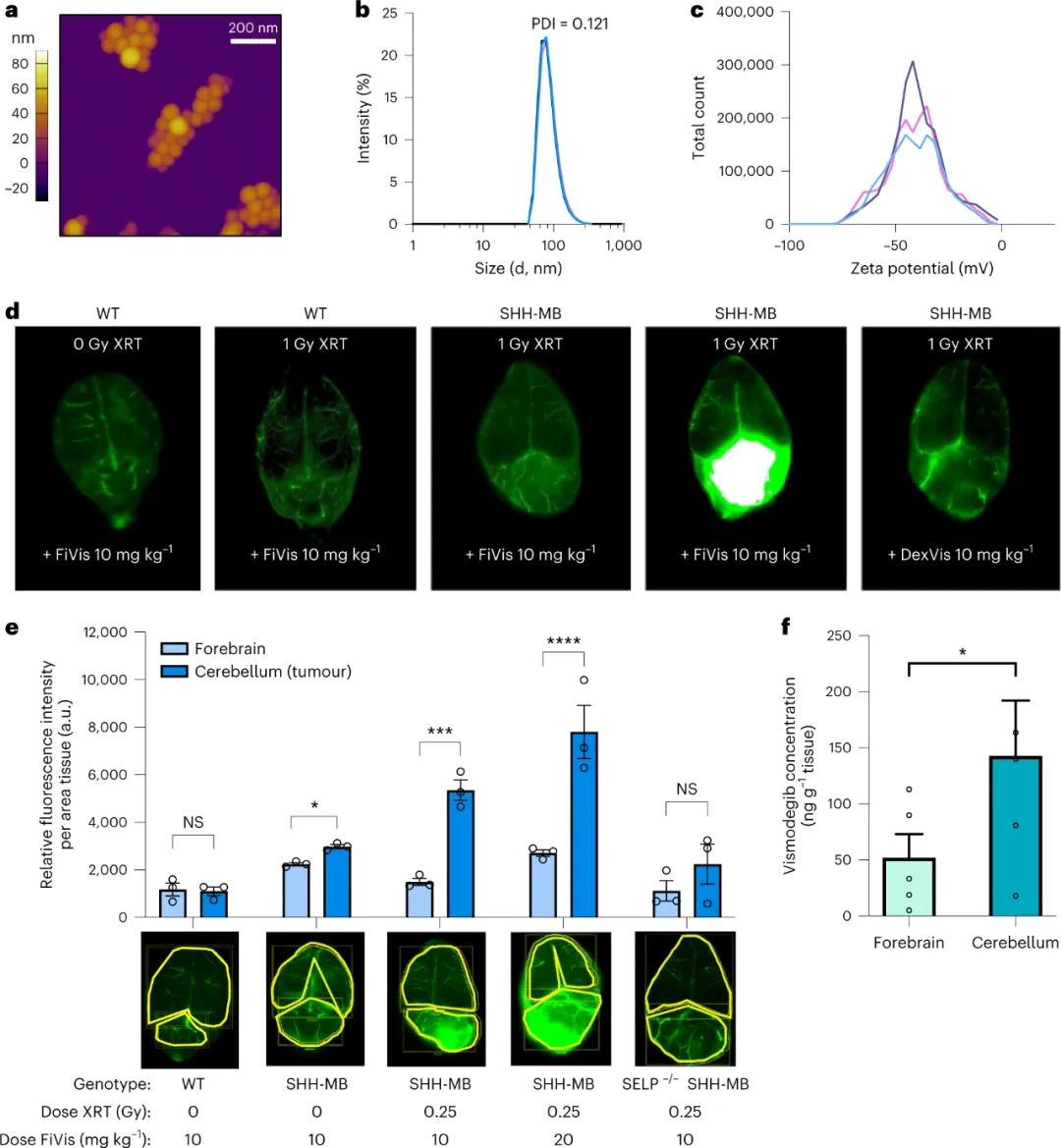
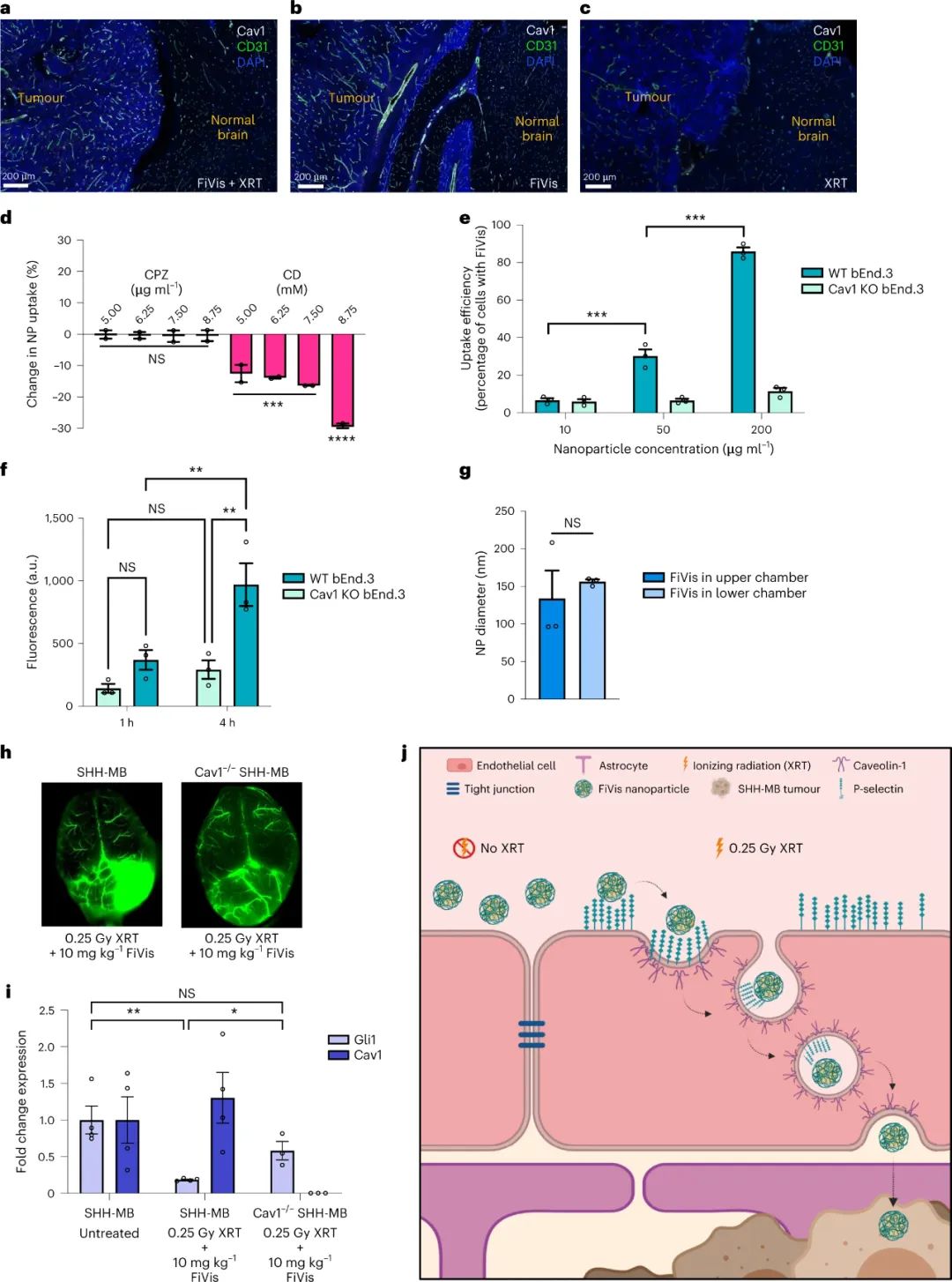
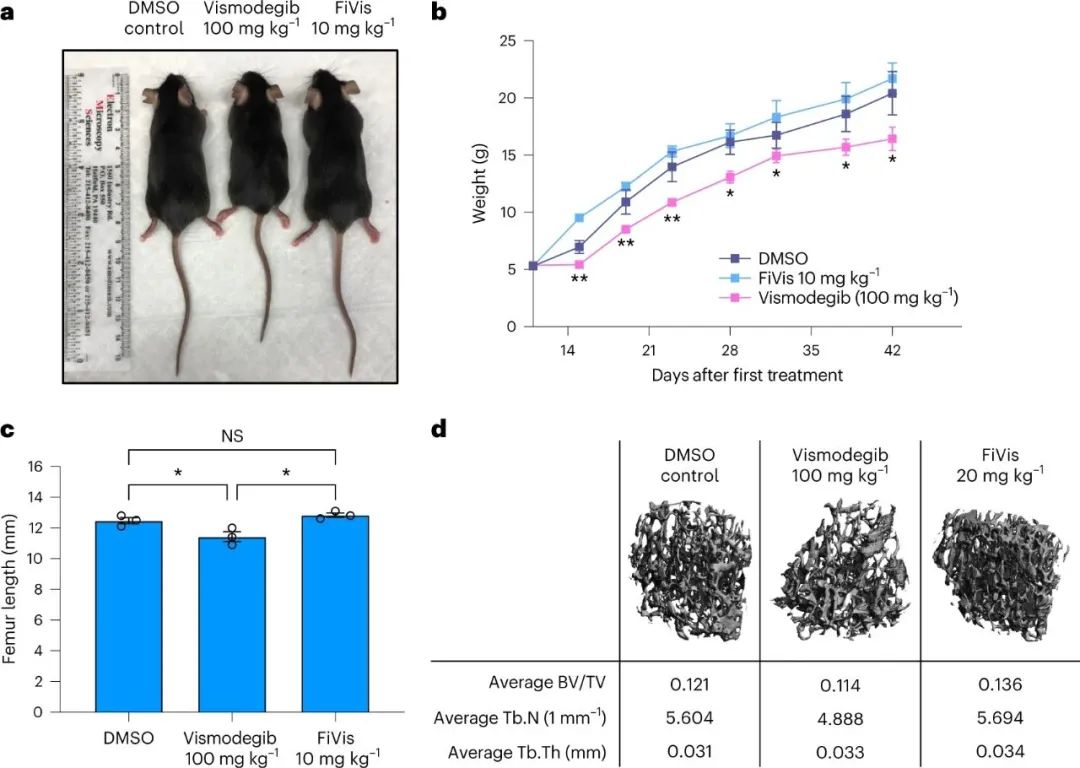
圖|低劑量照射后�,P-選擇素靶向納米顆粒優先靶向SHH-MB腫瘤該研究的另一個有趣發現是由管腔側的內吞作用引發的后續納米顆粒轉胞吞作用����。轉胞吞作用過程依賴于caveolin-1,一種參與細胞膜穴樣內陷介導的細胞內轉運的蛋白質�����。研究人員使用基因工程的聲波刺猬髓母細胞瘤小鼠模型�����,展示了在 0.25 Gy 的 X 射線治療后高效的巖藻多糖納米顆粒轉胞吞作用和藥物遞送至腫瘤組織�。雖然作者沒有研究細胞內囊泡分選和腔外胞吐作用的機制���,但有效的納米顆粒遞送表明有效的轉胞吞作用導致vismodegib治療髓母細胞瘤的治療指數提高�。圖|FiVis納米顆粒通過血腦屏障是由Cav1介導的圖|FiVis納米顆粒消除了vismodegib治療對幼鼠的骨毒性因此,內皮轉胞吞作用可能是一種優雅的策略�����,可以有效地將納米粒子輸送到各種實體瘤類型����,從而有可能實現更安全、更有效的納米醫學治療���。根據最近的證據表明納米顆粒進入實體瘤的主要機制是主動的內皮轉胞吞作用,作者的研究還支持該領域尋求提高納米顆粒遞送效率的新方法�。然而�����,需要更多的研究來探索這種用于納米藥物開發的遞送策略的臨床可行性。例如���,有機會研究輻射誘導的 P-選擇素表達靶向在其他實體瘤模型中的普遍性,同時進一步評估血小板和其他內皮細胞同時表達 P-選擇素的潛在安全風險��。用納米藥物靶向 P-選擇素可能會進一步影響受體的生理功能和炎癥或某些免疫療法期間白細胞募集的可用性���。此外��,需要對內皮轉胞吞作用進行更詳細的機制研究,以充分了解納米藥物對實體瘤(包括髓母細胞瘤)的療效。總的來說�,這項研究展示了內皮轉胞吞作用克服基于納米顆粒的藥物遞送中的生物障礙的令人興奮的機會���。利用內皮轉胞吞作用途徑可能會促進更安全����、更有效的癌癥納米藥物的開發�,用于治療腦部惡性腫瘤和其他潛在的實體瘤。Tylawsky, D.E., Kiguchi, H., Vaynshteyn, J. et al. P-selectin-targeted nanocarriers induce active crossing of the blood–brain barrier via caveolin-1-dependent transcytosis. Nat. Mater. 22, 391–399 (2023).https://doi.org/10.1038/s41563-023-01481-9