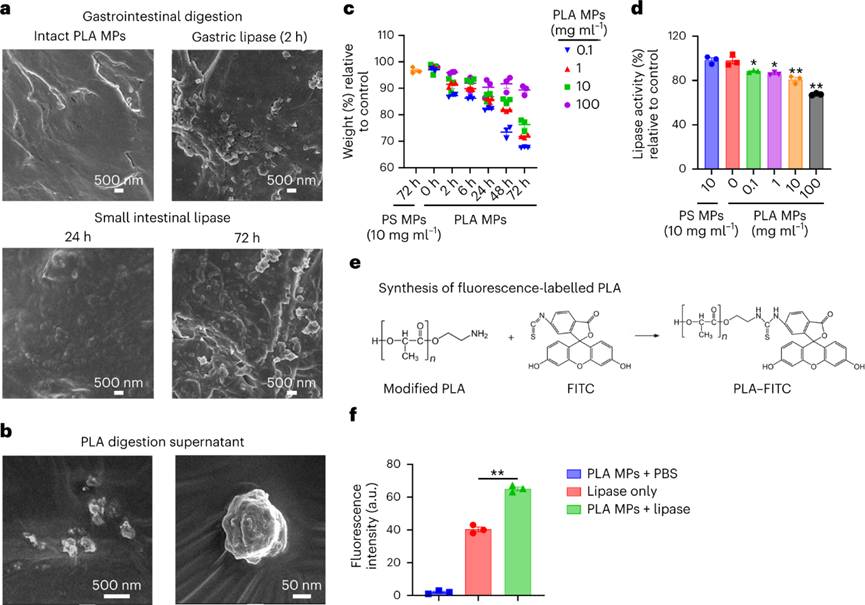
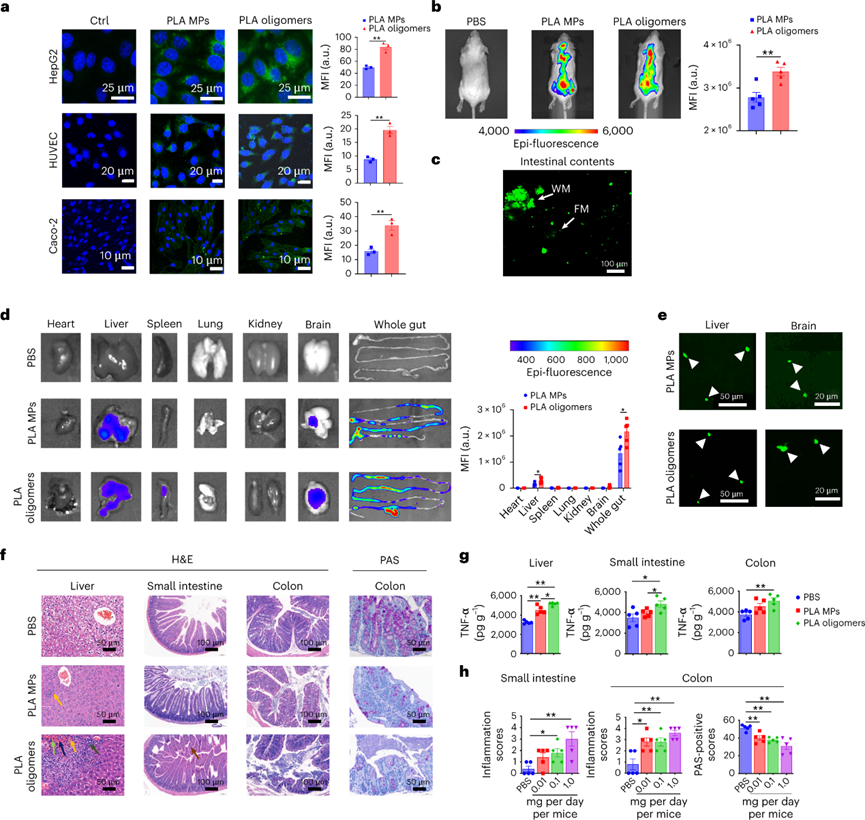
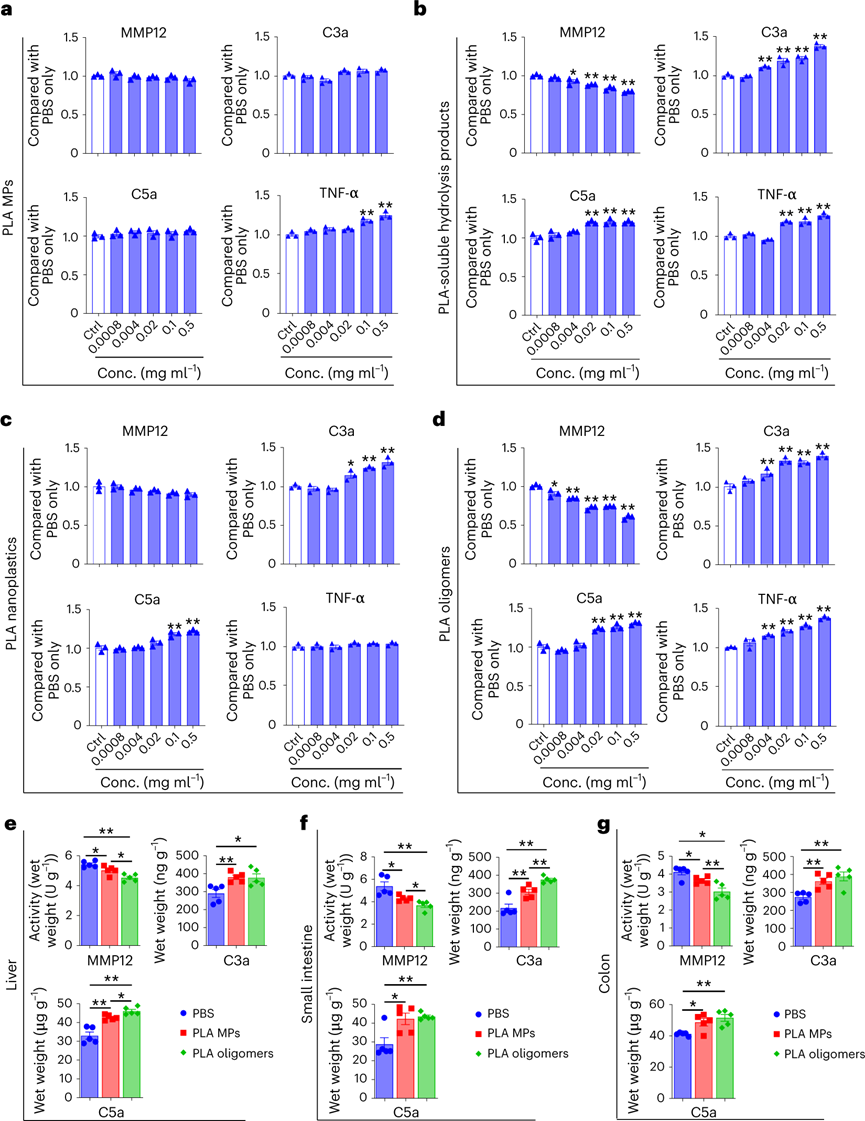
白色污染是一個(gè)老生常談的環(huán)境問題,雖然世界各國出臺(tái)了各式的法案進(jìn)行處理,但是這些污染降解形成的微塑料(MP)在水生和陸地環(huán)境中無處不在。由于其對(duì)環(huán)境和人類健康的潛在風(fēng)險(xiǎn),是世界上最緊迫的環(huán)境問題。MP在環(huán)境中轉(zhuǎn)移,并通過食物鏈和直接吸入或攝入人體進(jìn)行生物積累。盡管人類MP暴露的確切數(shù)量涉及很大的不確定性,但研究初步估計(jì),通過口服攝入的每周MP消耗量范圍為0.1至5.0克MP顆粒。對(duì)小鼠、牡蠣和貽貝的研究表明,接觸與環(huán)境相關(guān)的MP會(huì)導(dǎo)致生殖受損、DNA損傷和神經(jīng)毒性,而導(dǎo)致這些影響的機(jī)制仍然是未知的。為了減輕塑料污染,人類使用可生物降解塑料作為傳統(tǒng)塑料的替代品。生物塑料聚乳酸(PLA)就廣泛用于制造食品包裝,一次性餐具和生物醫(yī)學(xué)遞藥載體。但是在人類和小鼠模型研究中表明,基于PLA的植入會(huì)引發(fā)炎癥。同時(shí)PLA塑料可能比傳統(tǒng)塑料產(chǎn)生更多的MPs,所以PLA MPs越來越多地存在于土壤,沉積物和室內(nèi)灰塵中。PLA MP攝入的毒理學(xué)值得進(jìn)一步深入研究,學(xué)界仍然缺乏關(guān)于它們?cè)谀c道中的生物轉(zhuǎn)化如何影響人類健康的認(rèn)知。近日,復(fù)旦大學(xué)環(huán)境科學(xué)與工程系的陳建民教授、南洋理工大學(xué)土木與環(huán)境工程學(xué)院的方明亮教授、安徽醫(yī)學(xué)大學(xué)黃以超教授等人報(bào)道了一項(xiàng)關(guān)于“環(huán)保”可降解塑料對(duì)人類胃腸道與健康風(fēng)險(xiǎn)影響的工作。作者證明了聚乳酸微塑料通過在胃腸道中競爭甘油三酯脂肪酶來水解,產(chǎn)物通過自組裝形成低聚納米塑料顆粒。在小鼠模型中,聚乳酸低聚物及其納米顆粒在肝臟、腸道和大腦中生物積累。同時(shí)暴露于聚乳酸低聚物后會(huì)導(dǎo)致不良腸道炎癥作用。雖然,可生物降解塑料被認(rèn)為是解決環(huán)境塑料污染的解決方案,但生物塑料的胃腸道降解和毒性也必須有所認(rèn)知。首先測試PLA MPs與不同的消化液反應(yīng)。在人工胃和腸液中進(jìn)行體外消化后,SEM圖像顯示PLA MPs的表面粗糙。進(jìn)一步用胃脂肪酶處理PLA MPs,其表面表現(xiàn)出實(shí)質(zhì)性的改變。將PLA MPs在含有小腸脂肪酶的PBS中生物降解3天。SEM分析表明,隨著孵育時(shí)間的延長,表面磨損增加。在小腸脂肪酶中生物降解的PLA MPs質(zhì)量在6小時(shí)后迅速減少了其初始質(zhì)量的15%。脂肪酶處理后PLA MPs的分子和晶體結(jié)構(gòu)沒有實(shí)質(zhì)性變化。因此,這表明MP可能分別被胃和腸液中的脂肪酶降解。脂肪酶在胃和腸液中水解PLA,可能是基于PLA的羧酯鍵和脂肪酶的豐度。進(jìn)一步評(píng)估PLA和消化脂肪酶之間的相互作用,使用甘油三酯作為陽性對(duì)照。PLA結(jié)合消化脂肪酶,通過競爭性結(jié)合阻止甘油三酯降解。消化過程中納米級(jí)塑料顆粒形成機(jī)制:通過體外消化模型,研究納米級(jí)塑料顆粒形成機(jī)制。PLA在胃脂肪酶消化2小時(shí)后在培養(yǎng)基上清液中形成了每毫升6.09 × 108個(gè)顆粒。這種小納米塑料顆粒的形成呈現(xiàn)劑量依賴性,前3小時(shí)顯示出最大的產(chǎn)量,這可能是由于生成的顆粒或相關(guān)低聚物解聚。酶解2 h后PLA納米顆粒的平均尺寸為200 nm,酶解1 d后的平均尺寸為50 nm,在接下來的連續(xù)兩天內(nèi)趨于穩(wěn)定。TEM圖像顯示納米塑料具有多個(gè)中心核心,表明顆粒可能發(fā)生自我聚集。GPC分析顯示,在消化的PLA MP中低分子量范圍(~900 Da)中存在微小的峰,這可能是解聚低聚物。使用高分辨率質(zhì)譜法對(duì)低聚物單元的進(jìn)一步分析表明,八單元低聚物的豐度最高。研究了釋放的PLA低聚物對(duì)脂肪酶酶活性的影響。分子動(dòng)力學(xué)模擬表明,PLA低聚物通過與Ser153、His264和Asp177催化三聯(lián)體的氫鍵占據(jù)了脂肪酶的活性位點(diǎn)。同樣,PLA低聚物-脂肪酶相互作用的親和力高度依賴于單元數(shù),因?yàn)楦嗟膯卧纬筛鼜?qiáng)的氫鍵。PLA的羧碳與Ser153的羥基氧之間的距離比甘油三酯的距離更近,表明親核進(jìn)攻容易發(fā)生。此外,由于沒有氫鍵,甘油三酯對(duì)催化位點(diǎn)的結(jié)合親和力較PLA低聚物的結(jié)合親和力弱。PLA低聚物的過渡態(tài)具有0.11 eV的相對(duì)能壘,表明一旦Ser153脂肪酶親核進(jìn)攻羧基,后續(xù)的催化步驟可能會(huì)自發(fā)發(fā)生。為了研究釋放的納米塑料或低聚物是否可以在體外被肝細(xì)胞吸收,用熒光PLA納米塑料和低聚物處理HepG2。兩幅圖像都顯示出高信號(hào)強(qiáng)度,PLA低聚物發(fā)出更高的信號(hào)。對(duì)小鼠施用熒光PLA MP和低聚物一周,并追蹤它們的組織生物分布和腸道內(nèi)容物。根據(jù)目前的數(shù)據(jù)顯示,人類每周可能攝入~0.1-5.0克MP,小鼠最初以每天1.0mg的速度給予PLA MP和低聚物。熒光結(jié)果顯示,PLA廣泛分布于小鼠體內(nèi)。此外,攝入的PLA MPs以小片段(亞微米)的形式存在于腸道中。PLA納米粒子和低聚物的熒光信號(hào)主要集中在肝臟、腸道和結(jié)腸。在肝臟和大腦切片中業(yè)觀察到了不同程度的熒光斑點(diǎn)。并且低聚物處理小鼠中觀察到肝臟和腸道中的更強(qiáng)信號(hào)。組織病理學(xué)顯示,用PLA MPs刺激的小鼠表現(xiàn)出肝臟,小腸和結(jié)腸的炎癥和浸潤。與對(duì)照組相比,結(jié)腸PAS染色檢測到腸道粘液減少。低聚物同樣引起了這些不利作用且效率更高。肝臟,小腸和結(jié)腸中促炎細(xì)胞因子TNF-α濃度顯著升高。進(jìn)一步給予與人類攝入水平相近的PLA MP,其小鼠小腸和結(jié)腸均有炎癥,減少小腸和結(jié)腸中的粘液產(chǎn)生。圖 PLA納米塑料/低聚物在體外和體內(nèi)的生物分布和組織病理學(xué)低聚物介導(dǎo)炎癥的蛋白質(zhì)靶標(biāo):為了確定誘導(dǎo)炎癥的潛在機(jī)制,首先測試了腸道微環(huán)境的pH值,因?yàn)镻LA的水解會(huì)釋放酸性基團(tuán)。但在給定劑量下,緩沖溶液的效力變化很小。進(jìn)一步假設(shè)低聚物通過直接與某些促炎蛋白相互作用來調(diào)節(jié)炎癥。雖然沒有關(guān)于PLA低聚物-蛋白質(zhì)相互作用的已發(fā)表數(shù)據(jù),但使用藥效團(tuán)模型計(jì)算八聚體與16,646種蛋白質(zhì)的結(jié)合親和力。通過合并GPC結(jié)果和質(zhì)譜數(shù)據(jù)進(jìn)行篩選。結(jié)果顯示,PLA(8個(gè)單位)-基質(zhì)金屬蛋白肽酶12(MMP12)的適應(yīng)度得分最高。計(jì)算分析進(jìn)一步表明,10個(gè)單元后,與低聚物單位長度對(duì)應(yīng)的MMP12催化位點(diǎn)的親和力趨于穩(wěn)定。進(jìn)一步發(fā)現(xiàn),隨著PLA單位的增加,PLA的羧氧與鋅離子發(fā)生靜電相互作用。當(dāng)?shù)途畚飭卧臄?shù)量達(dá)到11個(gè)時(shí),這種靜電力開始顯著減弱。假設(shè)PLA低聚物和MMP12之間的疏水和氫鍵作用較弱,主要是羧基氧和鋅離子之間靜電作用。為了進(jìn)一步驗(yàn)證這種相互作用,進(jìn)行等溫滴定量熱法分析,結(jié)果表明MMP12與純PLA低聚物以及與水解產(chǎn)物的結(jié)合親和力(Kd)的分別為13.3和20.5μM。為了研究低聚物的免疫毒性,測量MMP12的生物活性以及低聚物處理的RAW 264.7產(chǎn)生的C3a,C5a和TNF-α濃度。用PLA MPs、PLA納米塑料、PLA低聚物以及可溶性水解產(chǎn)物處理,均會(huì)使MMP12生物活性減弱,同時(shí)C3a,C5a和TNF-α濃度升高。這種炎癥因子濃度的變化與刺激物的濃度呈現(xiàn)正相關(guān)。小鼠模型的體內(nèi)表型數(shù)據(jù)進(jìn)一步證實(shí)了用PLA MP和PLA低聚物刺激會(huì)引發(fā)MMP12生物活性的降低。同時(shí)肝臟,小腸和結(jié)腸中C3a和C5a的濃度增加。相比于PLA MP而言,低聚物引起了更劇烈的炎癥作用,這進(jìn)一步證實(shí)了低聚物的免疫調(diào)節(jié)作用。圖 PLA低聚物介導(dǎo)的MMP12失活誘導(dǎo)腸道炎癥可生物降解塑料已被提議作為解決“可持續(xù)性”塑料問題的主要解決方案。然而,這些替代品是否對(duì)人類健康構(gòu)成重大風(fēng)險(xiǎn)還遠(yuǎn)未得到了解。人類在日常生活中攝入大量可生物降解的塑料,胃腸道會(huì)直接改變它們的化學(xué)結(jié)構(gòu),從而改變它們的代謝、生物利用度和生物效應(yīng)。雖然這些塑料在自然環(huán)境中很容易降解,但其與人類健康相關(guān)的腸道轉(zhuǎn)化機(jī)制的了解還處于早期階段。作者團(tuán)隊(duì)證明了,胃和腸道脂肪酶對(duì)PLA MP的降解都有相當(dāng)大的影響。此外,PLA是甘油三酯特異性脂肪酶的底物,與人類健康具有重要相關(guān)性。納米級(jí)塑料顆粒的釋放速度快于預(yù)期,酶解僅3 h后就形成釋放峰。人體腸道在消化過程中產(chǎn)生更小的納米塑料(~50納米)。這些納米塑料的尺寸非常小,使它們更容易滲透到胃腸道,進(jìn)入循環(huán)系統(tǒng)到達(dá)其他組織,并進(jìn)一步賦予腸道健康風(fēng)險(xiǎn)。PLA低聚物對(duì)脂肪酶活性的直接抑制作用,有效地競爭甘油三酯與脂肪酶的特異性結(jié)合。與膳食脂肪相比,PLA的數(shù)量通常要少得多。因此,與脂質(zhì)消化和吸收相關(guān)的人類健康影響需要進(jìn)一步群體驗(yàn)證。在實(shí)際人類暴露劑量下的PLA MPs刺激小鼠的腸道和結(jié)腸中存在嚴(yán)重炎癥。觀察到的炎癥很可能是由水解和自組裝的低聚物引發(fā),而不是由PLA的顆粒碎片直接引起。八聚體作為PLA水解中的主要低聚物,使用配體-蛋白質(zhì)相互作用模型來篩選主要藥物靶蛋白中的可能靶標(biāo)。PLA低聚物對(duì)關(guān)鍵免疫調(diào)節(jié)劑MMP12的滅活也許可以解釋PLA在免疫調(diào)節(jié)中的作用。MMP12作為關(guān)鍵介質(zhì),為炎癥的消退奠定基礎(chǔ),因?yàn)樗诳刂平M織緊致性和通透性方面起主要作用。此外,MMP12使補(bǔ)體C3失活以減少補(bǔ)體活化,并使化學(xué)引誘藥過敏毒素C3a和C5a失活。目前的研究對(duì)于人類暴露于MP的評(píng)估并不包括短鏈MP聚合物或潛在有毒的低聚物。但已發(fā)表的研究表明,聚合物中的低聚物很可能是聚合物毒性的主要貢獻(xiàn)者。聚丙烯奶瓶、硅膠橡膠嬰兒奶嘴、尼龍袋、熱飲杯和塑料茶包等等生活中的塑料制品可能已經(jīng)自行降解,并釋放了數(shù)萬億納米塑料與更多有毒的低聚物,這可能使得學(xué)界低估了人類MPs的總暴露量。很少有毒理學(xué)研究報(bào)告PLA低聚物的健康影響,特別是在人類相關(guān)劑量下。因此,該工作從一個(gè)方向解釋了PLA降解低聚物在腸道炎癥形成的分子基礎(chǔ)。總之,該工作的結(jié)果促進(jìn)了對(duì)可生物降解塑料降解產(chǎn)物作為有毒污染物的認(rèn)知。Mengjing Wang, Qianqian Li, Changzhi Shi, et al. Oligomer nanoparticle release from polylactic acid plastics catalysed by gut enzymes triggers acute inflammation. Nat Nanotechnol. 2023 Mar 2.https://www.nature.com/articles/s41565-023-01329-y