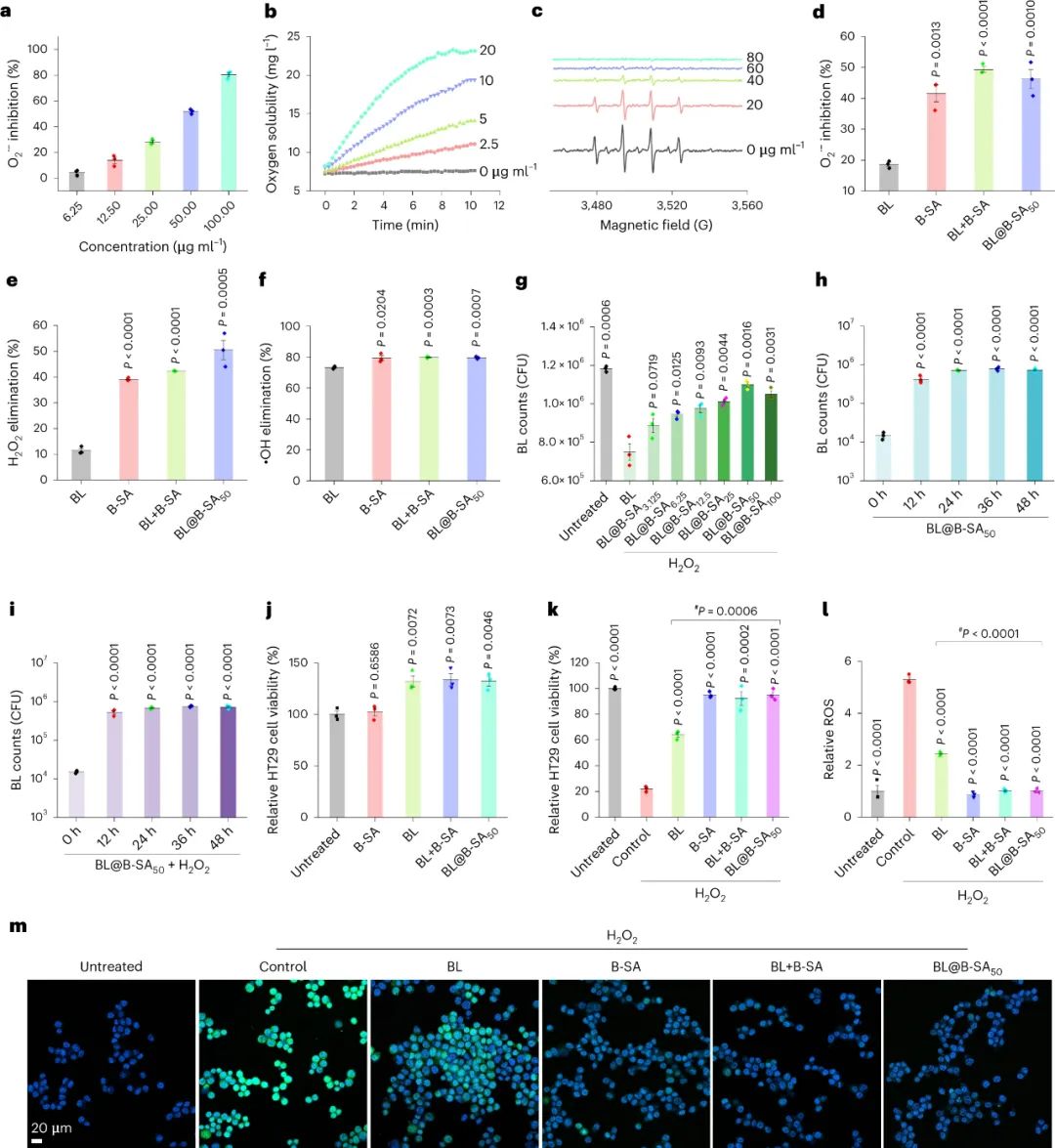
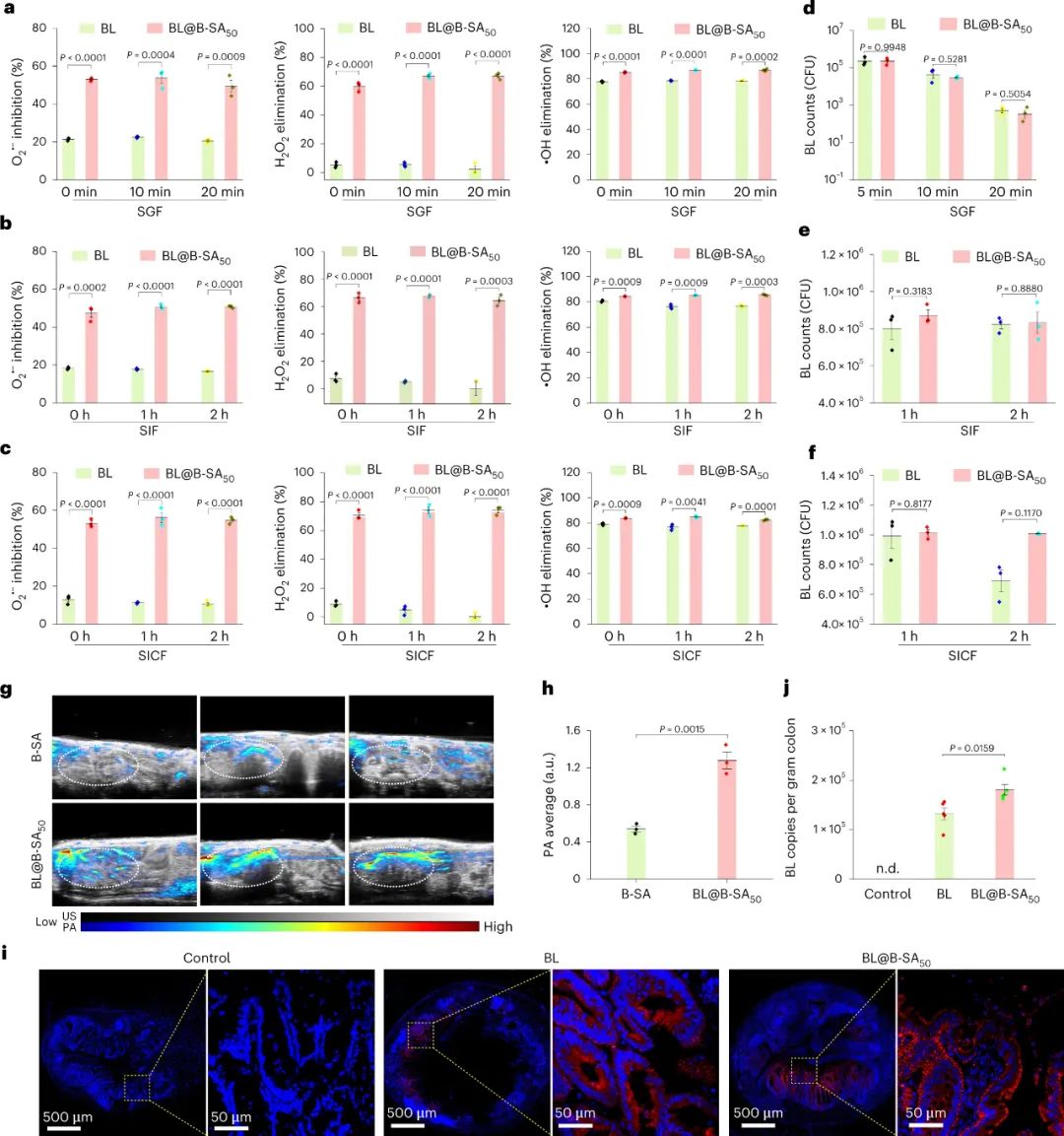
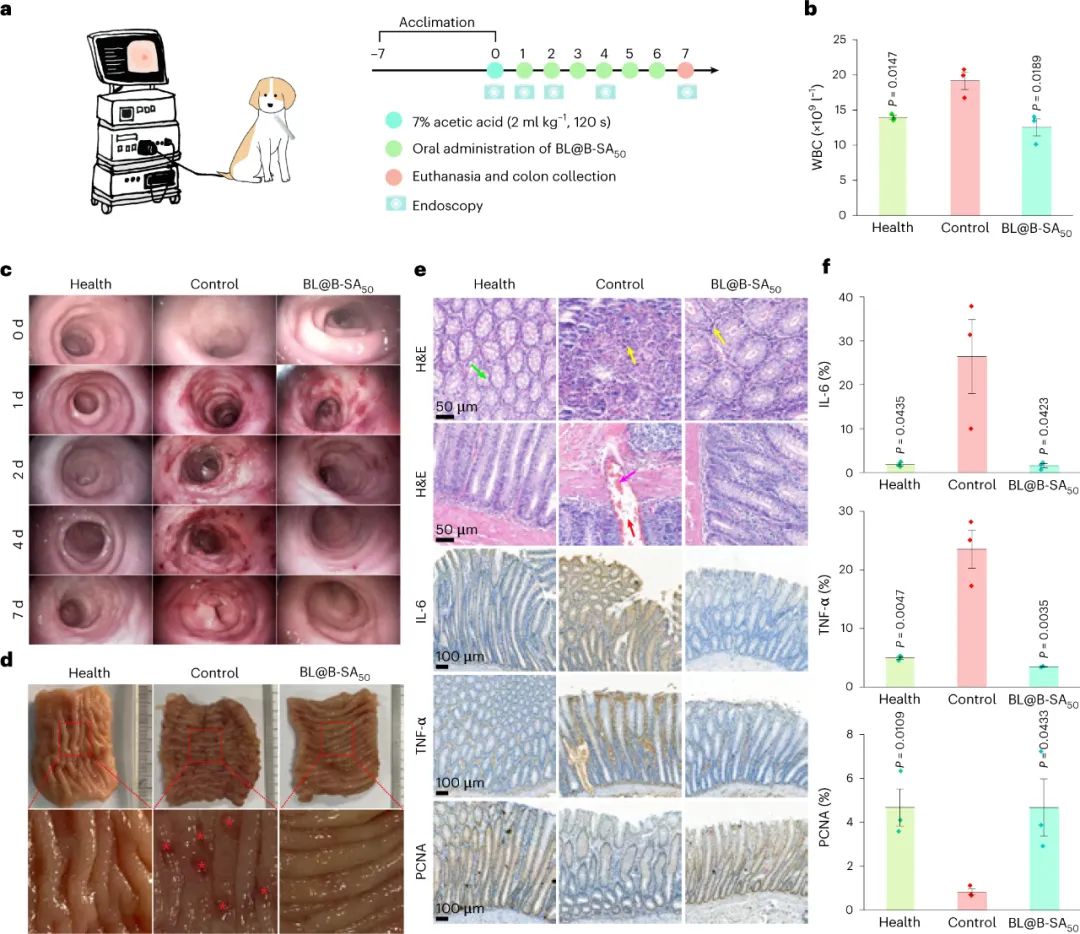
炎癥性腸病 (IBD) 是一類特發性腸道疾病,包括克羅恩病(CD)和潰瘍性結腸炎(UC)���,給全世界帶來健康和經濟負擔�����,并大大降低患者的生活質量���。盡管IBD的發病復雜且難以捉摸�����,但新出現的證據表明IBD與腸粘膜屏障功能障礙和細菌微生物群紊亂有關�����,隨后導致活性氧 (ROS) 和炎癥因子升高的過度活躍的免疫反應�。目前可用的臨床療法主要集中在通過抑制腸道炎癥負荷來改善疾病相關癥狀�����。盡管抗炎 5-氨基水楊酸鹽 (5-ASA) 和皮質類固醇甚至腫瘤壞死因子 (TNF) 拮抗劑的免疫抑制藥物具有強大的作用��,但它們并不能使所有患者受益。此外�,它們的長期使用可能導致嚴重的藥物不良反應����,包括死亡����,甚至增加感染和惡性腫瘤的風險。這些限制可能是由于這些傳統藥物的不可逆消耗、快速代謝和非選擇性相互作用造成的����。另一方面�����,口服益生菌療法已成為治療 IBD 的有前途的佐劑,它通過停留在腸道上以積極調節細菌組成的平衡并促進腸粘膜修復。然而,由于缺乏抗氧化酶��,如過氧化氫酶(CAT)和超氧化物歧化酶(SOD)����,這些嚴格厭氧的益生菌在IBD中易受ROS損傷�,從而降低治療效果并延長治療周期。對IBD的更有效和更安全的治療存在未滿足的需求��,它可以有效地靶向發炎的結腸并通過抑制炎癥���、重塑腸道屏障功能和調節感染組織中的腸道微生物組來快速重塑衛生的免疫微環境��。為了滿足這一需求�,浙江大學毛崢偉��、王偉林和新加坡國立大學陳小元等人構建了人工酶武裝的長雙歧桿菌(BL)益生菌來調節腸道炎癥�。

首先�,研究人員通過熱解金屬-有機骨架包裹的鐵前驅體制備了鐵單原子催化劑(Fe-SA)(Fe@MOF) 。所得的Fe SA顯示出菱形十二面體形狀����,平均尺寸為168nm�����。受快速簡便的基于硼酸鄰二醇的點擊反應的啟發,研究人員選擇了硼酸-聚乙二醇(C18–PEG-B)的連接體來結合厭氧BL和Fe-SA�。通過用C18–PEG-B功能化Fe-SA���,最初制備了模糊SA��,并顯示出增強的膠體穩定性。最后���,通過簡單地將不同比例的B-SA與BL混合,即可構建益生菌-人工酶系統BL@B-SAx�����。
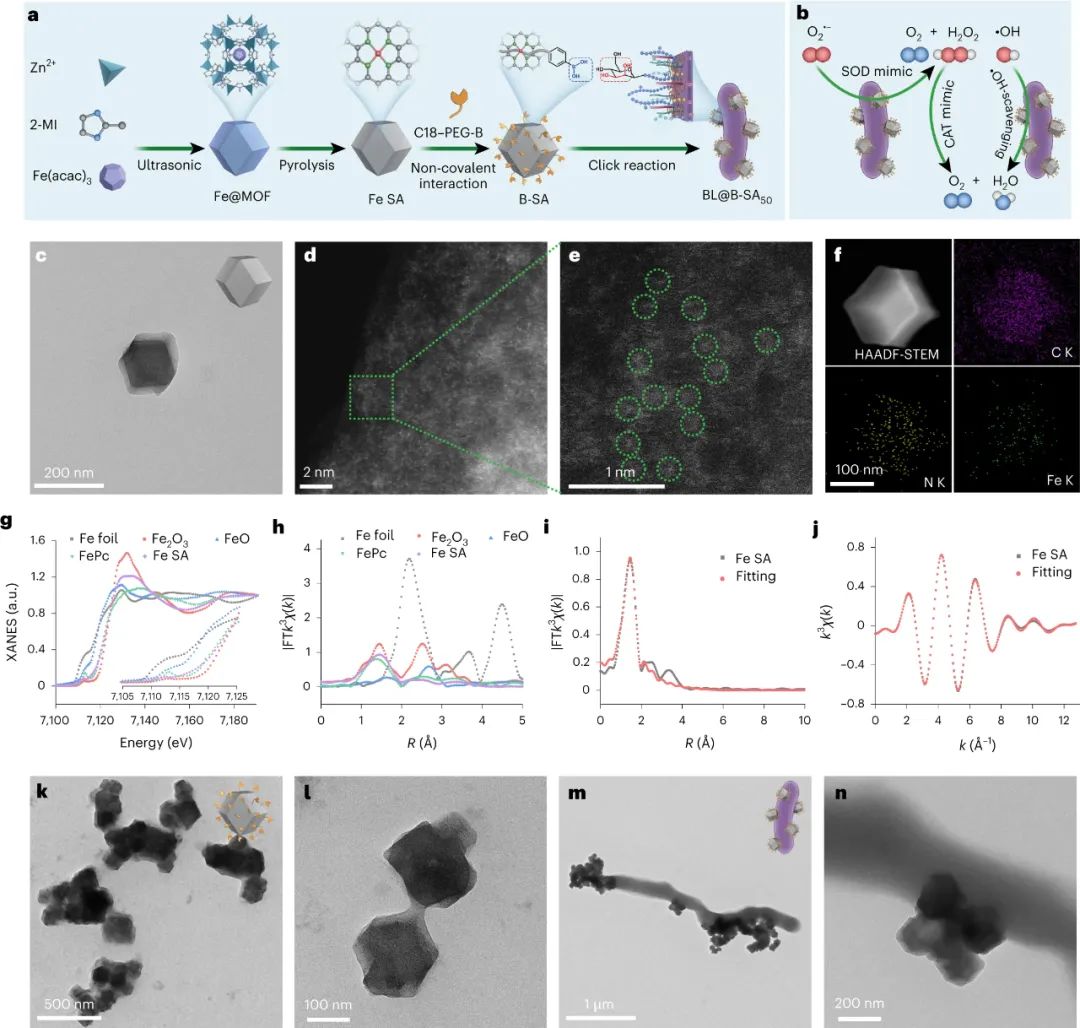
在該平臺中,單原子催化劑的人工酶(SAzymes)��,含有原子分散的活性金屬中心的納米材料����,被用于有效模擬天然抗氧化防御系統���,不僅可以替代臨床使用的抗炎藥���,還可以保護益生菌免受敵對應激源的影響����。具體而言,它們可以模仿SOD和CAT的抗氧化酶來清除超氧化物自由基(O2?-)和過氧化氫(H2O2)����,并作為抗氧化生物分子來消除羥基自由基(?OH)��,有力而迅速地緩解炎癥癥狀。此外��,它們可以作為益生菌的守護者����,保護這些被包裹的微生物免受發炎部位的氧化損傷,從而使屏障功能和腸道微生物組迅速轉向有益狀態�����。此外��,BL益生菌(一種常見的常駐細菌)不僅對宿主有健康益處�����,而且在結腸中具有優越的腸道定殖能力,確保了SAzymes在疾病部位可以得到持久的抗氧化治療�。因此�����,SAzymes武裝益生菌BL@B-SA50在UC和CD小鼠模型中�����,可以降低ROS水平���,抑制促炎細胞因子的產生��,恢復腸道屏障功能,并增加腸道微生物群的豐富性和多樣性。它們的治療潛力超過了臨床上使用的其他常規IBD療法��。圖|BL@B-SA50在發炎的結腸中的穩定性���、靶向性和保留性最重要的是�����,BL@B-SA50可以有效緩解TNBS引發的克羅恩?���。硪环NIBD)和乙酸引起的比格犬潰瘍性結腸炎的癥狀����,這與人類結腸炎的傳播和炎癥類型相似,大大加快了人工酶武裝益生菌在臨床轉化中的進程。在治療過程中�����,BL@B-SA50治療組的小鼠和狗在重復治療后未觀察到不良事件�����。這些結果共同突出了BL@B-SA50作為治療劑���,并支持針對不同類型IBD的進一步臨床評估�。圖|使用BL@B-SA50在比格犬身上進行UC治療綜上所述���,該研究用抗氧化人工酶改造BL益生菌��,以快速有效地調節IBD的微環境�。在這個系統中��,人工酶被用來模擬天然的抗氧化防御系統�,以取代臨床上使用的抗炎藥�。與臨床藥物相比,它們清除ROS以減少炎癥,具有持久的級聯催化和生物安全的優勢�����。反過來�����,炎癥環境的緩解提高了細菌的生存能力���,從而迅速重塑腸道屏障功能和腸道微生物群�����。這項工作中描述的工程BL益生菌可能代表著在應用催化人工酶和代謝益生菌開發抗炎益生菌以減少促炎分子和調節微生物群失調方面向前邁出了一步。Cao, F., Jin, L., Gao, Y. et al. Artificial-enzymes-armed Bifidobacterium longum probiotics for alleviating intestinal inflammation and microbiota dysbiosis. Nat. Nanotechnol. (2023).https://doi.org/10.1038/s41565-023-01346-x