特別說明:本文由學研匯技術中心原創撰寫,旨在分享相關科研知識。因學識有限,難免有所疏漏和錯誤,請讀者批判性閱讀,也懇請大方之家批評指正。現狀
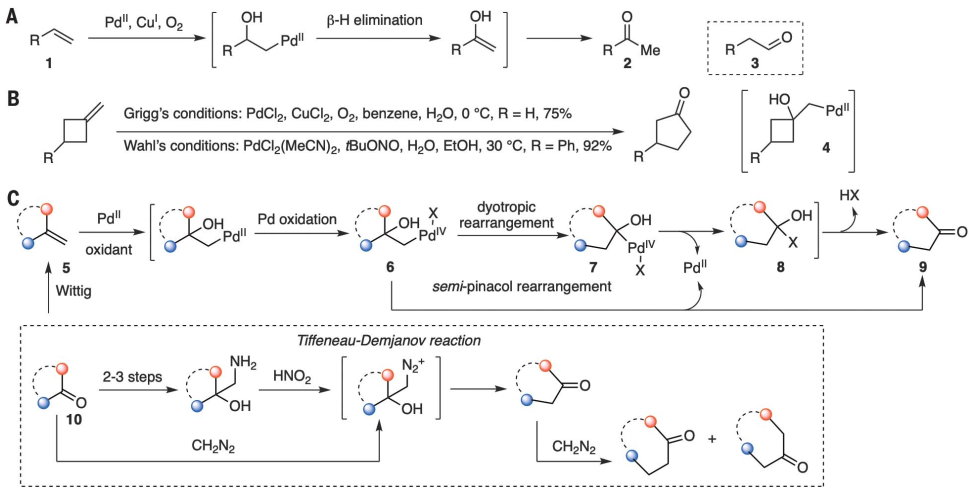
將乙烯轉化為乙醛的Wacker過程是基于過渡金屬催化的最重要的工業過程之一,PdII催化氧化過程廣泛應用于生物活性分子的合成(圖1A)。大量的工作致力于逆轉羥基烯烯化的區域選擇性,并研究了將終端烯烴轉化為醛的條件。然而,該反應通常提供兩種區域異構酮的混合物,除非相鄰的螯合基團可以指導羥酰化過程。Grigg等報道了亞甲基環丁烷在典型的Wacker條件下轉化為環戊酮(圖1B),但也描述了亞甲基環丁烷向環戊酮的環膨脹,且底物范圍非常有限。
啟發新思路
羰基在生物活性天然產物中的普遍存在及其合成的多功能性,開發一種允許將1,1-二取代烯烴轉化為重新排列的酮的通用方法將具有廣泛的用途。鑒于此,洛桑聯邦理工學院祝介平教授等報告了一種不使用不穩定和危險試劑,將多種功能化的末端烯烴轉化為重排的酮和將亞甲基環烷烴轉化為環擴張的環烷烴的方法,包括大環烷烴的實現。從Wacker條件下的PdII/0催化循環轉移到PdII/IV化學,利用向性重排的工作原理(圖1C),按照Markovnikov規則對烯烴5進行羥基化反應,可得到相當穩定的新戊基σ-PdII配合物,在適當的氧化劑存在下,該配合物可原位氧化為PdIV物種。論文以《Oxidative rearrangement of 1,1-disubstituted alkenes to ketones》題發表在Science上。

反應的發展
使用7-亞甲基三氯乙烯(11a)作為測試底物,通過系統地改變Pd(II)源、氧化劑、溫度、溶劑和配體來考察條件。在室溫條件下,在MeCN/H2O (v/v=4:1)中,選擇1-chloromethyl-4-fluoro-1,4-diazoniabicyclo[2.2.2]octane bis(tetrafluoroborate)和Pd(MeCN)4(BF4)2催化可使12a重排酮的產率達到75%。其他氟基氧化劑則效率很低,最多只能提供不到10%的產率。2-己辛烷-1,2-二醇和2-己基-2-羥基-三氟乙酸辛酯的分離清楚地表明反離子(X)在決定PdIV物種反應途徑中的重要作用(圖1C)。其他PdII鹽,如Pd(OAc)2, Pd(OCOCF3)2和PdCl2比Pd(MeCN)4(BF4)2催化效率低。
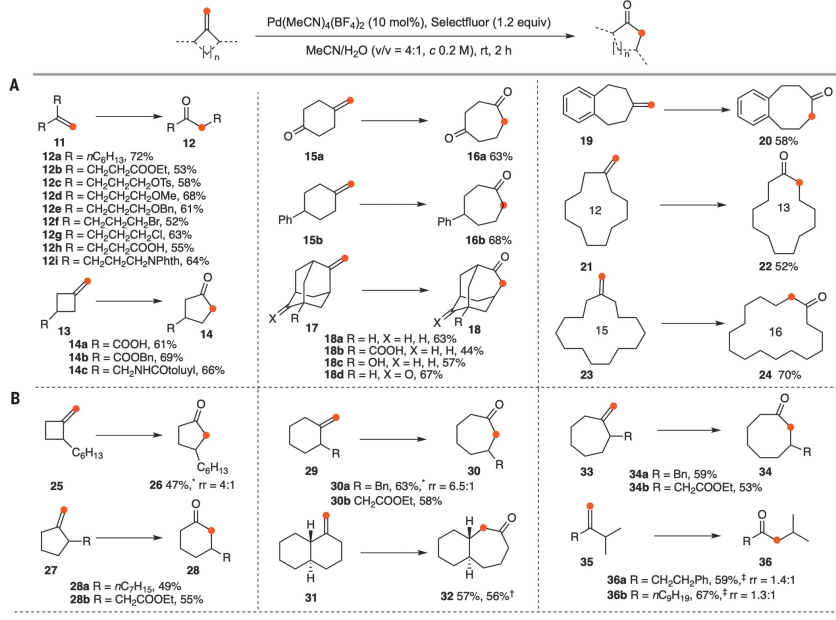
反應范圍
確定了最佳條件后,考察了具有不同官能團的對稱1,1-二取代烯烴以測試反應范圍(圖2A),發現產率良好。除了應變的亞甲基環丁烷(13a-13c)的單碳環膨脹,如預期的那樣得到了環戊酮14a-c,功能化的亞甲基環己烷(15a-b)的環膨脹同樣進行得很好,得到了七元環庚酮16a-b。進一步研究了不對稱1,1-二取代烯烴(圖2B)。2-取代環烷烴-1-酮通常通過Tiffeneau-Damjanov反應和重氮甲烷加成法低選擇性地轉化為兩個環放大酮的混合物,而線性不對稱的末端烯烴以低選擇性氧化重排為酮。線性不對稱末端烯烴的低區域選擇性促使研究常見有機官能團的定向效應。羧酸易于獲取和轉化,被認為是一個理想的候選人。當4-甲基戊烯-4-烯酸(37a)在標準條件下反應時,主要產物是羧基乙基遷移產生的5-氧己酸(38a, 72%)。在羧酸中引入取代基α提高了區域選擇性(38b-c): 38c的分離率為90%。同樣,環戊烷羧酸、環己烷羧酸和N-Ts哌啶-3-羧酸衍生物(39a-c)被重排成相應的δ-氧羧酸(40a-c),產率和區域選擇性都很好。當C sp2的兩個取代基都是仲烷基時,具有羧酸功能的取代基再次表現出更高的遷移能力,分別導致42和44的產率和選擇性都很好。苯乙烯衍生物47a-b轉化為兩個區域異構酮48a-b的混合物,由于苯基本質上具有較高的遷移能力,因此具有較低的選擇性。而苯乙烯衍生物49a-b則完全由于2-羧基苯基的優先遷移而轉化為50a-b。苯基的高遷移性和羧基的定向作用在這種情況下協同作用,表明精選氟在普遍性方面仍然是一種優越的氧化劑。此外,在只有1.0 mol %的Pd(MeCN)4(BF4)2的存在下,以6 mmol規模進行39a的反應,可得到40a,收率89%,表明了該方案的實用性。
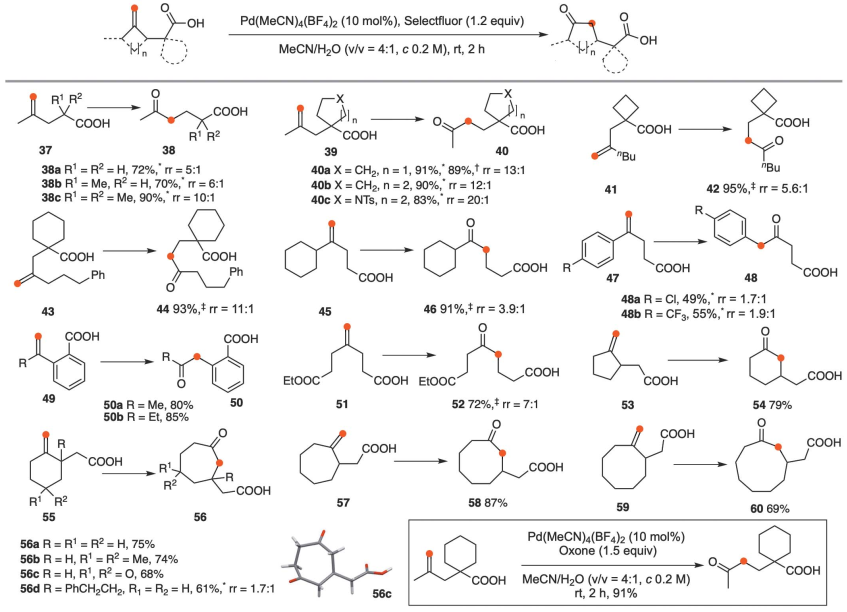
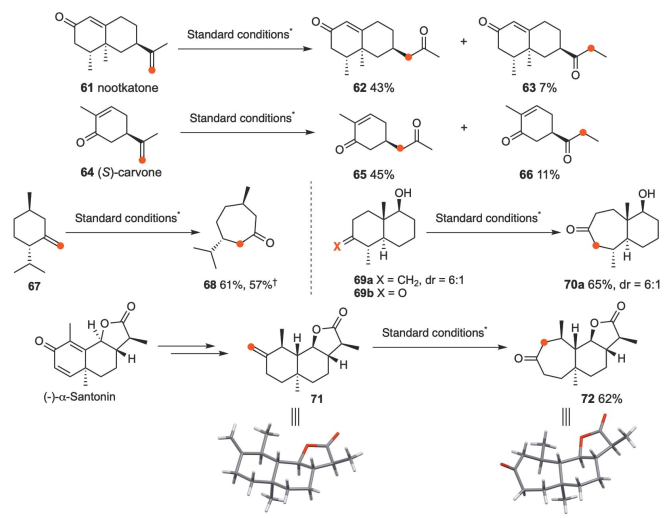
在標準條件下,諾卡酮(61)轉化為62(43%)和63(7%)兩個異構酮,(S)-香芹酮(64)轉化為65(45%)和66(11%)(圖4)。由L-menthone衍生的67和雙環化合物69a分別產生68(61%)和70a(65%),這是由于叔烷基的選擇性遷移。使用重氮甲烷法,酮69b中的羥基必須被保護以避免分解,并且在各種條件下形成了兩個重排酮的混合物。最后,對α-三冬素衍生物71進行區域選擇性環擴大,得到72,產率62%。從71和72結構可以看出,烷基基團在保持其絕對構型的同時發生了移位,說明了一個協同遷移過程。
機理研究
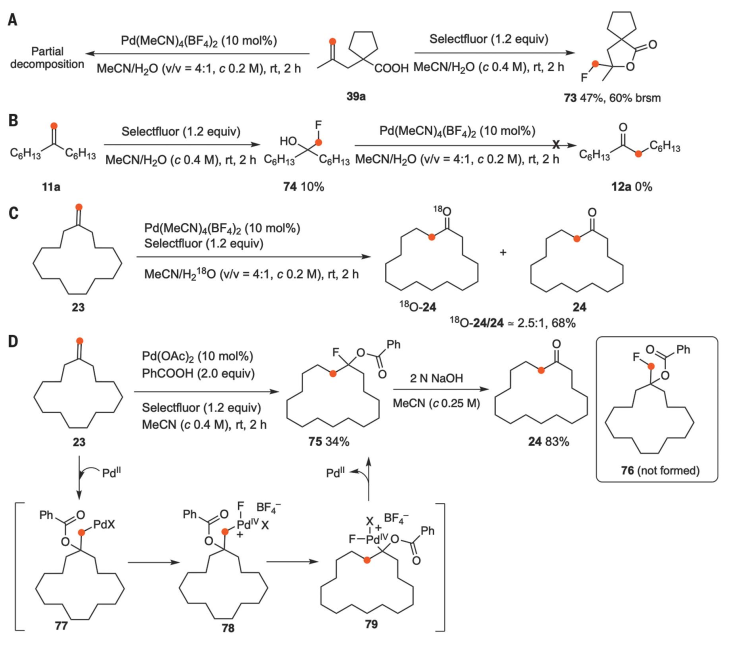
進行了對照實驗為深入了解反應機理。在沒有Selectfluor的情況下,在其他標準條件下,化合物39a被部分分解,而沒有形成重新排列的酮40a。另一方面,在室溫下,在沒有Pd鹽的情況下,用Selectfluor攪拌39a的MeCN/H2O溶液,可得到產率為47%的氟代化產物73(圖5A)。7-(氟甲基)三叉戟-7-醇(74)是通過選擇性氟介導的烯烴11a的分子間羥基氟化反應制備的,未能得到重排的酮(圖5B)。結果表明:選擇氟和PdII鹽都需要進行本反應,氟化醇74不是重新排列的酮12a的中間產物。NMR譜表明Selectfluor與Pd(MeCN)4(BF4)2在室溫下不發生反應,表明PdIV物種是在烷基alkylPdII中間體生成后形成的。用18O標記的H2O (97% 18O)取代H2O,亞甲基環十五烷以68%的收率轉化為環十六烷,表明水是氧氣的來源(圖5C)。最后,在催化量Pd(OAc)2的存在下,攪拌23,苯甲酸和Selectfluor的乙腈溶液,得到環膨脹產物75(收率34%),皂化后轉化為24。在這些條件下,未觀察到由烯烴氟化反應產生的化合物76。表明,在1,1-二取代烯烴氧化轉化為重排酮的過程中,向力重排可能是一個可能的反應途徑。
小結
研究開發了PdII催化的1,1-二取代烯烴氧化轉化為重排酮。該反應既適用于線型末端烯烴,也適用于亞甲基環烷烴,與烷基鹵代烴、芳基鹵代烴、烷基tosylate、羥基、羧酸、酯、內酯、酰胺、酮、α,β-不飽和酮等多種官能團兼容,為產品提供進一步的化學轉化。https://www.science.org/doi/10.1126/science.adg3182Qiang Feng et al. Oxidative rearrangement of 1,1-disubstituted alkenesto ketones.Science, 379: 1363-1368.DOI:10.1126/science.adg3182












