長期以來,由于治療劑向骨髓的遞送效率低下,骨疾病(如骨癌癥、骨髓炎、骨質疏松癥和骨關節(jié)炎)的治療受到限制。盡管增加治療劑量可以提高骨髓中的藥物濃度,但這會導致更大的不良脫靶效應。為了解決這一困境,研究人員制定了幾種策略。例如,一項研究發(fā)現(xiàn),尺寸小于~170nm的納米顆粒可以在骨髓中積聚,因為骨髓內皮細胞之間的細胞間隙很窄(~170nm)。使用150nm納米顆粒作為載體實現(xiàn)了紫杉醇向骨髓的改進遞送。其他人已經(jīng)表明,在納米顆粒上修飾骨靶向模式,如二磷酸鹽、適體和肽,可以改善骨髓輸送。盡管這些策略是令人鼓舞的,但用于疾病治療的骨髓中的高藥物積累仍然是微不足道的,因為骨骼中的低血液灌注以及顯著阻礙當前遞送系統(tǒng)滲透性的骨髓屏障。
由于主動靶向遞送優(yōu)于被動積累策略的潛力,使用活細胞作為載體來改善靶向治療遞送有望克服上述挑戰(zhàn)。攜帶治療劑的細胞通常被認為是“自我”的,往往不會被身體迅速清除,這會延長循環(huán)時間并增加對靶組織的治療遞送。某些細胞傾向于向其來源的組織或微環(huán)境遷移,并且一些細胞可以在感測到生物信號后遷移到特定的生理或病理微環(huán)境。由這些細胞遞送的治療藥物可以與載體細胞共同遷移,并實現(xiàn)位點特異性遞送。到目前為止,許多靶向腦、肺和腫瘤的基于細胞的藥物遞送平臺都是利用幾種嗜組織細胞類型設計的。然而,由于缺乏骨髓特異性遞送機制,使用細胞作為載體將治療劑遞送到骨髓是具有挑戰(zhàn)性的。
人類成年人每天產生1000億個中性粒細胞(NE),這些細胞的壽命很短,約為5.4天。隨著中性粒細胞的衰老,它們表達高水平的CXCR4,這是一種促進細胞遷移到骨髓進行細胞凋亡的蛋白質。
受此啟發(fā),浙江大學游劍、羅利華、李青坡等人通過搭便車的方式設計了一種骨髓靶向納米顆粒藥物遞送系統(tǒng)。成果發(fā)表在Nature Nanotechnology上。
如下圖所示,包封熒光染料DiR(DiR-NP)的聚乳酸-乙醇酸納米顆粒被老化的NE吞噬,以獲得DiR-NPs@NEs。研究人員觀察到,與用游離納米顆粒治療相比,在接受靜脈注射DiR-NPs@NEs后,小鼠骨髓中的DiR-NP水平增加了約7倍。此外,當遞送化療藥物卡巴他賽(CTX)時,CTX-NPs@NEs與CTX-NPs治療相比,CTX-NPs@NEs治療導致骨髓藥物濃度增加5至20倍。這些結果表明,納米粒子可以通過搭便車老化NE主動進入骨髓,并增加骨髓中的藥物積累。
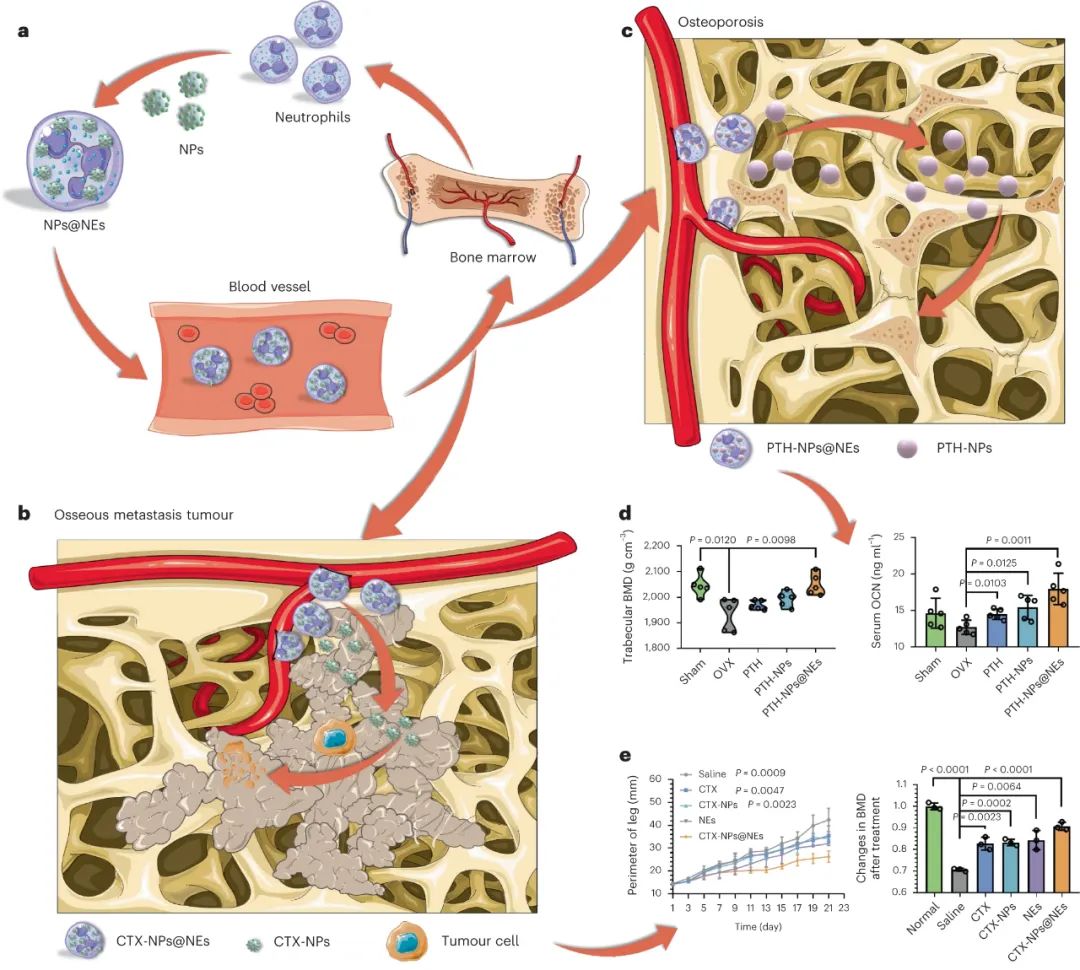
圖|基于中性粒細胞的骨髓靶向藥物遞送系統(tǒng)主動地將藥物遞送到骨髓中
研究人員隨后構建了小鼠骨轉移腫瘤模型,并測試了老化NE對CTX PLGA NPs的骨髓特異性遞送是否可以改善骨轉移性4T1乳腺癌的治療。他們發(fā)現(xiàn)CTX-NPs@NEs與CTX,CTX-NP和NE處理相比,顯著抑制骨腫瘤生長。在CTX,CTX-NP和NE治療組中觀察到腫瘤細胞進一步轉移至肺和隨后的肺損傷相關呼吸困難。然而,在接受治療的小鼠中CTX-NPs@NEs,未檢測到呼吸困難。值得注意的是,CTX-NPs@NEs治療也導致在第21天100%的小鼠存活,而其他組中的大多數(shù)小鼠不存活。
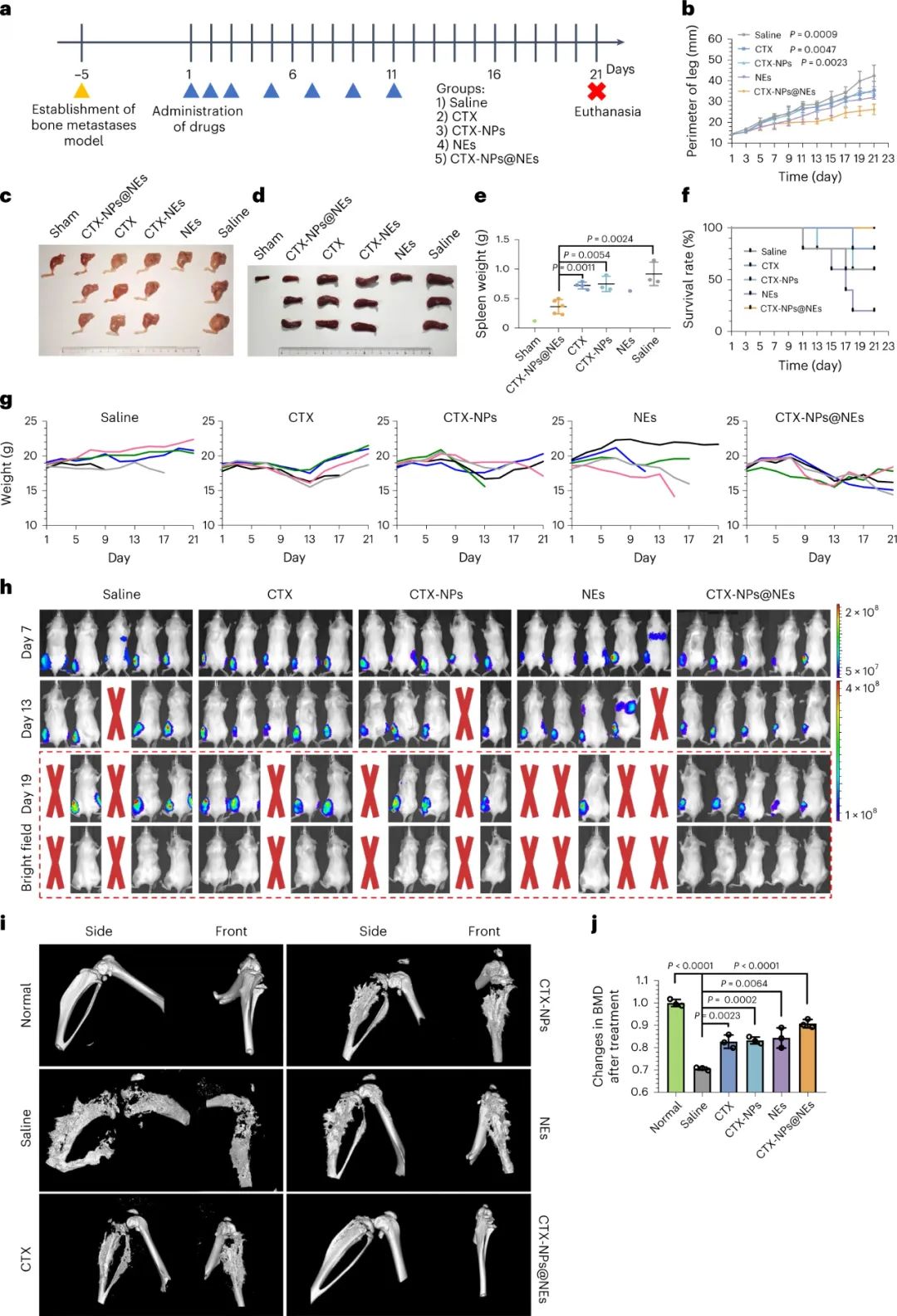
圖|CTX-NPs@NEs在乳腺癌癥骨轉移的抗腫瘤作用研究
除了在腫瘤模型中測試骨髓特異性遞送系統(tǒng)外,還構建了骨質疏松癥小鼠模型,并用于研究NE載有包裹特立帕肽的PLGA納米顆粒(PTH-NPs@NEs)的抗骨質疏松功效。PTH-NPs@NEs治療大大增強了成骨細胞的增殖,同時抑制了破骨細胞的生長。此外PTH-NPs@NEs改善骨小梁密度、骨體積分數(shù)、骨小梁分離,最終在體內治愈骨質疏松癥。鑒于骨癌癥和骨質疏松癥治療面臨的挑戰(zhàn),這項工作展示了一種提高治療效果的潛在方法。
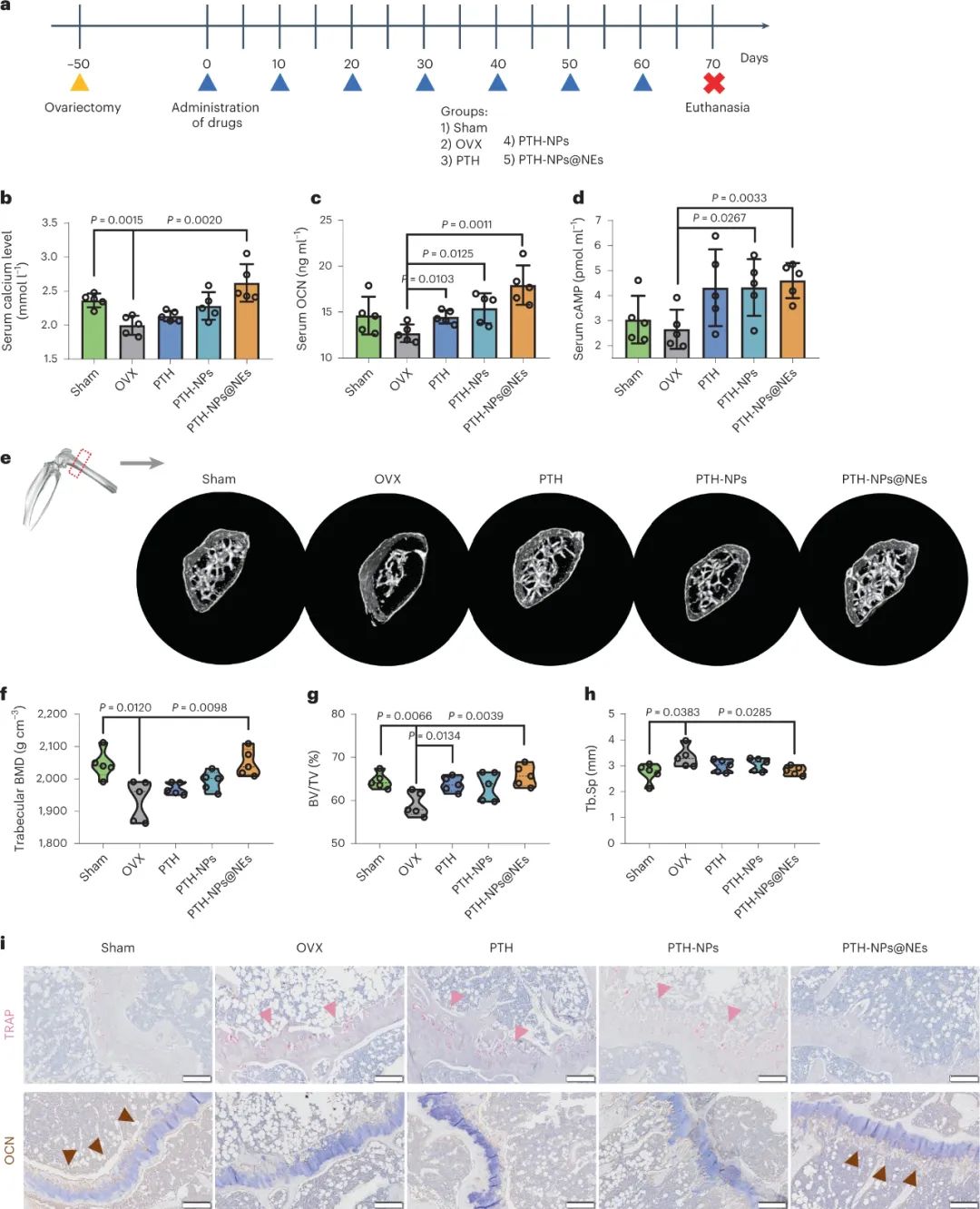
圖|PTH-NPs@NEs對于骨質疏松癥的影響
該研究對骨病治療領域也將引起廣泛關注,因為可以利用老化嗜中性粒細胞將一系列治療性貨物遞送到骨髓微環(huán)境中,而不僅僅是化學治療和抗骨質疏松癥藥物。例如,攜帶在骨腫瘤中累積的放射增敏劑的NE可以潛在地增強抗腫瘤功效,同時降低毒性,而攜帶包封編碼細胞因子或免疫檢查點阻斷的信使RNA(mRNA)的脂質納米顆粒的NE可以誘導用于癌癥免疫療法的腫瘤特異性免疫應答。此外,提供成像模式的NE可以幫助早期診斷各種骨病。
這里描述的搭便車的NEs策略的一個關鍵優(yōu)點是它們可以改善由于骨髓向性運輸而導致的貨物在骨微環(huán)境中的積累。觀察這種基于NE的遞送系統(tǒng)與用活性靶向配體(例如單克隆抗體)修飾或功能化的納米顆粒相比將是有趣的。該策略用于臨床轉化的優(yōu)點包括:i)中性粒細胞由于其在血液中的高濃度而易于獲得;ii)PLGA已獲得FDA批準用于一系列藥物輸送應用。未來的工作應該解決將藥物輸送到骨髓所需的大量老化NE是否會誘導不必要的毒性免疫反應,如細胞因子釋放綜合征,正如許多過繼性T細胞轉移療法中所報道的那樣。
參考文獻:
Luo, Z., Lu, Y., Shi, Y. et al. Neutrophil hitchhiking for drug delivery to the bone marrow. Nat. Nanotechnol. (2023).
https://doi.org/10.1038/s41565-023-01374-7











