特別說明:本文由學研匯技術 中心原創撰寫,旨在分享相關科研知識。因學識有限,難免有所疏漏和錯誤,請讀者批判性閱讀,也懇請大方之家批評指正。研究背景
B-enzocyclobutenes(BCBs)代表了一類重要的剛性四元碳環,存在于天然產物中,在材料科學和機械化學中顯示出作為治療性分子支架、多功能合成子和功能基序的巨大潛力。基于BCB的剛性和三維藥效團導致了伊伐布雷定的發現,伊伐布雷定是FDA批準的用于治療心力衰竭和心臟相關性胸痛的藥物。此外,與構象靈活的母體化合物和苯并環戊烷類似物相比,具有精神活性的2C-B的BCB類似物對受體具有更好的親和力。
關鍵問題
1、尚未實現控制BCBs合成的環加成反應區域選擇性目前,烯烴與苯炔的[2+2]環加成反應是BCBs最常見的合成路線之一。然而,控制該環加成反應的區域選擇性是一個尚未解決的問題。現有的BCB合成方法在范圍和效率方面存在局限性,使用這些反應合成具有藥用價值的雜環BCB具有挑戰性,需要尋找替代的、更具選擇性的途徑來制備富含C(sp3)特性的各種剛性碳環。
新思路
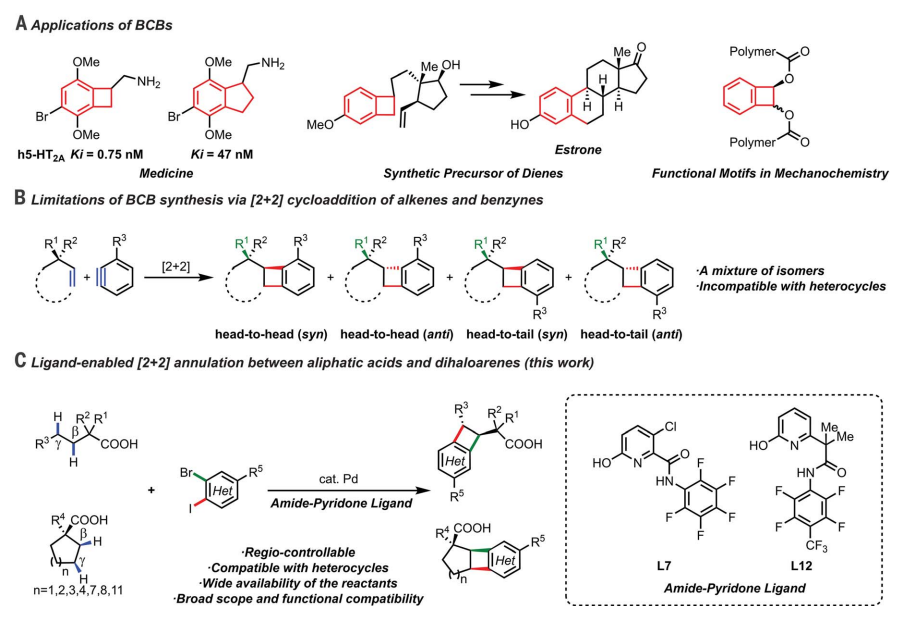
有鑒于此,斯克里普斯研究所Jin-Quan Yu等人報道了一種鈀催化的羧酸中兩個相鄰亞甲基單元的雙C-H活化,在雙齒酰胺-吡啶酮配體的作用下,通過僅涉及(兩個C-H鍵和兩個芳基鹵鍵)的s鍵的形式[2+2]環加成反應,實現了BCBs的區域可控合成。廣泛的環狀和非環狀脂肪酸以及二鹵代雜環芳烴是相容的,產生了多種功能化的BCBs和雜-BCBs,存在于藥物分子和生物活性天然產物中。

受到β,?-C-H氘化的啟發,作者探究了開發與鄰二鹵代芳烴的順序雙重C-H偶聯過程來構建 BCB 支架,通過實驗證實了反應的可行性并提高了分離效率。作者評估了[2+2]環化反應的底物范圍,表明多種環狀脂肪酸可提供順式BCB產品作為單一產品,較大的環狀脂肪酸產生反式 BCB產物作為主要異構體。作者發現六元螯合酰胺-吡啶酮配體是線性底物最有效的配體,提供多種反式 BCB,還展示了許多苯并環丁酸產品的合成加工。作者證明不同位置的取代基與該催化系統相容,氟、氯和溴等鹵素是相容的,能夠以良好的收率提供所需的BCB。作者發現吡咯、噻吩和呋喃等雜環化合物具有良好的耐受性,兩個C-H鍵和兩個芳基鹵化物鍵的順序激活具有出乎意料的排他性區域選擇性。1、成功地實現了Pd催化的BCB合成,實現了專一區域控制作者通過酰胺-吡啶酮配體實現的脂肪酸與二鹵代芳烴的環化反應,成功地實現了Pd催化的BCB合成,其中通過芳基碘和溴之間的差異實現了專一的區域控制。直接使用豐富且結構多樣的非環酸和環酸作為底物,無需預先官能團化,極大地擴展了獲得各種BCB的途徑,包括雜環BCB支架。
技術細節
在對二羧酸的亞甲基C-H內酯化反應的機理研究中,觀察到 7-乙氧基-7-氧代庚酸的β,?-C-H氘化。這一觀察結果促使作者研究是否可以開發與鄰二鹵代芳烴的順序雙重C-H偶聯過程來構建 BCB 支架。使用1a(1-丙基-1-環戊烷羧酸)和2a(二鹵代芳烴偶聯1-溴-4-氯-2-碘苯)以及Ag2CO3作為鹵化物清除劑,用一系列吡啶-吡啶酮配體測試這種轉化的可行性,結果表明所需的3a(BCB)確實形成為單一異構體。吡啶-吡啶酮配體的初步結果表明需要更有效的配體,作者專注于開發支架吡啶臂的替代品,合成了一類同時帶有吡啶酮和缺電子酰胺的雙齒配體全氟苯胺,通過廣泛的結構調整,將配體L7確定為最佳配體,以90%的分離產率提供3a。
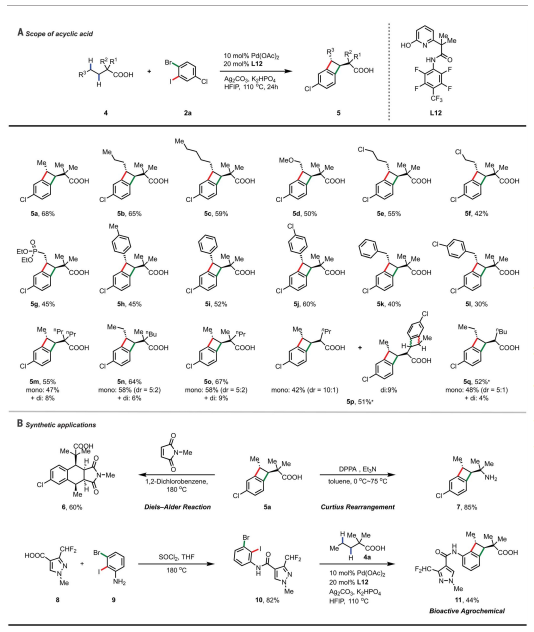
作者評估了[2+2]環化反應的底物范圍。包括五元環(1a-1l)、六元環 (1m-1t)、七元環(1u-1v)和八元環(1w)在內的多種環狀脂肪酸相容,可提供順式BCB產品作為單一產品區域異構體(3a-3w)。較大的環狀脂肪酸產生反式 BCB 產物作為主要異構體。當收率相對較低時,回收剩余的未反應的脂肪酸反應物。配體L7允許將Pd負載量從10降低到5或1%,同時保持二鹵代芳烴2a和酸之間[2+2]環化反應的合成有用收率。

無環脂肪酸4a在L7中僅產生低產率 (2%)。六元螯合酰胺-吡啶酮配體L12 成為這些線性底物最有效的配體,提供多種反式 BCB。甲氧基、氯、膦酸酯和取代的芳基等多種官能團是相容的。作者還展示了許多苯并環丁酸產品的合成加工。在180°C下加熱作為鄰醌二甲烷前體的5a與 N-甲基馬來酰亞胺在二氯苯中的溶液,以60%的收率提供Diels-Alder 加合物。5a可以很容易地轉化為具有重要藥用價值的胺。苯并環丁基酰胺是一種獲得專利的作物保護生物活性分子,可以通過脂肪酸4a和N-二鹵代芳基酰胺的[2+2]環化反應快速合成。
溴碘芳烴的廣泛范圍進一步擴大了BCBs的多樣性。不同位置的取代基與該催化系統相容。氟、氯和溴等鹵素是相容的,能夠以良好的收率提供所需的BCB。還對帶有給電子(12k-12l)和吸電子(12m-12t)基團的芳烴進行了測試,為產品提供了良好的產率。廣泛用于C-H活化的酰胺(12s-12t)和羧酸(12u)基團作為導向基團,也適用于該方案。芳基三氟甲磺酸酯是 Pd 交叉偶聯化學中的高反應性位點,也是可以耐受的(12m)。此外,二溴芳烴和二碘芳烴適用于標準條件,以中等至良好的收率生成所需的 BCB。正如預期的那樣,1b與 2,3-二溴甲苯 (2cBr) 的反應提供了兩種區域異構體的混合物,表明具有兩個不同活性位點的溴碘芳烴對于控制區域選擇性至關重要。
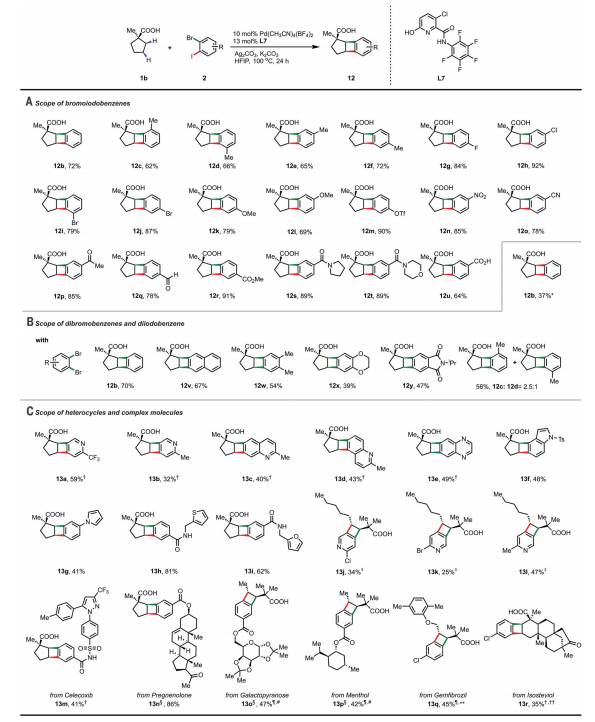
作者發現吡咯、噻吩和呋喃等雜環化合物具有良好的耐受性,能夠以優異的收率提供所需的產品。具有生物活性結構的二鹵芳烴如塞來昔布、孕烯醇酮、半乳糖和薄荷醇也相容。該方案還可以應用于生物活性分子的后期修飾。兩個C-H鍵和兩個芳基鹵化物鍵的順序激活具有出乎意料的排他性區域選擇性。
展望
總之,作者通過鈀催化的羧酸中兩個相鄰亞甲基單元的雙C-H活化,實現了BCBs的區域可控合成。除了實現兩個相鄰亞甲基C-H鍵的區域選擇性功能化之外,具有獨特區域選擇性的多種 BCB 的模塊化合成適用于制藥、材料科學、機械化學以及天然產物合成。反應機理的進一步研究正在進行中。JI-MIN YANG, et al. Regio-controllable [2+2] benzannulation with two adjacent C(sp3)–H bonds. Science, 2023, 380(6645): 639-644.DOI: 10.1126/science.adg5282https://www.science.org/doi/10.1126/science.adg5282










