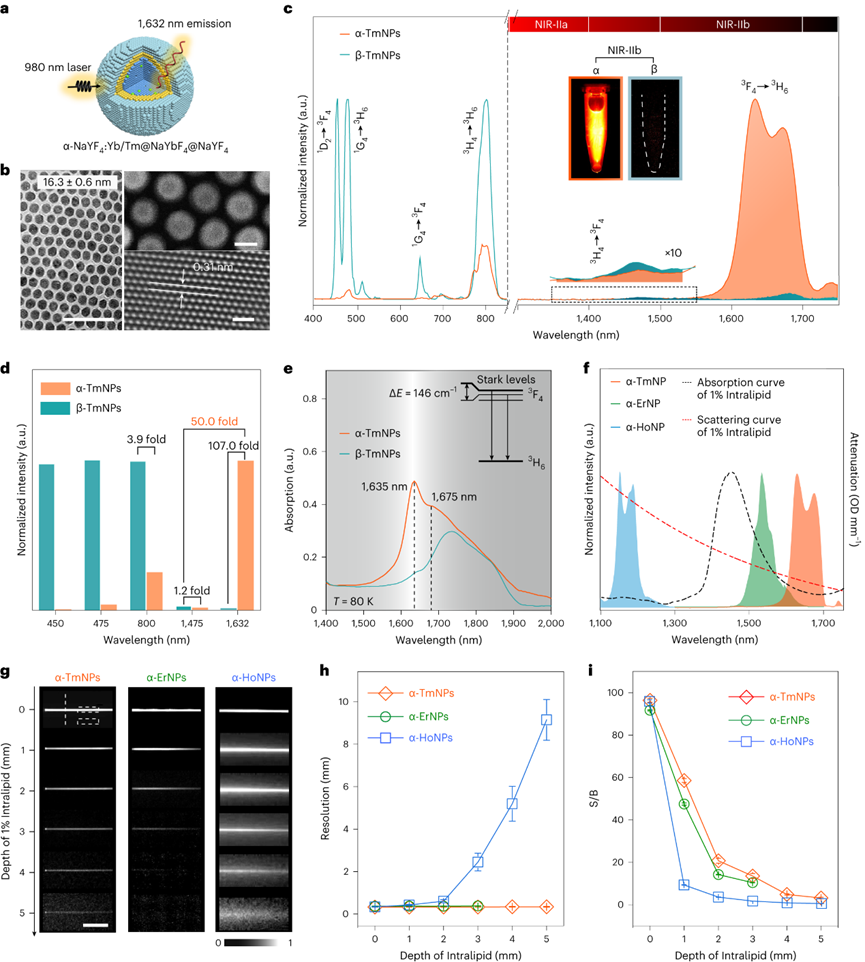
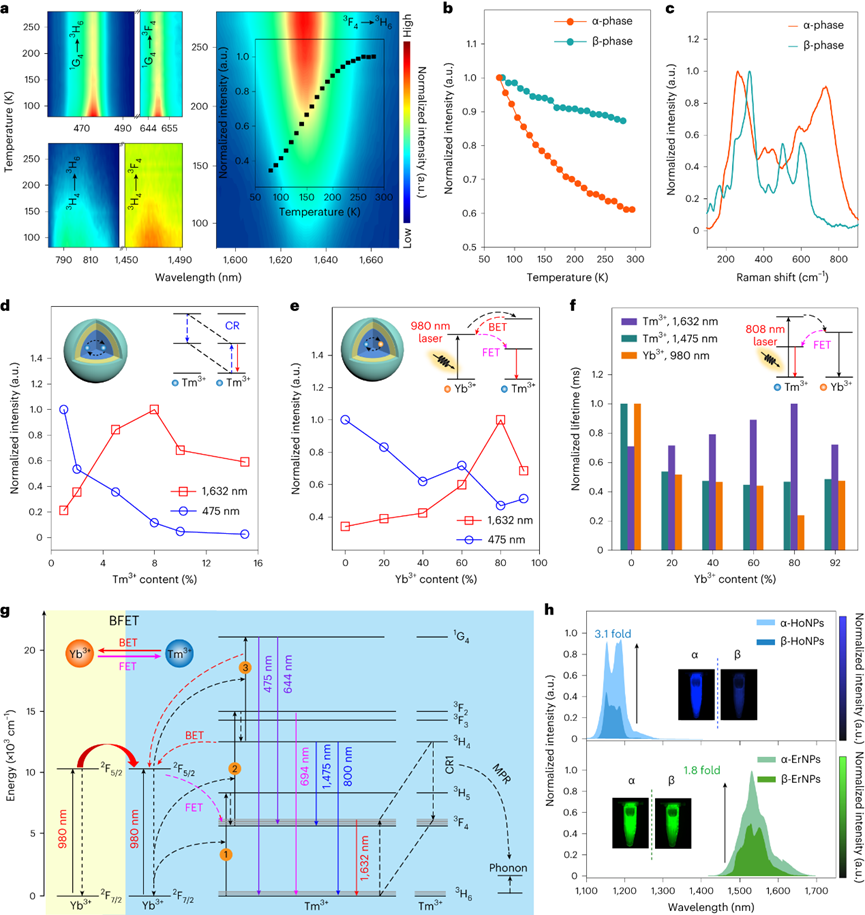
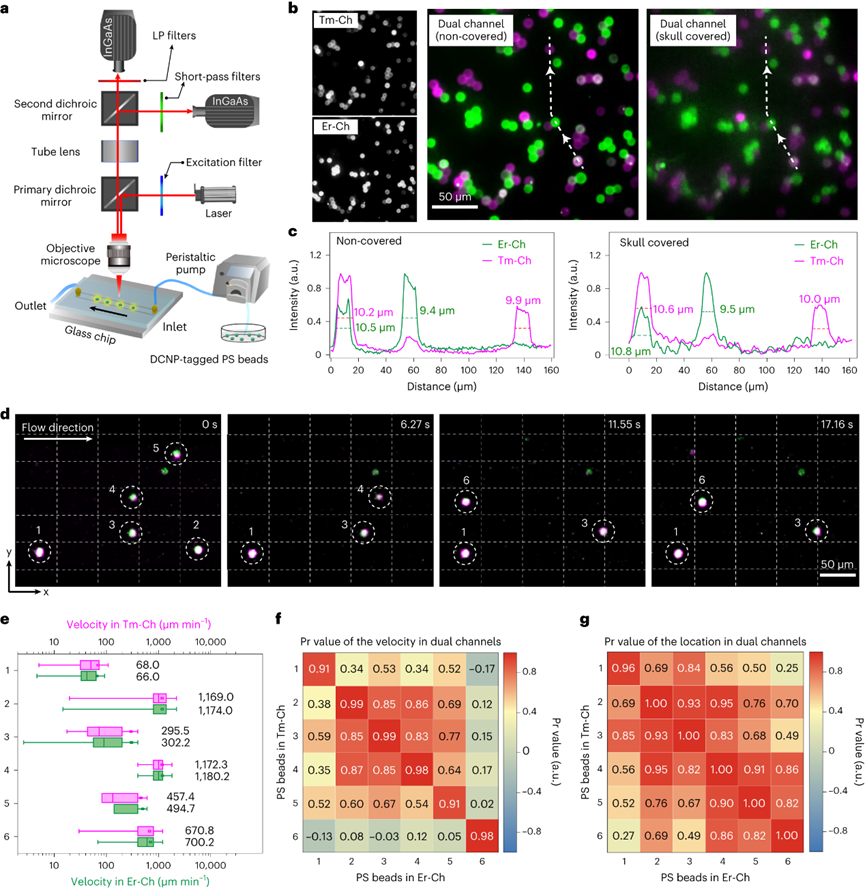
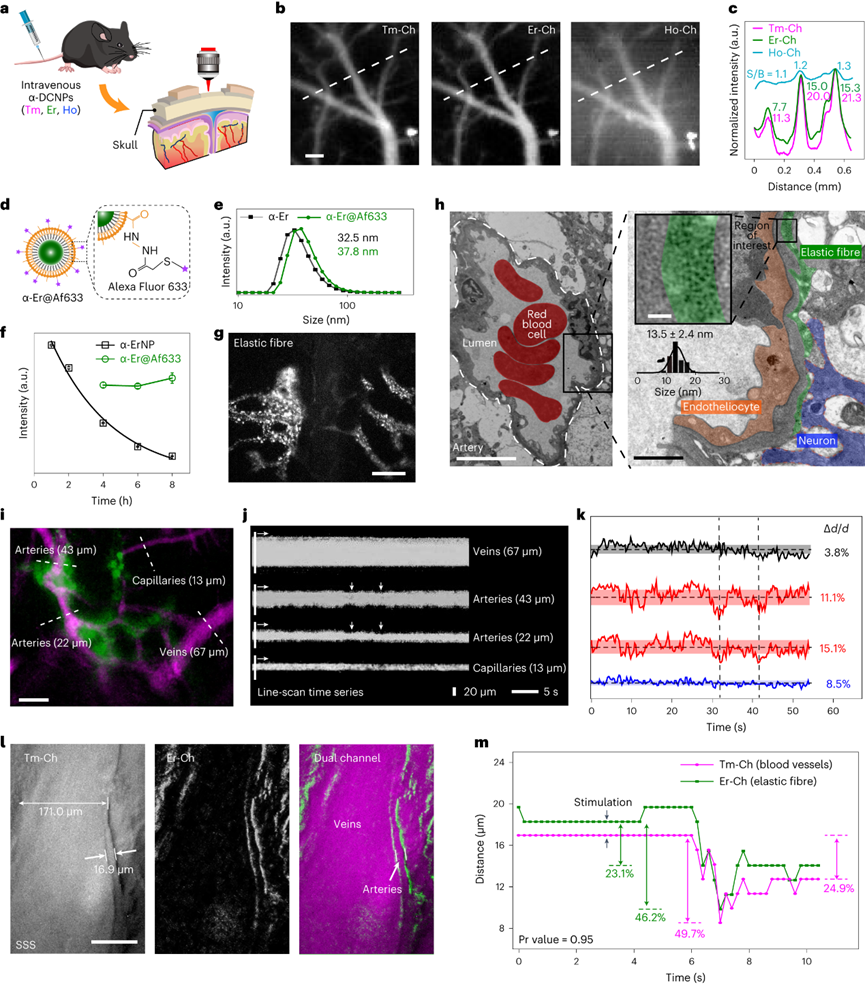
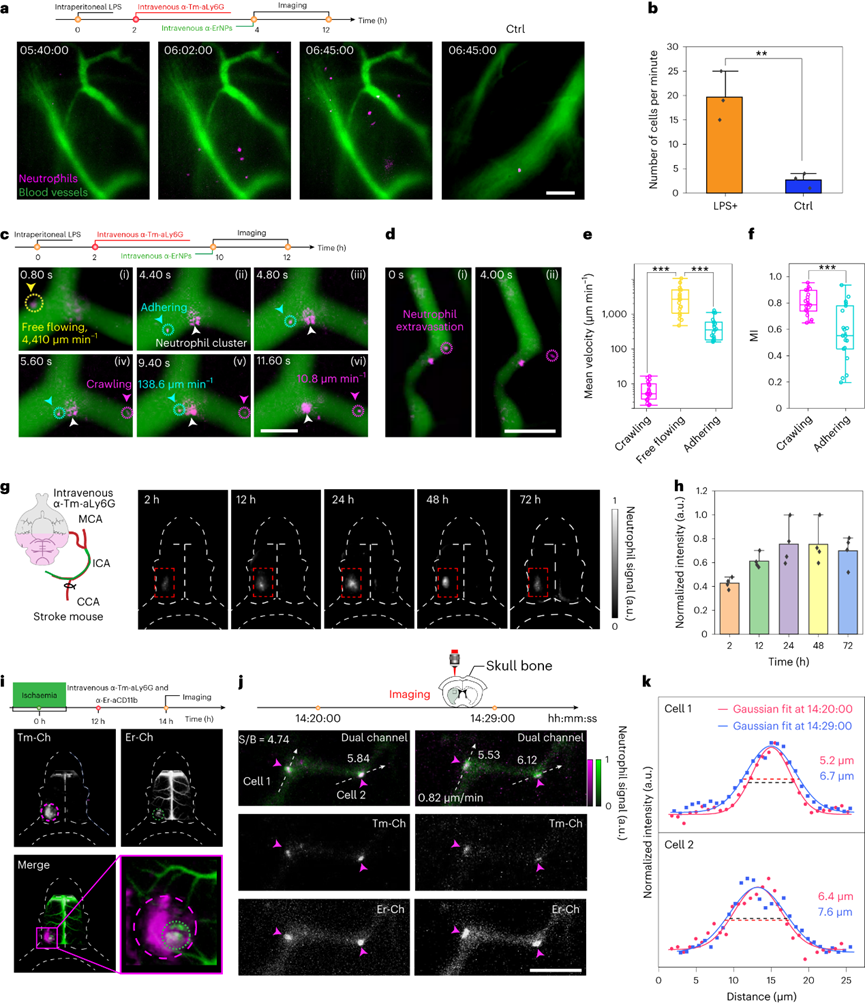
實時動態光學成像以其獨特的高靈敏度和時空分辨率,在生物醫學工程的成像領域引起了廣泛的關注。特別是,實時動態多重成像對于研究由復雜生物相互作用調節的病理生理過程至關重要,包括細胞介導的免疫反應、心血管疾病相關血流動力學和神經元回路的潛在活動。迄今為止,這些研究的實施主要依賴于帶有可見熒光探針。然而與單光子激發相比,由于非線性光學過程多光子激發遭受劇烈的熒光衰減。因此,需要侵入性手術來暴露組織以防止光衰減。最近,第二近紅外(NIR-II)窗口成像由于減少了組織中光子散射和自發熒光,促進了具有更深穿透深度的非侵入性生物成像。目前,NIR-II成像監測的動態過程主要依賴于通過切換濾光片對單個探測器順序獲得的快照進行積分。非侵入性實時動態的可視化血流動力學和多細胞動力學仍然是一個挑戰。為了解決這個問題,在NIR-IIb區(1500-1700nm)發射的明亮熒光探針是必不可少的,因為該區域提供了光子散射和組織自發熒光的最佳平衡。鑭系元素下轉化納米顆粒(DSNP)是實現此目的的理想候選探針,因為它們的NIR-II波長可調諧,發射帶寬窄,吸收和發射之間的光譜分離大。近日,復旦大學張凡教授率領其團隊報道了一項適用于深層組織的非侵入性體內實時動態多重成像平臺。張凡團隊專注于近紅外光學探針設計與合成,生物醫學成像和光學成像儀器設計的研究領域。他們開發了新的NIR成像探針庫,并利用這些探針促進生物醫學和臨床應用的進步。此次,張凡團隊開發了一種立方相銩基納米顆粒(α-TmNPs),可以實現近紅外Ⅱb區的熒光放大。同時,可以利用參雜其他稀土元素實現對發射光譜的調整。作者團隊進一步開發了摻鉺的α-ErNPs,與α-TmNPs構成了高同步性與準確性的雙通道成像系統,實現了對于小鼠腦卒中模型中血管相關活動的無創實時動態成像。作者團隊報道了一種在1632nm處發射熒光的銩基立方相納米顆粒(DSNP),呈現Yb0.8/Tm0.08@NaYbF4@NaYF4(α-TmNPs)的多層核殼結構。透射電子顯微鏡(TEM)圖像顯示呈現均勻球形,粒徑~16nm。在α-TmNPs中,Tm3+從Yb3+中提取激發能,在1632nm處產生增強的熒光納米,比傳統的六方相銩基納米顆粒(β-TmNPs)在1475nm的熒光亮約50倍。但是α-TmNPs的上轉換發光效率明顯降低,只有約為14.0%。低溫吸收光譜證實1632?nm熒光源自3F4晶體的斯塔克效應,這是能級分裂的結果。1632nm處的發射強度與激發功率呈非線性關系,這可能涉及了多光子躍遷過程,對應3F4?→?3H6。到目前為止,基于Er的DSNP在1530nm處發射熒光已經被報道用于深層組織生物成像,由于與吸水帶的部分光譜重疊導致其易熒光猝滅。而1632nm發射峰與吸水曲線重合小。α-TmNPs、α-ErNPs與α-HoNPs比較在仿生體液中的性能,由于長波長下水吸收較小,散射效應最小,α-TmNPs顯示出最好高的分辨率和信底比。此外,α-TmNPs和α-ErNPs在NIR-IIb區域的光學性能優于具有較短NIR-II發射的α-HoNPs,這表明它們在體內NIR-IIb多重成像的潛在應用前景。接下來探索1632?nm熒光放大機制。除了晶體場效應外,還觀察到多聲子輔助的非輻射弛豫(MPR)效應。α-TmNPs在80–290k范圍內呈現的溫度依賴性發光,說明從3H4和1G4能級躍遷強度降低而3F4能級增強。相反的趨勢歸因于隨著溫度的升高,非輻射的3H4?→?3F4轉換加速。α-TmNPs在1475nm處的熒光衰減超過β-TmNPs說明更多的能量通過非輻射路徑耗竭。考慮到發射極含量可能對發光躍遷產生重要影響,接下來關注Tm3+之間的交叉弛豫現象。1632nm發射光持續增強直到Tm3+含量達到~8mmol%,而475nm的發光轉變隨Tm3+含量增加而衰減,并且1475nm發射強度在Tm3+含量5?mmol%時最強,表明Tm3+–Tm3+交叉弛豫通過3H4?+?3H6?→?3F4?+?3F4顯著促進3F4數目。根據能隙定律,這種交叉弛豫過程的能量失配可以被立方相中的高能聲子效地橋接,這有助于1632nm的熒光放大。核心中Yb3+含量的升高通過Yb3+介導的向后-向前能量轉移(BFET)進一步增強了1632nm發射熒光。除了作為敏化劑吸收980nm光子將激發能轉移到Tm3+,Yb3+(80?mmol%)通過反向能量轉移(BET)捕獲來自Tm3+(3H4)的能量,然后通過正向能量轉移(FET)激發Tm3+(3F4)。此外,MPR和BFET效應也被驗證用于增強Ho3+和Er3+摻雜的納米顆粒的降頻熒光。這里觀察到優化的α-HoNPs(NaYbF4:Ho0.2@NaYbF4@NaYF4)和α-ErNPs(NaYbF4:Er0.1@NaYbF4@NaYF4)與其β相對應物的比較顯著增強了熒光強度,表明該策略的普適性。對于實時動態多重成像來說,多通道在時間和空間上同步的信號捕獲是必不可少的。為此,構建了一個帶有兩個InGaAs相機的雙通道NIR-IIb熒光成像系統,該系統允許以每秒110幀的最大速度進行動態成像。在存在高散射小鼠頭骨或皮膚的情況下,兩個NIR-IIb通道顯示出相當的空間分辨率和單色性,Tm通道(表示為Tm-Ch)和Er通道(表示為Er-Ch)中的珠粒直徑幾乎不變,證明了具有高空間分辨率的深層組織多重成像的可行性。進一步采用微流控系統來驗證成像系統的實時動態多路成像能力。將Tm/Er標記的聚苯乙烯(PS)珠粒分散在十六烷中,然后以25ml/h的流速泵入流動通道,在20秒內隨機跟蹤六顆珠子的運動。定量結果顯示珠子的平均速度Er Ch中為66.0–1180.4 μm/min,而Tm Ch中為68.0–1172.3?μm/min,顯示兩個成像通道之間的微小標準偏差。使腦血流動力學的無創熒光成像無需創建顱骨窗口,對于腦血管疾病的準確檢測意義極大。與NIR-IIa區相比,NIR-IIb區在血管成像中顯示出顯著優勢,如Tm Ch(11.3–21.3)和Er Ch(7.7–15.3)的信噪比比Ho Ch(1.1–1.3)高約7–16倍。得益于NIR-IIb成像在深層組織中的優勢,Alexa Fluor 633偶聯的α-ErNPs(α-Er@Af633)和α-TmNPs可以分別選擇性地突出腦動脈和腦血管上的彈性纖維。注射后4?h后,上矢狀竇(SSS)附近的動脈壁清晰可見,其中信號在8?h內保持穩定,持續時間超過24?h。TEM圖像顯示α-Er@Af633(~13?nm),進一步表明納米顆粒從血管腔滲出并標記動脈壁。多重成像顯示了不同水平的腦血管,包括通過彈性纖維標記和血管直徑識別。在約50s的時間過程中監測麻醉小鼠大腦血管的自發直徑變化。進一步應用去甲腎上腺素刺激來模擬神經血管耦合效應。靜脈注射去甲腎上腺素后,在Er-Ch和Tm-Ch中都觀察到收縮幅度大于20%的動脈收縮,而在不使用藥物時,它維持穩定。相關分析表明用于捕獲自發血管收縮時表現出高時空同步。中性粒細胞被認為是急性炎癥的第一反應者。評估中性粒細胞的體內實時動態成像,將Ly6G抗體標記的α-TmNPs(α-Tm-aLy6G)注射到患有皮下耳部炎癥的小鼠中。10h的實時多重傳輸圖像顯示血管中中性粒細胞自由流動(~4410?μm/min),表明它們處于未刺激和靜息狀態。此外,定向遷移至單個粘附中性粒細胞的小中性粒細胞簇具有高彎曲系數,表明炎癥微環境中的中性粒細胞趨化性。此外,還觀察到中性粒細胞的定向爬行和中性粒細胞外滲。進一步對腦卒中小鼠的單細胞免疫反應進行了動態監測。隨著時間的推移,在大腦一側觀察到NIR IIb信號增加,表明左大腦半球受損,這也與偏癱的行為癥狀一致。中性粒細胞活化與組織浸潤高度相關,組織浸潤會導致炎癥反應并加重缺血性中風。為了特異性追蹤活化的中性粒細胞,對Ly6G和CD11b進行了雙重分子靶向。在從血液循環中去除納米探針后,確定了損傷大腦中的中性粒細胞分布。Tm-Ch和Er-Ch熒光信號的共同定位以及電感耦合等離子體質譜測量證實了中性粒細胞特異性靶向。接下來,應用雙通道實時成像系統來研究通過完整頭骨示蹤激活的中性粒細胞。中性粒細胞的NIR IIb信號具有高達6.12的信噪比。特別是Er-Ch中的強信號表明活化的中性粒細胞表達CD11b整合素。實時圖像顯示活化的中性粒細胞以0.82μm/min的速度微弱地滾動和爬行?,表明它們在內皮表面牢固粘附。此外,雙色映射的中性粒細胞似乎沿著血流的剪切力被拉長,這通常被認為是中性粒細胞通過發炎血管外滲的最后一步。由于缺乏理想的NIR-IIb區中可用的熒光探針和成像技術,深層組織中的無創實時動態多重成像仍然是一個持續的挑戰。開發出1632nm處熒光放大的立方相TmNP,通過調節3H4 → 3F4非輻射躍遷和BFET過程,豐富了“組織最透明”的NIR-IIb區域中可用DSNP。鑒于鑭系離子豐富和梯狀的能級,基于已建立的機制,預計將發現更多潛在的NIR-II發射帶。DSNP固有的窄發射帶,加上自制的雙通道NIR-IIb熒光成像系統,實現了Tm和Er通道時空同步的實時動態多重成像。通過顱骨實時動態多重監測腦血管舒縮和中性粒細胞動力學,揭示了該技術在非侵入性血流動力學和單細胞水平免疫反應研究中的潛力。盡管已經實現了體內實時動態多重成像,但可以進一步采用NIR-IIb更高效的成像檢測,納米探針的亮度也仍需提高。有了靈敏的檢測器和更明亮的DSNP,體內免疫細胞的非侵入性多重時空圖譜可以進一步擴展,以增加細胞類型或標志物的數量,特別是用于在免疫復雜環境中進行研究,并實現合理的細胞治療。Yiwei Yang, Ying Chen, Peng Pei, et al. Fluorescence-amplified nanocrystals in the second near-infrared window for in vivo real-time dynamic multiplexed imaging. Nat Nanotechnol. 2023 Jun 22.https://www.nature.com/articles/s41565-023-01422-2