特別說明:本文由學研匯技術中心原創撰寫,旨在分享相關科研知識。因學識有限,難免有所疏漏和錯誤,請讀者批判性閱讀,也懇請大方之家批評指正。現存問題
水可以通過一系列化學過程轉化為有價值的H2,這使得它可以作為一種潛在的轉移加氫試劑用于還原不飽和化合物。然而,水活化的主要挑戰來自兩個特征(圖1a):1)水的去質子化(pKa=15.74)在合適的堿基下很容易實現,但由于O-H鍵的高鍵解離能(118 kcal mol-1),H2O具有較高的熱力學穩定性,因此均解具有挑戰性;2)如果產生羥基自由基,不能提供第二個氫原子,因為這將導致一個高能氧原子。目前的水活化方法遵循三種不同的策略: 氧化加成活化,金屬-配體協同活化和配位誘導的鍵減弱(圖1b)。前兩種方法主要集中在d塊過渡金屬的使用上,而處理主族元素的轉換仍然非常罕見。由于H2O加合物的形成也增加了酸度,大多數這樣的H2O配合物作為質子供體反應。釤(II)、鈦(III)、硼和鉍(II)等化合物可以實現O-H鍵的均裂。這些活性水配合物已被證明可以減少活性自由基,生成閉殼產物,其中氫原子轉移(HAT)在熱力學上是有利的(圖1c)。相比之下,從H2O-中間體到封閉殼π體系的分子間HAT導致反應性H加合物C自由基的例子,特別是考慮到不含金屬的H2O加合物中間體,仍然是可取的。考慮到過渡金屬的變體,有幾個挑戰需要克服。目前已知的能夠作為HAT試劑的水加合物是相對穩定的,因此氫轉移到π體系導致反應性C自由基是自耗的。此外,基于H2O的H供體應該很容易生成,具有足夠的反應性,以參與熱力學上有利的HAT-π體系,但同時必須具有足夠的壽命,這使得試劑設計具有很高的挑戰性。已經報道了一些金屬自由基H原子轉移實現閉殼π體系氫化的例子。然而,由于這些給氫體本身是穩定的閉殼化合物,反歧化反應中的分子間HAT是強吸熱的,動力學上不受歡迎。因此,這些過程的范圍非常狹窄,只發生在300°C以上的溫度下。
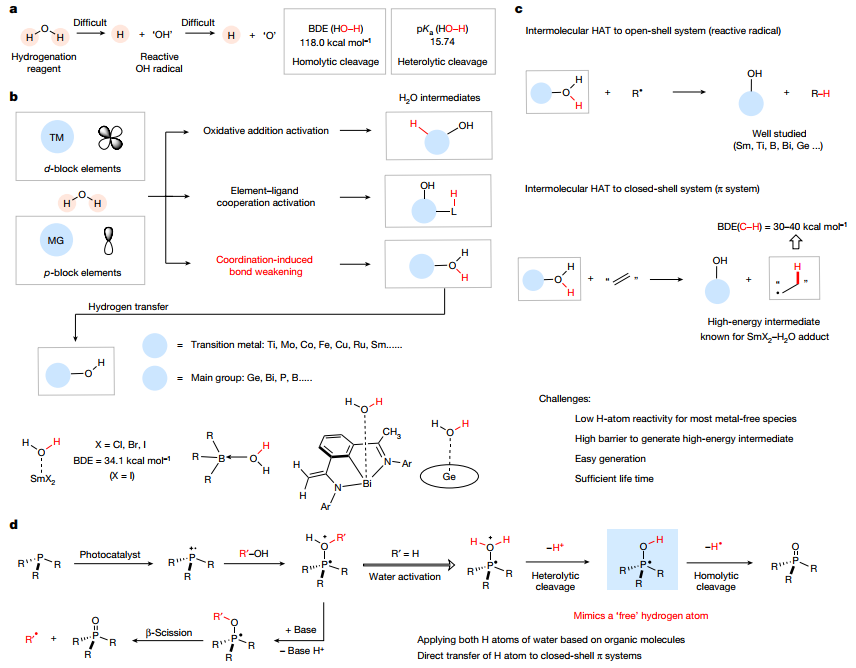
圖1:背景與概念
解決思路
基于此,德國威斯特伐利亞大學Armido Studer團隊考慮到磷化氫自由基陽離子在光氧化還原催化中可以作為可調介質,通過脫氧生成碳中心和雜原子中心的自由基(圖1d),設計了一種通過磷化氫自由基陽離子的單占據分子軌道與水相互作用,利用光氧化還原催化進行水活化的方法。PR3-H2O自由基陽離子可以去質子化,在O-H鍵異裂中產生PR3-OH自由基中間體。磷氧化物中P=O鍵的強鍵解離能為第二個O-H鍵的均裂提供了高的熱力學驅動力,使PR3-OH中間體表現得像一個“自由”的氫原子,為探索氫原子自由基化學提供了機會。論文以《Photocatalytic phosphine-mediated water activation for radical hydrogenation》題發表在Nature上。

反應設計及機理分析
為了實驗驗證PR3-OH中間體的反應設計和H原子反應性,首先研究了三苯基膦(PPh3)介導的析氫反應。在5 W藍色發光二極管(LED)照射下,在乙腈中以H2O為氫源,實驗驗證了溶液和氣相中H2的生成,同時生成副產物三苯基氧化膦(圖2a)。這表明,所提出的自由基PPh3-OH中間體是可以生成的,并且它有足夠的壽命,因此與這種H供體的分子間反應是可行的。受到這一發現的鼓舞,未活化烯烴與水作為氫供體進行了轉移氫化(圖2b),活化H2O的第一個H原子以質子形式釋放。基于此研究決定使用巰基助催化劑,該催化劑能夠通過硫代質子化將質子供體(PPh3-OH2+)轉化為自由基H供體。巰基反過來又能有效地還原烷基自由基。設計過程的關鍵物質是PR3-OH中間體,它應該表現出足夠的反應性,以將其H原子分子間轉移到未活化的烯烴上。選擇4-烯丙基甲苯(1a)作為模型底物,評價了定向自由基烯烴轉移加氫的可行性。得到了86%的分離收率獲得加氫產物2a。為了了解H給體的結構和H原子親和力,進行了DFT計算(圖2c)。P1和P4形成的H原子供體的鍵能最低,將H原子轉移到芳基取代基的鄰位會導致更穩定的結構。而由于分子內HAT的非線性,我們沒有發現這個過程的任何過渡態,因此環己二烯基自由基沒有進一步被認為是H原子的供體。
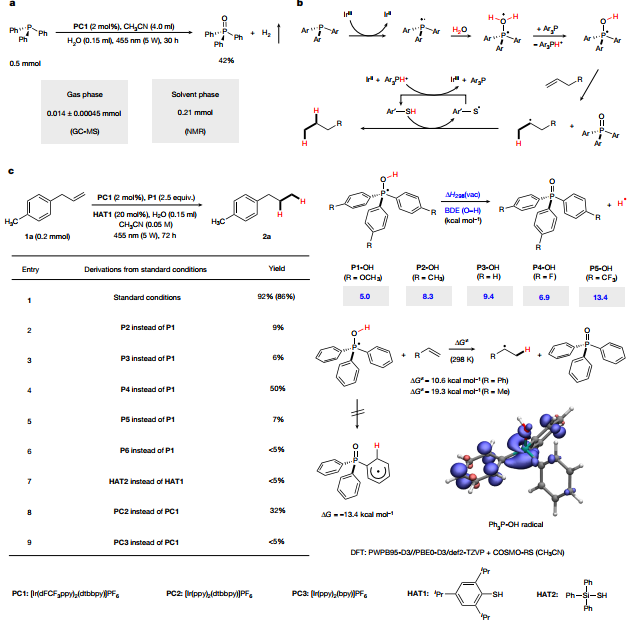
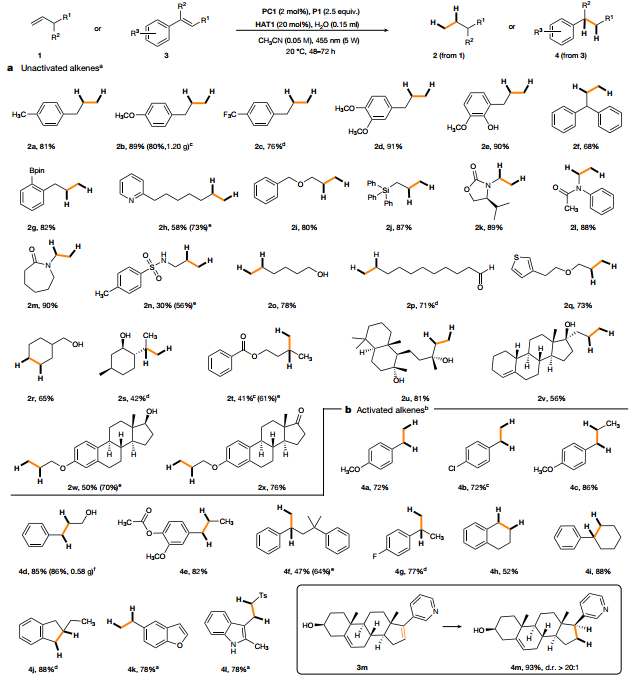
底物適用性
在優化條件下,具有不同官能團的各種非活化烯烴均可得到有效的氫化反應。烯丙芳烴在芳烴部分攜帶供電子或吸電子取代基,從而獲得相應的高收率丙烯2a-2f(圖3a)。自由基加氫與常用的官能團包括硼酸松醇酯(2g)、吡啶(2h)、醚(2i)、三苯基硅基(2j)、惡唑烷酮(2k)、酰胺(2l和2m)、磺酰胺(2n)、游離醇(2o和2r)、醛(2p)和噻吩(2q)基團相容。二取代烯烴也可以被還原(2s和2t)。溫和的方案也允許更復雜的帶有末端未活化雙鍵的化合物的后期氫化,如烯丙雌醇(2v),β-雌二醇(2w)和雌二醇衍生物(2x)。各種苯乙烯衍生物,包括α-和β-取代的同族化合物,以及三取代體系,可以以中等到優異的收率降低(圖3b)。
芳烴的氫化反應為通過易于接近的平面芳香族化合物構建三維結構提供了一種原子經濟、直接有效的途徑。然而,通過H原子轉移還原芳烴比烯烴加氫更困難。而計算表明:分子內H轉移到PAryl3-OH自由基中間體中的芳烴部分在熱力學上是可行的,因此進一步嘗試了具有挑戰性的芳烴氫化(圖4)。萘(5a)及其具有酯(5b)、氰基(5c)和羥基(5d)的衍生物可以氫化得到相應的四氫萘,產率很高。具有吸電子取代基的萘在取代芳烴環上進行了區域選擇性去芳化。含有供電子甲基或甲氧基的萘衍生物(5f和5g)提供了兩種可能的四氫萘的混合物。區域選擇性問題通過DFT計算進一步研究。所有的HATs都是放熱的,并且發生的勢壘較低。HAT到C4位的勢壘最低,但氫轉移到C8和C5導致其他區域異構體的勢壘也相似。
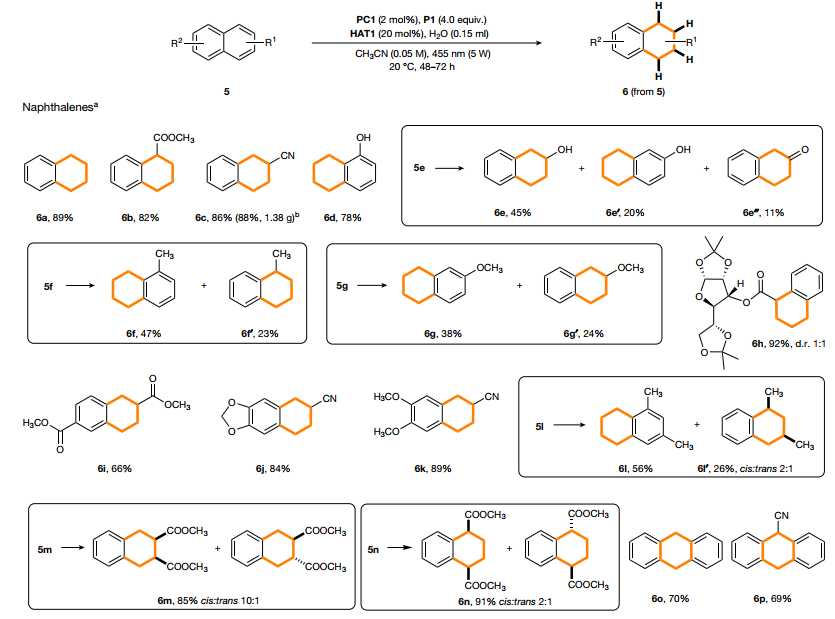
應用和機理研究
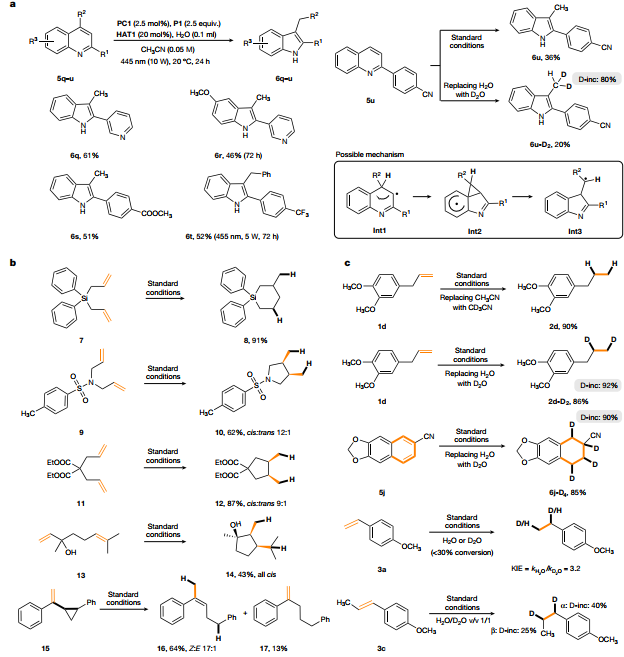
這種光催化膦介導的水活化體系具有獨特的H原子還原能力,其中氫化通過自由基中間體進行,通過實現喹啉類化合物的直接骨架編輯進一步驗證了這一能力(圖5a)。這種氫化重排對于任何其他自由基還原體系都是未知的,并且不能通過過渡金屬介導的氫化過程來實現。一些吲哚衍生物可以通過相應的喹啉衍生物的還原環收縮直接構造(圖5a)。用D2O代替H2O表明P1-OH中間體的初始HAT和硫醇共催化劑的最終HAT都發生在同一個碳原子上。進一步探索了兩種不同π系統的相對反應性。2-乙烯基萘(3n)中的烯烴部分比萘核心反應性更強,使用PPh3 (P3)得到的2-乙基萘具有完全的化學選擇性。通過對4-烯丙基苯乙烯中活化端烯烴與未活化端烯烴的對比,發現以較溫和的P3為介質,苯乙烯雙鍵加氫具有良好的化學選擇性,制得烯丙基(4-乙基苯基)醚的產率為82%。自由基型加氫的另一個優點是,相對于已建立的Pd/Rh/Ir催化過程,通常在H2氣體中進行,研究了伴隨環化或開環的加氫過程。同時,這些研究為這些轉變的激進性質提供了進一步的實驗支持(圖5b)。實驗表明,H2O是加氫過程中唯一的氫源,不涉及溶劑(乙腈)(圖5c),這表明這種自由基加氫可以利用便宜的D2O制備氘化化合物。
小結
在室溫下,原位生成的PR3-OH自由基可以作為HAT試劑與各種烯烴和萘反應,生成相應的H原子加成加合自由基。關鍵的PR3-OH自由基,可以被認為是形式的“自由”氫原子,很容易通過光催化膦介導的水活化產生。巰基用作π體系自由基加氫的催化共還原劑,將最初生成的PR3-OH2自由基陽離子中間體轉化為自由基氫原子給體。這種共催化方法確保了水的兩個H原子都可以用作還原π體系中的H原子供體。該策略將為未開發的“氫原子自由基化學”打開大門。https://doi.org/10.1038/s41586-023-06141-1Jingjing Zhang et al. Photocatalytic phosphine-mediated wateractivation for radical hydrogenation.Nature (2023).DOI:10.1038/s41586-023-06141-1












