“手性(chirality)”是微觀小分子和宏觀物質的一種基本屬性,就像人們的左右手,互為鏡像異構體,但是左手與右手無法相互重疊。手性催化劑(具有共同結構特征并在一系列反應中具有對映選擇性的催化劑)大大改變了化學研究的格局。利用光作為外部刺激來克服基態反應性邊界是當代催化學的核心研究方向。
近年來,人們通過光激活的激發態催化獲得了新的反應模式,但基態優勢催化劑的選擇性是否能與之匹配尚不清楚。盡管基態循環對光生中間體的截留部分解決了這一挑戰,但同時調節反應活性和選擇性的單一手性光催化劑卻很少。到目前為止,精確的供體-受體識別基序仍然是對映選擇性光催化劑設計的關鍵。
在此,來自德國明斯特大學Johannes Neugebauer和Ryan Gilmour團隊展示了具有明確光物理性質的Al-salen配合物,可用于環丙基酮的高效光化學去甲基化。在λ=400 nm(紫光)下照射可提高商用催化劑的反應活性,從而同時調節反應活性和對映體選擇性。這就避免了定制催化劑-底物識別圖案的需要。據預測,這項研究將促使人們重新評估激發態過程中許多古老的(基態)手性催化劑,最終確定在兩種反應模型中均可被視為最佳的候選催化劑。

技術優勢:
本工作推進了Al-salen框架作為手性光催化劑的發展,它允許利用酮官能團作為識別元素,從而向合成有用的去甲基化邁出了重要的一步。其次,這項研究提供了一種新的去甲基化反應框架(C-C鍵斷裂),即通過斷裂/重組C-C鍵而不C-H鍵或C=C鍵來實現去甲基化。這原則上為完全取代的立體中心的去甲基化打開了大門。最后,也是最重要的一點,Al-salen配合物作為手性光催化劑的鑒定是一個潛在的突破,因為它們具有合成的可及性,并且在整個反應平臺上的立體誘導得到了驗證--這也是本文的催化優勢所在。
環丙烷的脫乙酰化驗證salen光催化的概念
利用光作為外部刺激來克服基態反應性邊界雖然成功突出了光催化在形成新鍵方面的有效性,但活化的非共價性質,加上生成的中間體的高反應性,使對映體控制成為一個明顯的挑戰。但是,當存在互補(H鍵)識別基序時,在單一手性光催化劑的支持下,可以實現顯著水平的對映誘導。將這個模型擴展到包括具有常見官能團的基板,以進行識別是非常有吸引力的,并最終導致更普遍的手性光催化劑的識別。不過,本文的目的是確定基態識別模式,可以在激發態模型中復制。這使得作者在創造一個新興手性藍圖中的Lewis酸-Lewis堿組分時,探索了富含地球的鋁的強親氧性。并且手性Al-Salen配合物可以通過電子轉移到羰基而有效地用于環丙基酮的去甲基化,這將通過底物配位和隨后的配體生色團激發以及在手性環境中的電子轉移來實現。

圖 對映選擇性光催化
驗證手性光催化劑對映誘導的假設
作者使用丙酮中的商用Al-Salen配合物Al-1,在-70 ℃下催化環丙烷rac-1脫烷基。根據光催化劑和底物的吸收光譜,在400 nm波長下照射反應混合物,實現了催化劑的選擇性激發。4.5小時后,分離出對映體富集產物(+)-1,收獲率率為78%。并且,作者還進行了反應優化過程,首先加入一種可溶性鹽以穩定電荷分離的中間產物。n-Bu4NCl的加入提高了產率(80%)和對映選擇性。通過反應監測觀察到rac-1的快速去甲基化,耗竭量為(-)-1,并在100分鐘后完成。研究了溫度對映體選擇性的影響,揭示了一個經典的溫度依賴關系。
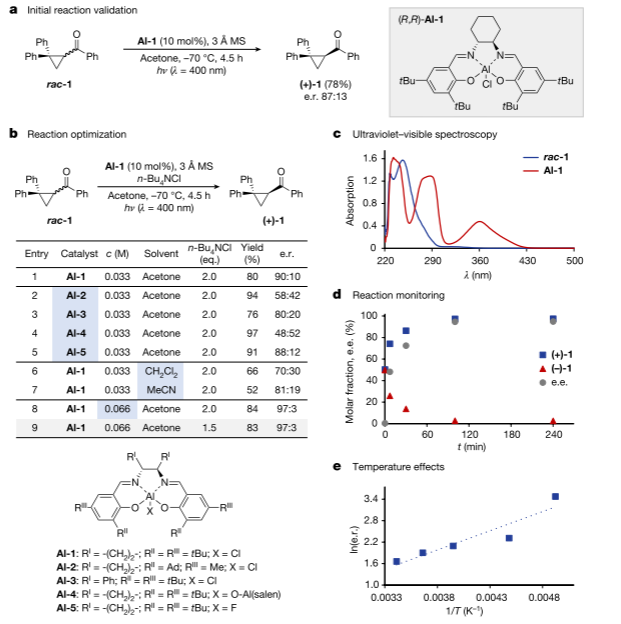
圖 利用Al-salen光催化技術使環丙基酮脫烷基化
環丙基酮的脫烷基的局限性
在確定了優化條件后,對該方法的范圍和局限性進行了研究。對位取代底物具有較高的收率和對映體選擇性,對映體富集1的單晶X射線分析使絕對構型歸屬為(S)。為了擺脫geminal-substitution,本研究還在該salen光催化平臺的框架內探索了非對稱取代的環丙烷。作者猜測,通過正式的動力學解析過程,可以獲得由對映體非對映異構體混合物組成的光致變性成分。
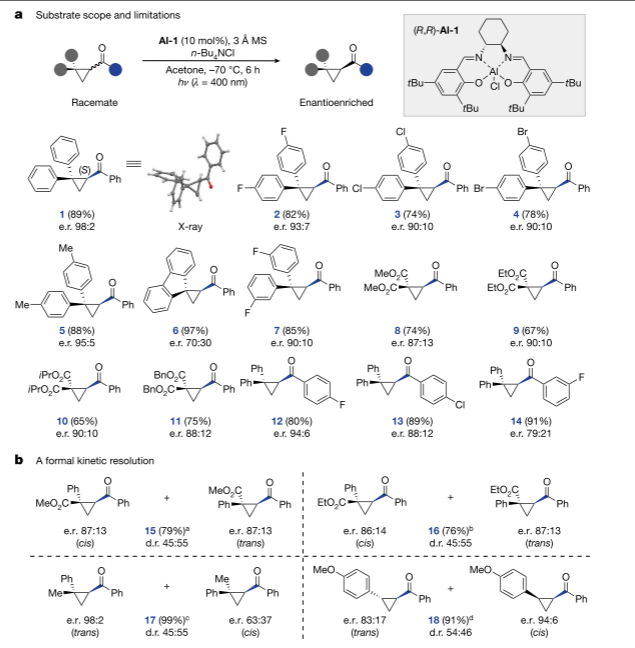
圖研究環丙基酮的脫烷基范圍
揭示Al-salen光催化的脫鈣作用的機理
為了揭示Al-salen光催化的脫鈣作用的機理,并為前面工作假設提供支持,作者將紫外可見光譜數據、反應進程監測和溫度數據與實驗觀察結果進行了對比。結果發現,在沒有Al-salen或光的情況下,脫鈣化反應被完全抑制,這使得環丙烷rac-1得以定量回收。此外,漏掉分子篩會降低反應效率,突出了水對反應過程的不利影響。所以作者又研究了電荷轉移過程的可行性。此外,為了進一步研究脫甲基化機理,作者還進行了scalemic 19和20的對照反應,并證實沒有發生可檢測到的背景外消旋化。
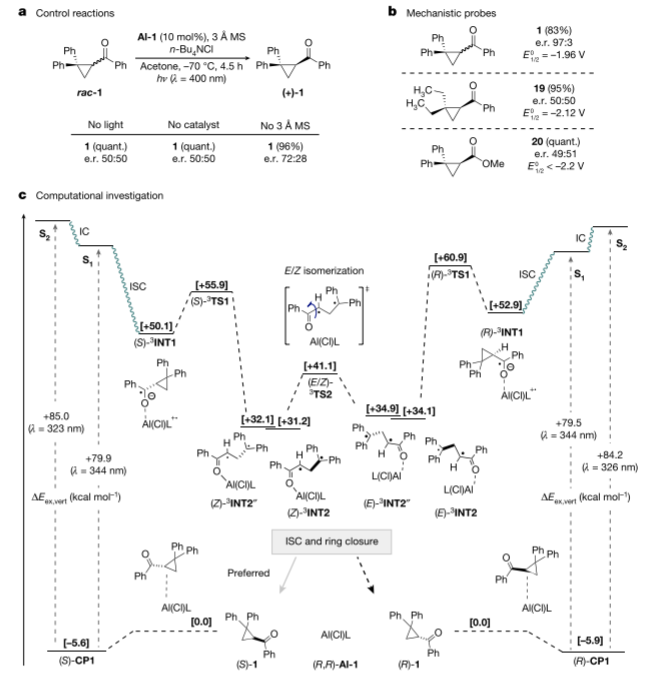
圖機理研究
驗證獲得光學富集、官能度高的環丙烷衍生物的合成實用性
為了證明上述方法在獲得光學富集、官能度高的環丙烷衍生物方面的合成實用性,作者進一步修飾了(+)-1和(+)-8/(+) -10的gem-diaryl和gem-diester衍生物。苯酮發色團在操作上的簡單裂解被認為是有利的。因此,通過Beckmann重排或Baeyer-Villiger氧化直接轉化為酰胺或酯的方法得到了驗證。Johnson-Corey-Chaykovsky 環氧化和還原(+) -1生成(+)-22和(+)-23的過程完全是非對映選擇性的,還原/環化過程也是如此,可獲得融合的內酯衍生物(+)-25。(+)-8的廣泛還原也很有效,并使三元醇(+)-26的制備在不影響光學純度的情況下進行。
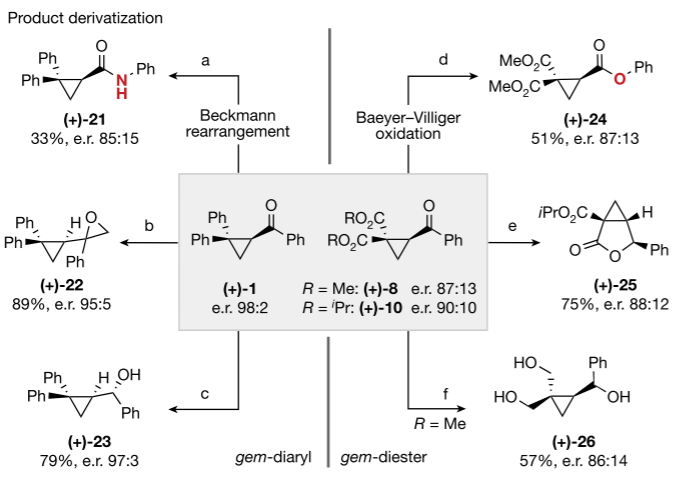
圖Al-Salen光催化去乙酰化對映體富集環丙基酮的功能化研究
來自德國明斯特大學Johannes Neugebauer和Ryan Gilmour等人的工作描述了使用雙功能Al-Salen催化劑在可見光介導的環丙烷脫甲基化反應。作者提出了一種概念新穎的不對稱光催化方法,該方法將Al的Lewis酸性質所提供的酮的LUMO降低激活與環丙基酮的可逆均裂作用以及配體提供的不對稱誘導結合起來。這種流形不同于手性H鍵給體-受體能量轉移和基態手性LA激活過程。總之,Salen催化劑可以用來控制激發態對映體選擇性的發現是非常有價值的,所描述的轉化過程也是非常有趣。
參考文獻:
Carina Onneken, Tobias Morack, Julia Soika1, Olga Sokolova1, Niklas Niemeyer, Christian Mück-Lichtenfeld, Constantin G. Daniliuc, Johannes Neugebauer*, Ryan Gilmour*. Light-enabled deracemization of cyclopropanes by Al-salen photocatalysis. Nature, (2023). https://doi.org/10.1038/s41586-023-06407-8.











