
特別說明:本文由學研匯技術 中心原創撰寫,旨在分享相關科研知識。因學識有限,難免有所疏漏和錯誤,請讀者批判性閱讀,也懇請大方之家批評指正。
原創丨彤心未泯(學研匯 技術中心)
編輯丨風云
脂肪族胺和氮雜環化合物在天然產物、藥物、農用化學品和其他生物活性化合物中的廣泛存在,具有十分重要的應用價值。醫學研究對更復雜的三維結構和旋光性胺的需求不斷增加,推動了開發各種實用方法來構建C(sp3) -N鍵)。氨基氮原子富含電子的特性使它們成為強親核試劑,可以攻擊烷基鹵化物、醇衍生物和羰基的極化化學鍵,從而形成新的C(sp3) -N鍵。在C(sp3) -N鍵構建中加入無處不在的非極性C - C鍵可以直接用于修飾分子骨架,從而獲得傳統上具有挑戰性或難以獲得的脂肪胺。
然而,脂肪胺的制備仍存在以下問題:
1、C-C鍵胺化的經典方法的C-C鍵源和N源受限
C-C鍵胺化的經典方法,包括Lossen, Hofmann, Curtius, Beckmann和Schmidt重排,雖然這些經典的轉化是獲得氮插入產物的有力方法,但C-C鍵的來源大多限于酮和羧酸,氮原子的來源僅限于插入一個N原子的氮原子。
2、亟需開發利用原始材料的骨架復雜性來獲得手性胺結構的方法
盡管schmidt型反應、羧酸和酮衍生物的解構C(sp3) -N偶聯等研究試圖解決C-C鍵和C-C胺化中氮原子來源的限制并取得了一定進展,但除了羰基化合物之外,用于胺化的C-C鍵的新來源仍有很大的空間。
3、烯烴是理想的C-C鍵胺化前體,但C-C鍵胺化的研究很少
天然產物中的烯烴部分可能作為理想的C-C鍵胺化前體,但在烯烴基序上安裝氮基團的大多數方法都集中在C-C ?鍵上加成以產生外周胺化產物,相鄰的C(sp3) - C(sp2) ?鍵在C -N鍵構建中受到的關注較少。
有鑒于此,加州大學Ohyun Kwon以及北京大學校友和志奇博士等人報告了溫和反應條件下的臭氧分解和銅催化如何使烯烴C(sp3)–C(sp2)的?鍵斷裂交叉偶聯反應用于構建新的C(sp3)–N鍵。作者已成功將這種非常規轉化用于激素、藥物試劑、肽和核苷的后期修飾。此外,作者將豐富的萜烯和萜類化合物與氮親核試劑偶聯,獲得了人工萜類生物堿和復雜的手性胺。作者應用一種商品化學品α-甲基苯乙烯作為甲基化試劑,在一個合成步驟中直接從經典核苷制備甲基化核苷。本工作的機理研究表明了一種不尋常的銅離子對協同過程。
技術方案:
1、闡明了該策略的研究歷程
為了實現設計,作者首先研究了銅鹽、配體和溶劑的影響,發現可以在溫和的反應條件下高效地進行氨基脫烷基化反應,然后評估了該策略適用的底物范圍。
2、探究了烯烴的底物范圍
作者對一系列萜烯、萜類及其衍生物進行了解構性C-N偶聯處理,得到了各種人工萜類生物堿,證實了無論底物是什么都能獲得良好的產率,但非對映選擇性差異取決于扭轉和空間效應的組合。
3、證實了手性伯胺的合成及其應用
作者以75%的產率從植物酚衍生的鄰苯二胺中制備了伯胺以及一系列手性氨基醇,證實了氨基脫烯化在手性伯胺合成中的應用。此外,作者還證實了該策略在核苷甲基化的應用,并成功構建了萜烯核苷。
4、解析了烯烴胺化的反應機理
作者探究了反應機理表明[CuCl2]-參與了氫過氧化物分解,而[(Phen)2Cu]+參與了C-N耦合,[CuCl2]-同時影響了C-C裂解和C-N偶聯過程。
技術優勢:
1、實現了復雜分子結構的結構與重組
作者提出了不尋常的C-C鍵斷開的C-N鍵偶聯策略用于烷基胺合成,實現了從天然存在的手性分子構建復雜的手性胺。
2、證實了C(sp3) -C (sp2)胺化策略在生物活性試劑合成中具有潛在的實用性
為了解決脂肪族烷基烷比烯烴的烷基C(sp3) -C (sp2)?鍵更易斷裂的根本問題,作者利用臭氧來激活烯烴并促進其C(sp3)–C(sp2) σ鍵斷裂。
技術細節
反應的發展
為了實現設計,作者研究了銅鹽、配體和溶劑的影響。發現在室溫條件下,在乙腈(MeCN)中加入20mol%的CuCl和20 mol %的1,10-phenathroline時,可以在溫和的反應條件下高效地進行氨基脫烷基化反應。在確定反應條件后,評估了多種氮親核試劑與(-)-異戊二醇作為模型烯烴底物的脫烷基C-N偶聯,證實了該方案可用于對映體純吲哚衍生物以及其他重要的取代雜環化合物,包括氮唑、吲哚、咔唑、吡唑和吡咯等。為了證明該方案在藥物發現中的效用,作者將脫烷基C-N偶聯策略應用于復雜生物活性分子的后期功能化。
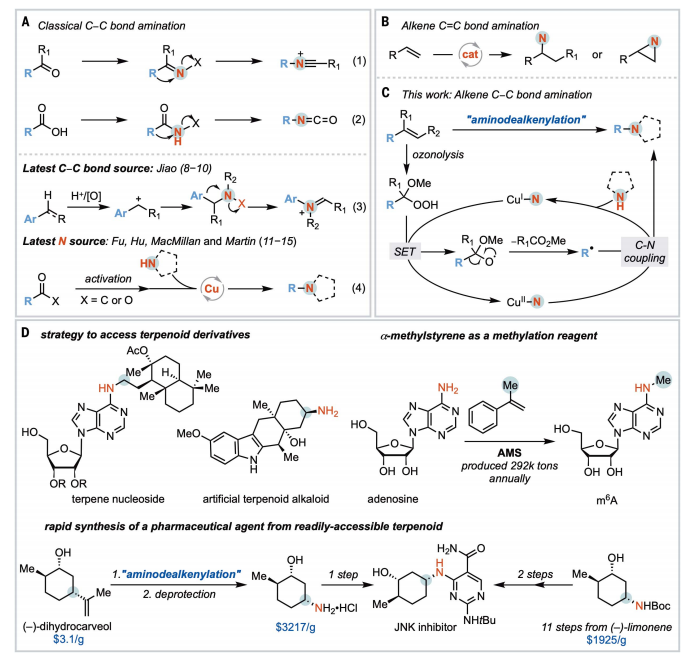
圖 脫烷基C(sp3)-N鍵偶聯的概念與發展
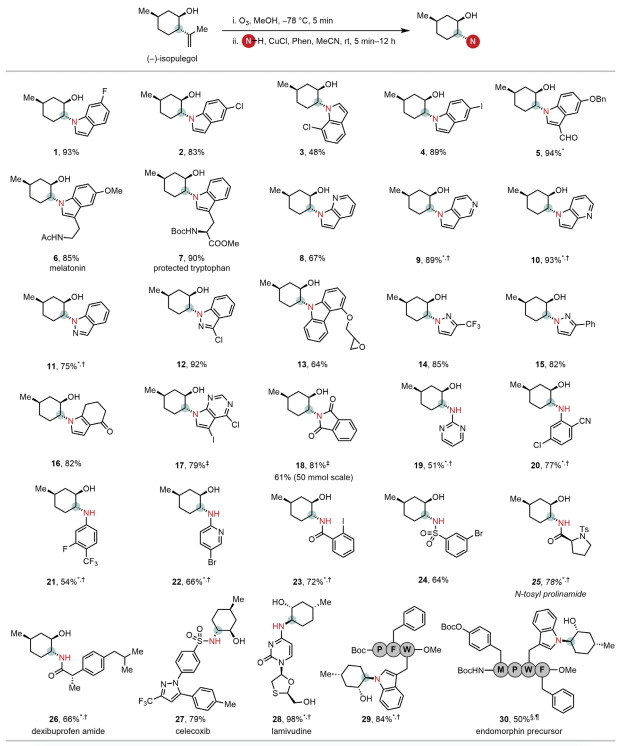
圖 氮親核試劑的底物范圍
烯烴的底物范圍
除了(-)-異戊二醇之外,作者還對一系列萜烯、萜類及其衍生物進行了解構性C-N偶聯處理,得到了各種人工萜類生物堿。這些底物大多是天然產物衍生的單一對映體,或者本身就是天然產物。盡管無論底物是什么都能獲得良好的產率,但非對映選擇性差異很大。觀察到的非對映選擇性與環自由基反應中常見的立體選擇性趨勢一致,其中加成物的立體選擇性是由扭轉和空間效應的組合決定的。
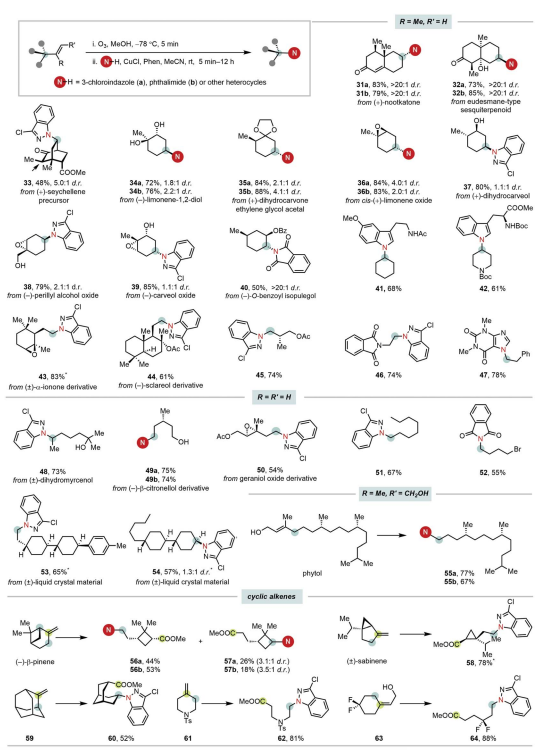
圖 烯烴的底物范圍
手性伯胺的合成及其應用、甲基化反應、萜烯核苷
利用氨基脫烯化將鄰苯二胺單元安裝到手性分子中的能力為合成手性伯胺提供了機會。作者以75%的產率從植物酚衍生的鄰苯二胺中制備了伯胺以及一系列手性氨基醇。萜類化合物中豐富的官能團也通過多樣化促進了更精細的氨基醇的合成。例如,從順式(-)-檸檬烯氧化物經氨基脫烯化、硫代化和脫保護制備了氨基醇。作者還證實了在臭氧和Cu催化劑的作用下,與AMS反應很容易產生1甲基-3-氯茚唑和咖啡因,收率分別為84%和67%,并證實了氨基脫烯化在甲基化反應中的應用。受成功的核苷甲基化的鼓舞,作者使用氨基脫烯化快速構建了萜烯核苷。萜烯核苷類似物可作為生物功能的化學探針,其先天生物活性也可為開發藥物研究中的先導化合物提供平臺。
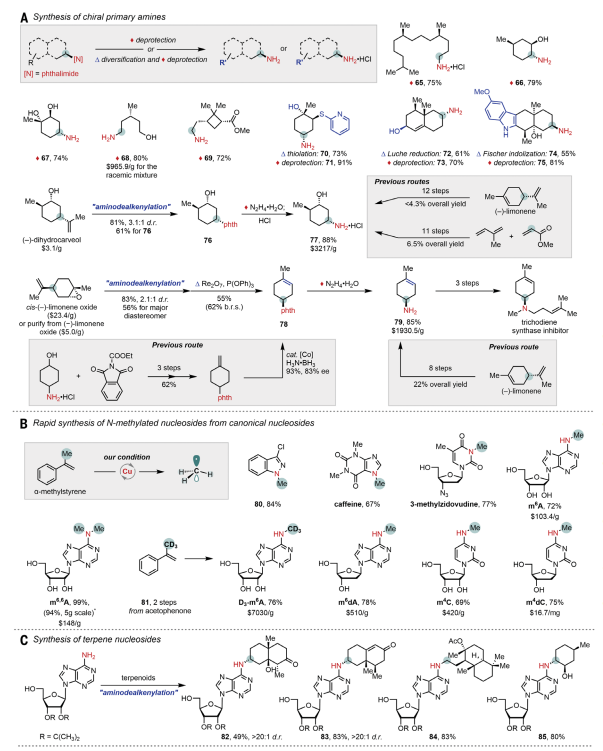
圖 脫烷基C(sp3)-N鍵偶聯在生物活性化合物合成中的應用
機理研究
作者進行了幾次實驗以深入了解反應機理。紫外可見光譜測量表明,離子對絡合物[(Phen)2Cu]+ [CuCl2]-是MeCN中的優勢物種。為了直接探測活性銅的性質,制備了一系列銅配合物,并比較了它們在(-)-二氫卡維醇和鄰苯二胺之間的氨基脫烷基化反應中的性能,表明離子對可能是活性催化物質。為了進一步了解銅催化胺化的機理,通過變時間歸一化分析(VTNA)進行了動力學研究,推測催化劑的靜息態是相應的銅(II)種,催化劑的動力學階數為1.3表明兩種催化物種在循環中運行。[CuCl2]-和[(Phen)2Cu]+的不同反應動力學表明[CuCl2]-參與了氫過氧化物分解,而[(Phen)2Cu]+參與了C-N耦合。由于C-C裂解發生在C-N偶聯之前,[CuCl2]-同時影響了C-C裂解和C-N偶聯過程。
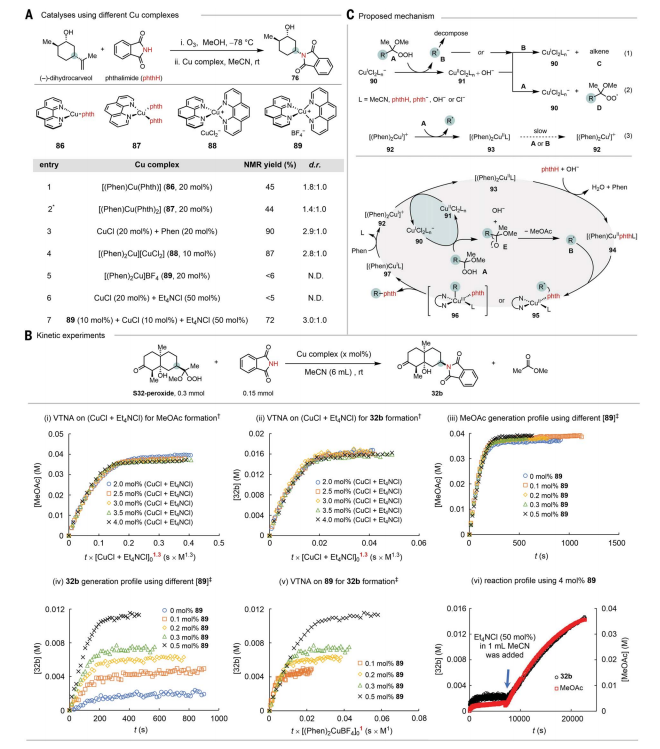
圖 機理研究
總之,作者提出了[CuCl2]--[(Phen)2Cu]+協同催化的參與,實現了溫和條件下烯烴C(sp3)–C(sp2)的鍵斷裂交叉偶聯反應和新的C(sp3)–N鍵的合成。考慮到通過不尋常的烯烴骨架斷裂模塊化引入氮部分的直接性質,預計銅催化脫烷基C-N偶聯將在制備復雜的生物活性三維分子和有機合成和藥物化學中的光學活性胺中具有廣泛應用。
參考文獻:
ZHIQI HE, et al. Aminodealkenylation: Ozonolysis and copper catalysis convert C(sp3)–C(sp2) bonds to C(sp3)–N bonds. Science, 2023, 381(6660): 877-886
DOI: 10.1126/science.adi4758
https://www.science.org/doi/10.1126/science.adi4758











