
特別說明:本文由學研匯技術中心原創撰寫,旨在分享相關科研知識。因學識有限,難免有所疏漏和錯誤,請讀者批判性閱讀,也懇請大方之家批評指正。
不清晰之機制
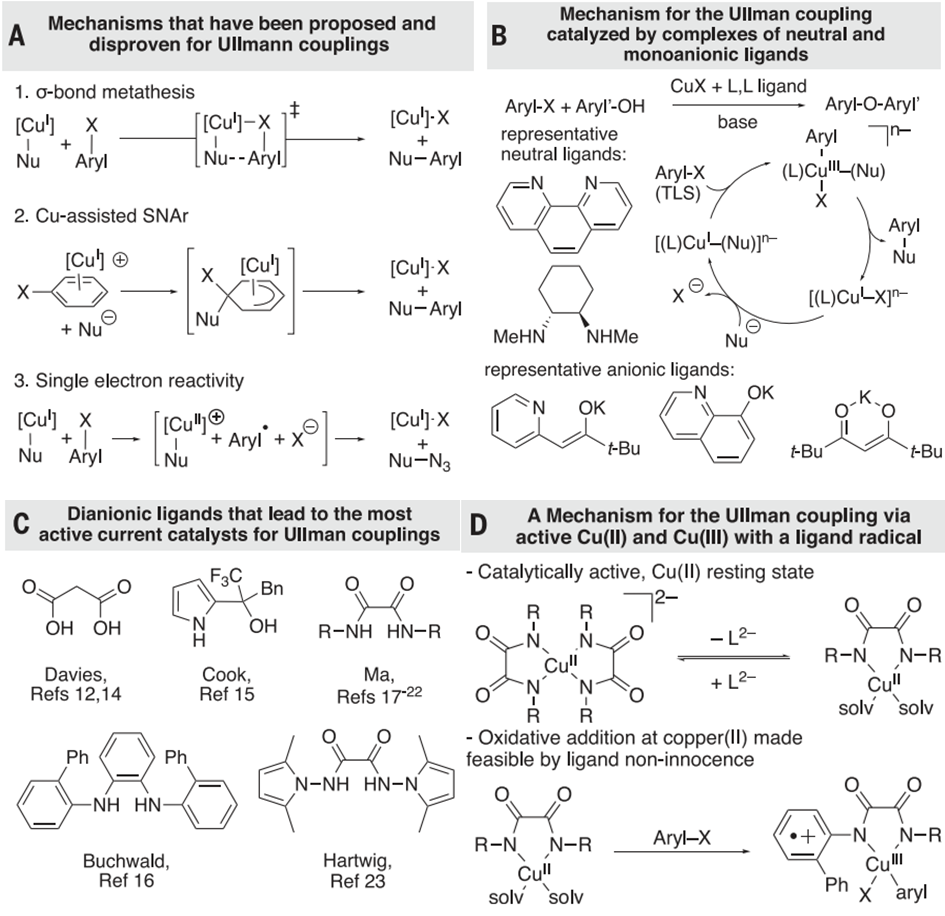
芳基鹵化物親電體和雜原子親核體之間的金屬催化交叉偶聯反應是有機合成領域(包括藥物合成、材料化學和天然產物合成等)中一種重要的方法,這種反應利用金屬催化劑的作用,使芳基鹵化物親電體和雜原子親核體之間發生反應,通過此反應,可以構建復雜的有機分子結構,擴展有機合成的化學空間。此外,金屬催化交叉偶聯反應還具有高效、高選擇性和環境友好的特點,成為現代有機合成中不可或缺的工具。目前常用的金屬催化劑通常是過渡金屬,如鈀、銅等,能夠促進反應的進行,提高反應的效率和選擇性。但與鈀催化的偶聯相比,由于銅配合物的順磁性,導致在光譜上識別,因此銅催化偶聯的機制知之甚少。目前,已知的反應機制包括σ鍵復分解,芳烴π配位激活碳-鹵素鍵,或電子轉移形成芳基自由基、Cu(I)配合物與中性或陰離子結合的機制等(圖1)。但沒有關于催化劑高活性的機制解釋的報道。
大佬之思路
基于此,美國加州大學伯克利分校John F. Hartwig教授團隊發現草酰胺配體的配合物催化芳基鹵化物與酚和其他可能的親核試劑的交叉偶聯的新機制(圖1D),其機制不同于烏爾曼型偶聯反應中Cu(I)和Cu(III)中間體的機理。該機制經歷了一個協調的,決定速率的銅插入芳基鹵化物的碳-鹵素鍵的過程。Cu(II)草酰胺配體催化烏爾曼偶聯,通過芳基鹵化物與Cu(II)的協同氧化加成,形成高價物質,該物質通過草酰胺配體上的自由基特性而穩定,從而形成芳基醚中的C-O鍵。最終Cu(II)草酰胺配合物在空氣條件下催化偶聯,并催化了周轉量超過1000的氧化苯酚與芳基氯親電體的偶聯反應。相關結果以《Cross-coupling by a noncanonical mechanism involving the addition of aryl halide to Cu(II)》為題發表在Science上。以芳基溴和酚之間形成聯芳醚的反應為模型反應進行機理研究。由碘化銅(I)和雙-(2-苯基苯基)草酰胺催化1-溴-4-氟苯與苯氧化鉀的偶聯反應生成4-氟聯苯醚,產率為98%(圖2A)。對單陰離子配體的研究表明,酚類化合物的偶聯是通過將芳基鹵化物氧化加成到Cu(I)苯氧化合物絡合物上而發生的,因此研究首先嘗試生成一種由單或雙陰離子形式的草酰胺配體結合的Cu(I)苯氧化合物絡合物,并測試其與芳基鹵化物的反應性。在室溫條件下,1-溴-4-氟苯(1)與5和苯氧化鉀的混合物生成少量芳醚(圖2B)。而100°C處理樣品后,雖然溶液中不存在Cu(I)苯氧化物絡合物,但也會形成產率為75%的聯芳烴醚3和產率為18%的氟苯,說明這些Cu(I)物種不是催化過程中的中間體。
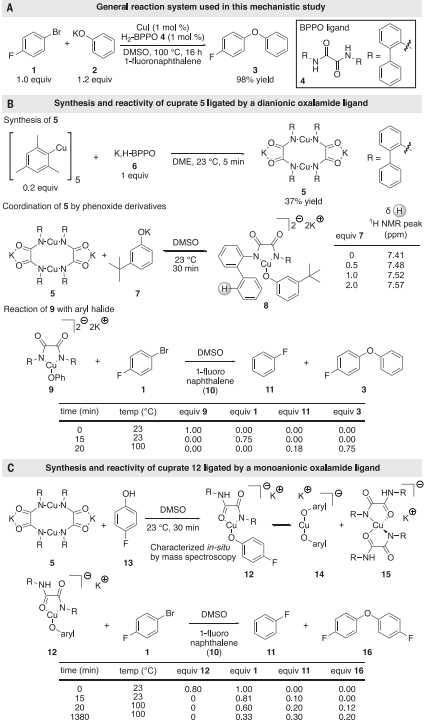
圖 2:草酰胺配體Cu(I)配合物的合成及其反應性Cu(II)配合物的鑒定和反應,評價其在催化反應中的中間作用使用EPR光譜探測催化反應中的Cu(II)配合物(圖3A)。在DMSO中100°C加熱處理20分鐘后,芳烴鹵化物1、苯氧化合物2、碘化銅和草酰胺4產生的冷凍反應混合物的EPR信號對應于一種4個氮原子結合的銅(II)二草酰胺配合物(圖3B)。Cu(II)配合物可以引發由Cu(I)/Cu(III)偶對催化的反應,因此進一步評估了Cu(II)配合物是真正的催化劑還是還原為Cu(I)的預催化劑(圖4A)。如果配合物17是預催化劑,并且比偶聯反應更快地轉化為活性催化劑,則在催化劑活化步驟中會消耗等摩爾量的銅試劑,導致聯芳醚的產率較低,會觀察到一個誘導期。結果發現聯芳醚的產率接近99%,與17的中間作用或由17可逆形成機制一致。動力學研究(圖4B)表明4-氯苯氧化鉀的反應為零級,反應的發生與催化劑濃度呈線性關系,盡管有明顯的非零截距。CV表明17被氧化為Cu(III)種和相應的17被還原為Cu(I)種都是可逆的,并且相隔1.81 V。這一分離結果表明,17的兩個等價物歧化成Cu(I)和Cu(III)的速率大于41 kcal/mol,這為Cu(II)歧化產生活性催化劑提供了有力的證據。
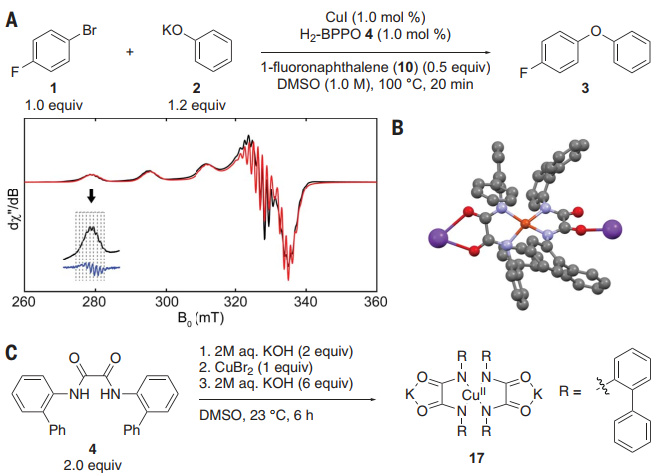
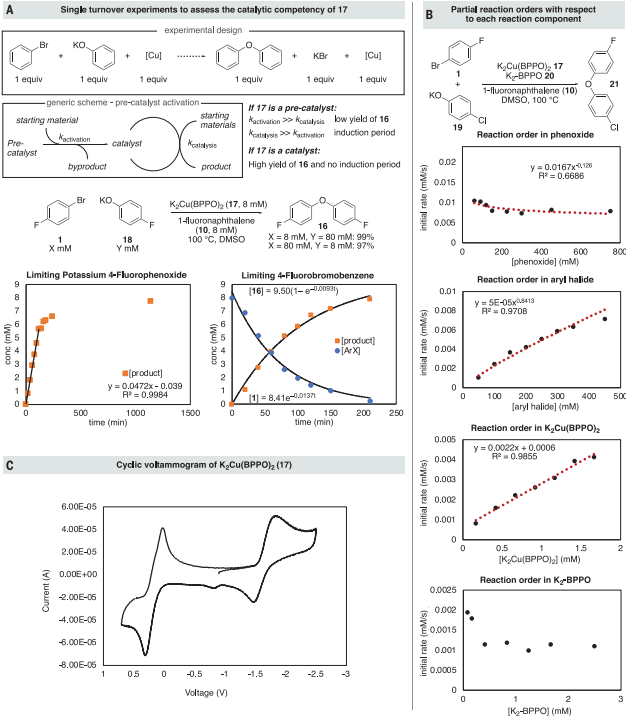
圖 4:機理實驗確定的靜態,周轉限制步驟,和預平衡圖5A顯示了Ullmann耦合的四種機制。為了區分這些機制,進行了一系列進一步的實驗。(i)只有當苯氧化合物在靜止狀態下與銅結合,并通過限制周轉的步驟保持結合時,σ鍵復分解機制才與該研究的動力學數據一致。當銅與芳基鹵化物反應時,沒有檢測到苯氧化合物的性質對反應速率的影響(圖5B),證實了苯氧化合物衍生物與Cu(II)配合物17沒有結合。(ii)進一步測量了13C KIE(圖5C)以確定在Cu(II)和芳基鹵化物之間的限速反應中是否發生了芳烴配位或C-X鍵的斷裂,13C KIE值與芳基碘化物氧化添加到Cu(I)配合物的KIE值相當,排除了芳基鹵化物在親核芳香族取代之前的不可逆結合。(iii)通過銅(II)配合物催化苯氧化合物與芳基鹵化物的偶聯來評估電子轉移機制(圖5D)。排除了電子轉移機制。最終,研究發現所有的數據都與第四種機制一致,即芳基鹵化物與草酰胺配體的Cu(II)配合物的協調,決定速率的反應,以切割碳-鹵素鍵。
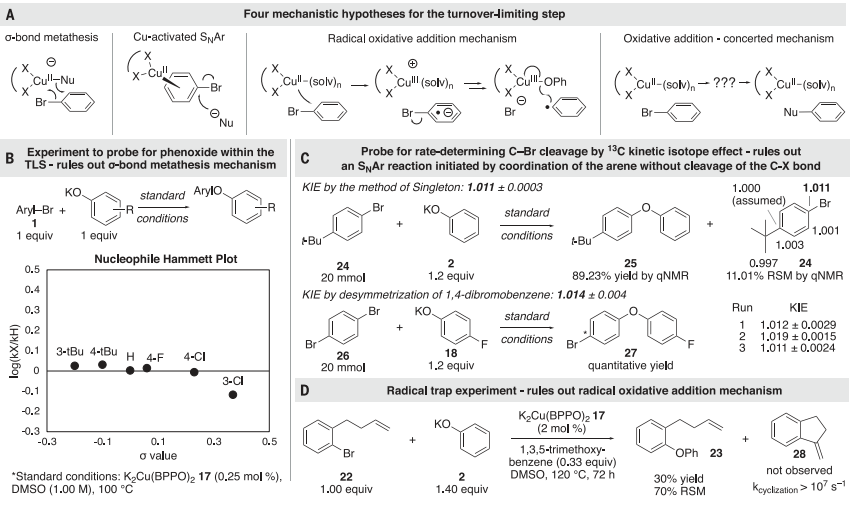
圖 5:機制研究以探討靜息狀態和失誤限制步驟的性質進一步,研究通過DFT計算評估了Cu(II)與芳基鹵化物反應裂解碳-鹵素鍵的機理。研究了通過協同氧化加成的步驟將Cu中間體插入到芳基鹵化物的碳-鹵素鍵中的可行性。圖6A顯示的計算的反應能量與實驗結論一致,即Cu(II)在速率決定步驟中切割碳-鹵素鍵,并表明這種鍵的切割可能通過氧化加成發生。
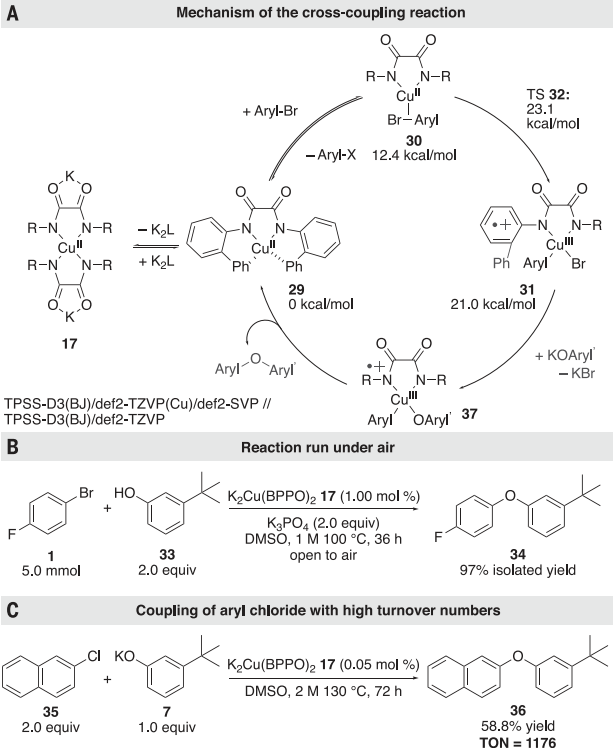
應用及展望
最后實驗探究了Cu(II)的靜態對空氣和歧化反應穩定以探索其適應應用潛力。在130℃僅含百萬分之500的純17作為催化劑條件下,2-氯萘與3-叔丁基苯氧化鉀偶聯反應對應的,聯芳醚36的收率為59%,得到>1000次周轉,表明其穩定性及高活性,展現出應用潛力,為下一代銅或其他金屬催化劑配體的發展提供了參考。https://www.science.org/doi/10.1126/science.adi9226Connor P. Delaney et al. Cross-coupling by a noncanonical mechanisminvolving the addition of aryl halide to Cu(II).Science (2023).DOI:10.1126/science.adi9226














